Борис Кудрявцев - Первоначала вещей [Очерк о строении вещества]
- Название:Первоначала вещей [Очерк о строении вещества]
- Автор:
- Жанр:
- Издательство:Молодая гвардия
- Год:1955
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Борис Кудрявцев - Первоначала вещей [Очерк о строении вещества] краткое содержание
Первоначала вещей [Очерк о строении вещества] - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Если бы мы построили микроскоп, в который можно было бы видеть отдельные молекулы, и стали бы с его помощью рассматривать спокойный воздух или какой-либо газ, то обнаружили бы в «спокойном» воздухе или газе невообразимую сутолоку и суету. Молекулы газа движутся беспорядочно по всем направлениям с самыми различными скоростями. На первый взгляд здесь нет никакого порядка, никаких правил движения. Есть молекулы быстрые, есть и молекулы медленные; и те и другие движутся по всем направлениям. Однако если измерить скорости большого числа молекул, то окажется, что очень быстро и очень медленно движется совсем небольшая доля молекул.
Важный для науки закон, который указывает, как распределяются молекулы по скоростям (то-есть сколько молекул движется медленно, сколько — быстро), был найден английским физиком К. Максвеллом.
По этому закону подавляющее большинство молекул движется со скоростями, мало отличающимися друг от друга. Таким образом, без большой ошибки можно считать, что все молекулы движутся с одной и той же средней скоростью .
Сказанное можно пояснить таким примером. Если собрать всех только что призванных в армию солдат одного года рождения, построить их рядами, так, чтобы в каждом ряду стояли солдаты одного роста, затем ряд самых высоких поставить справа, а самых низких слева, то окажется, что новобранцев очень высокого и очень маленького роста будет только несколько человек, а чем ближе к середине, тем длиннее будут ряды. Большинство призывников имеет близкий к среднему рост. Это правило будет оправдываться всегда, когда мы будем брать достаточно большое количество призывников. Если же мы захотим проверить сказанное, взяв десять-одиннадцать призывников, то можно случайно встретиться со значительными отклонениями от этого правила. Точно так же и замена различных скоростей молекул средней скоростью не будет приводить к ошибкам только в том случае, если молекул достаточно много, потому что тогда доля молекул со скоростями, значительно отличающимися от средней, будет невелика. Но даже в очень небольшом количестве газа, например в объеме, равном булавочной головке, содержится громадное число молекул, исчисляющееся цифрой с 16 нулями. Поэтому во всех практических случаях можно без существенной ошибки считать, что все молекулы движутся с одной и той же средней скоростью.
Какова же величина средней скорости движения молекул газа?
У разных газов она различна.
Самые быстрые молекулы — молекулы легкого газа водорода. Медленнее движутся молекулы кислорода. Еще медленнее — молекулы углекислоты, тяжелого газа, образующегося при многих химических превращениях и, в частности, при горении.
При обычной температуре молекула водорода пробегает около 2 километров в секунду, то-есть около 7 000 километров в час (рис. 11).
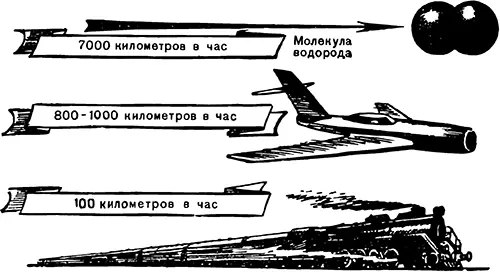
Рис. 11. При обычных температурах молекулы водорода движутся быстрее самолета и поезда.
Молекулы кислорода совершают за 1 секунду путь около 500 метров, то-есть около 1 800 километров в час. Скорость движения молекул углекислоты — 1 200 километров в час. Еще медленнее движутся молекулы некоторых сложных веществ; например, молекулы вещества, называемого карбонилом никеля, проходят за час меньше 600 километров. Такую молекулу легко обгонит современный самолет.
Эти цифры вызывают законное удивление. В самом деле, молекулы водорода, двигаясь беспрепятственно, облетели бы вокруг Земли по экватору всего за 6 часов. Даже медленная молекула углекислоты совершила бы это путешествие меньше чем за двое суток.
С другой стороны, мы знаем, как медленно распространяются запахи. Если на некотором расстоянии от нас разольют бензин, то для того, чтобы запах дошел до нас, необходимо некоторое время. Но ведь скорость распространения запаха — это и есть как будто скорость движения молекул пахучего вещества в воздухе. Как же примирить быстрое движение молекул, проходящих сотни метров в секунду, с медленным распространением запаха?
«Очевидно, что отдельные атомы воздуха, взаимно приблизившись, сталкиваются с ближайшими… вторые атомы друг от друга отпрыгнули, ударились в более близкие к ним и снова отскочили; таким образом, непрерывно отталкиваемые друг от друга частыми взаимными толчками, они стремятся рассеяться во все стороны», — писал М. В. Ломоносов.
Распространение одного газа в другом, вызванное беспорядочным движением молекул, называется диффузией. Теперь нам понятно, почему диффузия происходит медленно.
Соударение молекул! Вот в чем причина медленности диффузии. Хотя молекулы газов и движутся с очень большими скоростями, они проходят без соударения только очень короткие пути — миллионные доли сантиметра.
Соударения резко изменяют направление движения молекул и придают их путям причудливую, замысловатую форму.
Таким образом, двигаясь очень быстро, но непрерывно меняя направление своего движения, молекулы как бы «толкутся» на месте. В этом суетливом движении молекулы медленно перемещаются вперед.
Чем чаще происходят соударения, тем медленнее диффундирует газ. В окружающем нас воздухе соударения молекул происходят очень часто. Если бы мы попытались сосчитать удары, которые испытывает молекула только за одну секунду, и при этом условились тратить одну минуту на сосчитывание ста ударов, то для этого понадобилось бы около двухсот лет.
Молекулы, летящие со скоростью пули, бесчисленные соударения, причудливый узор пути, своеобразный закон распределения молекул по скоростям… Все это может заронить сомнение в реальности наших объяснений.
В науке установилось золотое правило — проверять опытом все предположения, как бы остроумны они ни были. Нет оснований делать исключение и для молекул. Надо измерить скорости движения мельчайших частиц, проверить, как распределяются эти скорости: какая доля молекул движется быстро, какая медленно.
Не фантазия ли это?
Однако как же измерить скорость движения молекул, если молекулы столь малы, что их нельзя рассмотреть даже в самый сильный микроскоп?
Вероятно, многие замечали, что стеклянный колпачок перегоревшей электрической лампочки часто бывает покрыт темным налетом. Отчего возникает этот налет?
Когда электрическая лампочка включена, металлический волосок, от которого исходит свет, сильно накален. От его поверхности непрерывно отрываются атомы металла. Оторвавшись, атомы разлетаются в разные стороны и, ударившись о стенку стеклянного колпачка, прилипают к ней. Так, волосок, теряя атомы, делается все тоньше и тоньше, а на стекле образуется постепенно утолщающийся слой осевших атомов. Когда слой осевших атомов сделается достаточно толстым, его можно будет различить глазом: мы увидим на стекле темный налет. Чем больше осядет атомов, тем темнее будет этот налет.
Читать дальшеИнтервал:
Закладка:
![Обложка книги Борис Кудрявцев - Первоначала вещей [Очерк о строении вещества]](/books/1065461/boris-kudryavcev-pervonachala-vechej-ocherk-o-stroeni.webp)









