Владимир Базылев - Основы общей и экологической токсикологии
- Название:Основы общей и экологической токсикологии
- Автор:
- Жанр:
- Издательство:Литагент СпецЛит
- Год:неизвестен
- ISBN:978-5-299-00410-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Владимир Базылев - Основы общей и экологической токсикологии краткое содержание
Пособие предназначено для студентов, аспирантов и преподавателей экологических и медико-экологических факультетов высших учебных заведений, а также для научных работников и практиков, работающих в области охраны окружающей природной среды.
Основы общей и экологической токсикологии - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Атмосферу можно рассматривать как огромную окислительную систему с высоким содержанием основного окислителя – кислорода. Соединения, содержащие атомы C, H,SиNприродного и антропогенного происхождения, попадая в атмосферу, превращаются в стабильные долгоживущие соединения (например, СО 2)иливкороткоживущие соединения кислотного характера (оксиды азота и серы), которые участвуют в жидкофазных процессах с образованием кислот, удаляемых из атмосферы с осадками. Это и есть кислотные дожди.
В этих превращениях кроме кислорода участвуют озон О 3, гидроксильный радикал НО *, гидропероксидный радикал НО 2 *, органические пероксидные радикалы (ROO *), пероксиацетилнитрат (ПАН), пероксид водорода (Н 2О 2), нитрат-ион 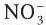 . Наиболее реакционноспособный гидроксильный радикал НО *, он участвует в окислении оксидов азота и серы в азотную и серную кислоты:
. Наиболее реакционноспособный гидроксильный радикал НО *, он участвует в окислении оксидов азота и серы в азотную и серную кислоты:
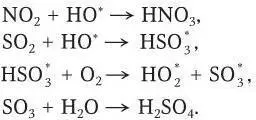
В Средней и Северной Европе, а также Северной Америке кислотные дожди стали важной международной проблемой и даже поводом для конфликтов.
Из всего количества кислот, выпавших с дождями над территорией Центральной Европы, в среднем 2/ 3приходится на серную кислоту, 1/ 3– на азотную.
Многие страны Европы, как бы «экспортирующие» и «импортирующие» серу (имеется в виду поступление и вынос серы через воздушные границы), можно условно разделить на государства с положительным и отрицательным балансом. Так, например, Норвегия, Швеция, Финляндия, Австрия и Швейцария больше получают от своих соседей, чем выпускают через собственные границы. Дания, Нидерланды, Бельгия, Великобритания, Германия и Франция больше направляют выбросов диоксида серы к соседям, чем получают от них.
При изучении кислотности водоемов возникает вопрос, в какой степени кислотность определяется выбросами из антропогенных источников и не связаны ли изменения кислотности с природными факторами. В США проведен глубокий геолого-палеонтологический анализ, результаты которого свидетельствуют о том, что кислотность большинства озер в послеледниковый период была не выше рН 8. В настоящее время для тех же зон кислотность гораздо выше (рН 4,6 – 5,0).
При анализе состава кислотного дождя основное внимание обращается на содержание катионов водорода (Н +), определяющих его кислотность (рН), а также анионов – сульфата 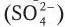 , нитрата
, нитрата 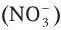 , хлорида (Cl), фосфата , катионов –
, хлорида (Cl), фосфата , катионов – 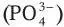 аммония
аммония 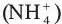 ,
,
натрия (Na +), калия (К +), кальция (Са 2+), магния (Mg 2+). Для суммарной характеристики растворенных ионов иногда используют электропроводность.
При рН 7 среда нейтральна (в дегазированном состоянии), при рН<7 – кислая. Однако это определение кислотности не столь очевидно для природной воды. Вода находится в равновесии с окружающим воздухом, насыщение диоксидом углерода приводит к образованию угольной кислоты с рН 5,6. Это состояние можно считать исходным для определения кислотности природной воды. Как правило, рН большинства рек и озер составляет 6 – 8, при высоком содержании минеральных и органических кислот рН заметно ниже – 3,2. Для засушливых регионов (Индия и другие страны Юго-Восточной Азии) характерны сильнощелочные почвы, и рН вод в них иногда выше 9.
В то же время в природных водах в больших количествах могут присутствовать растворимые карбонаты (обычно их пересчитывают на эквивалентное количество CaCO 3), анионы органических кислот, которые образуются в результате микробиологических процессов, и растворимые гидроксиды металлов. Наличие таких соединений приводит к нейтрализации катионов Н +, поскольку органические анионы связываются в слабодиссоциирующие кислоты, а карбонат-анион переходит в бикарбонат-анион. Поэтому введен термин « кислото-нейтрализующая способность » (КНС) воды, который определяется в мг-экв катионов Н +, необходимых для достижения рН 5,6. Обычно кислото-нейтрализующая способность дистиллированной воды в равновесии с газообразным СО 2равна 0; при наличии указанных выше соединений она больше 0.
Показатель кислото-нейтрализующей способности является наиболее распространенным критерием закисления вод. Разница между суммой катионов (с коррекцией на морскую соль) и радикалами сильных кислот отражает запас или дефицит гидрокарбонатов, а в случае с водами, обогащенными гумусовыми кислотами, – их сумму, т. е. буферную способность системы. Кислото-нейтрализующая способность воды может быть рассчитана двумя способами:
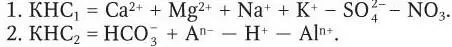
Содержание элементов представляется в эквивалентах и корректируется на устранение доли морских аэрозолей по соотношению соответствующих элементов к хлору. Принимается, что хлориды в воде имеют морское происхождение. Содержание органического аниона (A n-) рассчитывается по концентрации органического вещества (С РОВ):
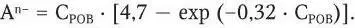
Если химические анализы проведены корректно и баланс ионов сходится, то значения КНС 1и КНС 2совпадают. Американские исследователи экстремальным считают значение КНС – 50 мг-экв/дм 3, норвежские специалисты – 20 мг-экв/дм 3.
Изменение в соотношении молярной концентрации 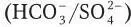 в сторону превалирующего положения сульфатов может являться симптомом закисления вод.
в сторону превалирующего положения сульфатов может являться симптомом закисления вод. 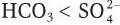 – есть признак переходного состояния водных объектов к закислению.
– есть признак переходного состояния водных объектов к закислению.
Водоемы с различной естественной кислотностью водной среды населяют гидробионты, адаптированные к определенным интервалам концентраций водородных ионов (эвриионные организмы приспособлены к наиболее значительным колебаниям рН водной среды, стеноионные, наоборот, жизнеспособны при незначительных колебаниях рН). В соответствии с предложенной классификацией типов природных водоемов гумидной зоны России в зависимости от фактора рН водоемы различной трофности и состава флоры и фауны подразделяются на нейтрально-щелочные (рН = 6,8 – 8,5), олигоацидные (рН = 6,7 – 5,6), мезоацидные (рН = 5,5 – 4,0) и полиацидные (рН ≤ 4,0).
Читать дальшеИнтервал:
Закладка:










