Ю Корзюков - Болезни аквариумных рыб
- Название:Болезни аквариумных рыб
- Автор:
- Жанр:
- Издательство:Колос
- Год:1979
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ю Корзюков - Болезни аквариумных рыб краткое содержание
Болезни аквариумных рыб - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
После этого пипеткой вносят на дно 2 мл концентрированной соляной кислоты или 3 мл 25 %-ной серной кислоты. Склянку закрывают, содержимое вновь взбалтывают и приступают к титрованию жидкости гипосульфитом. Для этого пипеткой Мора или мерным цилиндром из склянки берут 50 мл испытуемой жидкости, переливают ее в колбу и титруют 0,01 н. раствором гипосульфита до появления светло-желтого окрашивания жидкости, хорошо заметного на белом фоне бумаги, лежащей под колбой. Затем в смесь добавляют 1 см? крахмала (если при фиксации кислорода исследуемой воды растворами хлористого марганца и смеси едкого натра с йодистым калием жидкость не буреет, то раствор крахмала вливают сразу же перед титрованием, отчего она становится темно-синей, и титруют до осветления.
Расчет.Установив количество израсходованного на титрование гипосульфита, определяют содержание растворимого в воде кислорода по формуле:
х = 1,117 * П * К,
где х — количество растворимого в воде кислорода, мг/л;
1,117 — постоянный коэффициент;
П — количество гипосульфита, израсходованного на титрование, мл;
К — поправочный коэффициент гипосульфита.
Определение поправочного коэффициента гипосульфита. В колбу для титрования вносят 10 мл 0,01 н. раствора KIO 3и 0,5 г сухого йодистого калия (KI). После растворения последнего добавляют 2 мл концентрированной соляной кислоты или 3 мл 25 %-ной серной кислоты. Полученную жидкость титруют гипосульфитом, как и пробу на кислород. Затем количество взятого 0,01 н. раствора KIO 3(10 мл) делят на количество миллилитров гипосульфита, израсходованного на титрование. Полученный результат является поправочным коэффициентом гипосульфита.
Жесткость воды определяется количеством растворенных в ней солей кальция и магния. При незначительном содержании их воду называют мягкой, при большом количестве — жесткой. Различают общую, постоянную и временную жесткость воды. Сумма постоянной и временной жесткости составляет общую жесткость. Постоянная жесткость воды зависит от содержания в ней сульфатов и хлоридов кальция и магния, временная жесткость — от содержания в ней бикарбонатов кальция и магния. Обычное кипячение воды приводит к выпадению солей кальция и магния в осадок, чем в значительной степени снижается жесткость воды. Наглядным примером тому служит накипь, образующаяся на стенках чайников и самоваров.
Жесткость выражается суммой миллиграмм-эквивалентов ионов кальция и магния в 1 л воды. 1 мг-экв жесткости, или 1° жесткости, отвечает содержанию 20,04 мг/л Са или 12,16 мг/л Mg. В ряде стран жесткость воды измеряется в градусах жесткости. В аквариумном рыбоводстве жесткость воды наиболее удобно выражать в русских или немецких градусах, которые равны 0,35663 мг-экв/л.
Различают воду: очень мягкую — 0–4°, мягкую — 4–8°, средней жесткости — 8-12°, жесткую — 12–18° и очень жесткую — 18–30°
Большинство аквариумистов пользуются водопроводной водой, жесткость которой непостоянна и зависит от материковых пород, времени года, количества атмосферных осадков. Например, в Москве жесткость воды от 4 до 12°, в Ленинграде вода значительно мягче — 2–3°, в Одессе — 12° и выше.
Солевой состав воды влияет на количество углекислоты, растворенной в воде. В жесткой воде, т. е. содержащей много солей кальция и магния, всегда мало свободной углекислоты, а в, мягкой — ее значительно больше.
Жесткость воды имеет большое значение для физиологического состояния рыб. Одним видам рыб необходима мягкая вода, другим — средней жесткости или даже жесткая. Следует учитывать, что при пересадке рыб из старой воды в свежую и наоборот они резко реагируют на изменение ее жесткости: наблюдаются скачкообразные движения, судороги, выпрыгивание из воды и нередко гибель рыб. Наибольшее значение жесткость воды имеет в период размножения рыб. Например, неоновые рыбы и филомены нерестятся в очень мягкой воде (от 0,5 до 4°), гетеробарбусы и серпасы — в мягкой (4–5°), менее прихотливы грими (2,5–7°), а такие рыбы, как фонарики, могут размножаться как в мягкой, так и в жесткой воде.
В аквариуме с многовидовым составом рыб трудно установить жесткость воды, необходимую для каждого вида в отдельности. Неудачи в этом случае чаще всего связаны с солевым составом воды.
Наличие в аквариуме большого количества моллюсков, различных ракушек и раковин, содержащих соли кальция, способствует повышению жесткости воды. В связи с этим присутствие в аквариуме их в большом количестве нежелательно.
Аквариумисту нужно уметь определять жесткость воды, а также составлять воду нужного солевого состава.
Принцип определения.По количеству трилона Б — натриевой соли этилендиаминотетрауксусной кислоты (порошок белого цвета), пошедшего на титрование пробы воды с индикатором эриохромом черным Т, рассчитывают содержание растворенных в ней солей кальция и магния. Так как индикатор меняет свою окраску не только от изменения концентрации ионов кальция и магния, но и в зависимости от рН раствора, в титруемый раствор добавляют буферную смесь (NH 4OH + NH 4Cl), поддерживающую рН около 10.
Реактивы:
Раствор трилона Б, 0,05 н. раствор: растворяют 9,3 г трилона Б в дистиллированной воде с последующим доведением объема до 1 л.
Буферный раствор: 20 г химически чистой NH 4Cl растворяют в дистиллированной воде, добавляют 100 мл 20 %-ного раствора NH 4OH и доводят объем дистиллированной водой до 1 л.
Раствор индикатора: 0,5 г эриохрома черного Т растворяют в 10 мл буферного раствора и доводят объем 96 %-ным этиловым спиртом до 100 мл.
Ход анализа.В коническую колбу емкостью 200–250 мл наливают 50 мл исследуемой воды, добавляют 5 мл буферной смеси и 10–15 капель индикатора эриохрома черного Т (до появления интенсивного вишнево-красного цвета). При непрерывном покачивании колбы пробу титруют раствором трилона Б. По мере прибавления трилона Б вишнево-красный цвет переходит в лиловый. С этого момента титрование следует проводить медленнее. Окончание титрования устанавливают по появлению синего цвета с зеленоватым оттенком.
Расчет.Содержание растворимых в воде солей кальция и магния вычисляют но формуле:
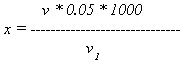
где х — количество растворимых в воде солей кальция и магния, мг-экв/л;
v — количество трилона Б, пошедшее на титрование, мл;
0,05 — нормальность трилона;
1000 — пересчет на 1 л воды;
v 1 — объем исследуемой воды, мл.
Для перевода в градусы жесткости полученную цифру умножают на 2,8.
Читать дальшеИнтервал:
Закладка:










