БСЭ БСЭ - Большая Советская Энциклопедия (ЗО)
- Название:Большая Советская Энциклопедия (ЗО)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (ЗО) краткое содержание
Большая Советская Энциклопедия (ЗО) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
З. называется также воздушный невозвратный клапан автомобильной шины.
Лит.: Лемберг М. Д., Системы гидроавтоматики, М. — Л., 1965; Веллер В. Н., Автоматическое регулирование паровых турбин, М., 1967.
С. М. Лосев.

Рис. 1. Коробчатый золотник: 1 — коробка; 2 — тяга; 3 — золотниковое зеркало; 4, 5 — окна; 6 — замкнутое пространство; 7 — полость.
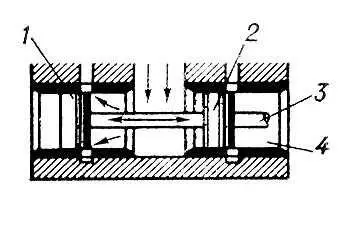
Рис. 2. Цилиндрический золотник: 1, 2 — поршни; 3 — шток; 4 — втулка.
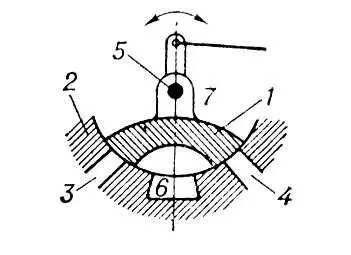
Рис. 3. Крановый золотник: 1 — коробка; 2 — втулка; 3, 4 — окна; 5 — ось; 6, 7 — камеры.
Золотниковое распределение
Золотнико'вое распределе'ние,применяется для изменения и распределения потока жидкости или газа посредством золотника. См. также Парораспределение.
Золото
Зо'лото(лат. Aurum), Au, химический элемент 1 группы периодической системы Менделеева; атомный номер 79, атомная масса 196,9665; тяжёлый металл жёлтого цвета. Состоит из одного устойчивого изотопа 197Au.
Историческая справка. З. было первым металлом, известным человеку. Изделия из З. найдены в культурных слоях эпохи неолита (5—4-е тыс. до н. э.). В древних государствах — Египте, Месопотамии, Индии, Китае добыча З., изготовление украшений и др. предметов из него существовали за 3—2 тыс. до н. э. З. часто упоминается в Библии, «Илиаде», «Одиссее» и др. памятниках древней литературы. Алхимики называли З. «царём металлов» и обозначали его символом Солнца  ; открытие способов превращения неблагородных металлов в З. было главной целью алхимии.
; открытие способов превращения неблагородных металлов в З. было главной целью алхимии.
О развитии добычи З. см. Золотодобывающая промышленность, Благородные металлы.
Распространённость в природе. Среднее содержание З. в литосфере составляет 4,3·10 -7% по массе. В магме и магматических породах З. рассеяно, но из горячих вод в земной коре образуются гидротермальные месторождения З., имеющие важное промышленное значение (кварцевые золотоносные жилы и др.). В рудах З. в основном находится в свободном (самородном) состоянии (см. Золото самородное ) и лишь очень редко образует минералы с селеном, теллуром, сурьмой, висмутом. Пирит и др. сульфиды часто содержат примесь З., которое извлекают при переработке медных, полиметаллических и др. руд.
В биосфере З. мигрирует в комплексе с органическими соединениями и механическим путём в речных взвесях. 1 л морской и речной воды содержит около 4·10 -9 г З. На участках золоторудных месторождений подземные воды содержат З. приблизительно 10 -6г/л. Оно мигрирует в почвах и оттуда попадает в растения; некоторые из них концентрируют З., например хвощи, кукуруза. Разрушение эндогенных месторождений З. приводит к образованию россыпей З., имеющих промышленное значение. З. добывается в 41 стране; его основные запасы сосредоточены в СССР, ЮАР и Канаде.
Физические и химические свойства. З. — мягкий, очень пластичный, тягучий металл (может быть проковано в листки толщиной до 8·10 -5 мм, протянуто в проволоку, 2 км которой весят 1 г ), хорошо проводит тепло и электричество, весьма стойко против химических воздействий. Кристаллическая решётка З. гранецентрированная кубическая, а = 4,704 Å. Атомный радиус 1,44 Å, ионный радиус Au 1+1,37 Å. Плотность (при 20°С) 19,32 г/см 3 , t пл 1064,43°С, t kип2947°С; термический коэффициент линейного расширения 14,2·10 -6(0—100°С); удельная теплопроводность 311,48 вт /( м ·К) [0,744 кал/см ( сек ·°С]; удельная теплоёмкость 132,3 дж /( кг ·К) [0,0316 кал / г ·°С] (при 0°—100°С); удельное электросопротивление 2,25·10 -8 ом ( м (2,25·10 -6 ом ( см ) (при 20°С); температурный коэффициент электросопротивления 0,00396 (0—100°С). Модуль упругости 79·103 Мн/м 2 (79·10 2 кгс/мм 2 ), для отожжённого З. предел прочности при растяжении 100—140 Мн/м 2 (10—14 кгс/мм 2 ), относительное удлинение 30—50%, сужение площади поперечного сечения 90%. После пластической деформации на холоду предел прочности повышается до 270—340 Мн/м 2 (27—34 кгс/мм 2 ) . Твёрдость по Бринеллю 180 Мн/м 2 (18 кгс/мм 2 ) (для З. отожжённого около 400 °С).
Конфигурация внешних электронов атома З. 5d 106s 1. В соединениях З. имеет валентности 1 и 3 (известны комплексные соединения, в которых З. 2-валентно). С неметаллами (кроме галогенов) З. не взаимодействует. С галогенами З. образует галогениды, например 2Au + 3Cl 2=2AuC13. В смеси соляной и азотной кислот З. растворяется, образуя золотохлористоводородную кислоту H [AuCl 4]. В растворах цианида натрия NaCN (или калия KCN) при одновременном доступе кислорода З. превращается в цианоаурат (I) натрия 2Na [Au (CN) 2]. Эта реакция, открытая в 1843 П. Р. Багратионом, получила практическое применение только в конце 19 в. (см. Цианирование ). Для З. характерна лёгкая восстановимость его из соединений до металла и способность к комплексообразованию. Существование закиси З., т. е. оксида З. (I) Au 2O, сомнительно. Хлорид З. (I) AuCl получается при нагревании хлорида З. (III): AuC1 3= AuCl + C1 2.
Хлорид З. (III) AuC1 3получается действием хлора на порошок или тонкие листочки З. при 200 °С. Красные иглы AuC1 3дают с водой коричнево-красный раствор комплексной кислоты: AuC1 3+Н 2О=Н 2[AuOC13].
При осаждении раствора AuC1 3едкой щёлочью выпадает амфотерная жёлто-коричневая гидроокись З.(III) Au (OH) 3c преобладанием кислотных свойств; поэтому её называют золотой кислотой, а её соли — ауратами (III). При нагревании гидроокись З. (III) превращается в окись З. Au 2O 3, которая выше 220° разлагается по реакции:
2Au 2O 3= 4Au + 3O 2.
При восстановлении солей З. хлоридом олова (II) 2AuC1 3+ 3SnCl 2 = 3SnCl 4+ 2Au
образуется весьма стойкий пурпуровый коллоидный раствор З. (кассиев пурпур); это используется в анализе для обнаружения З. Количественное определение З. основано на его осаждении из водных растворов восстановителями (FeSO 4, H 2SO 3, H 2C 2O 4и др.) или на применении пробирного анализа.
Получение З. и его аффинаж. Из россыпных месторождений З. можно извлечь отмучиванием, основанным на большой разности плотностей З. и пустой породы. Этот способ, применявшийся уже в глубокой древности, сопряжён с большими потерями. Он уступил место амальгамации (известной уже в 1 в. до н. э. и применявшейся в Америке начиная с 16 в.) и цианированию, получившему широкое распространение в Америке, Африке и Австралии в 1890-х гг. В конце 19 — начале 20 вв. основным источником З. стали коренные месторождения. Золотоносную породу сначала подвергают дроблению и обогащению. Из полученного концентрата извлекают З. раствором цианида калия или натрия. Из раствора комплексного цианида осаждают З. цинком; при этом выпадают и примеси. Для очистки (аффинажа) З. электролизом (способ Э. Вольвилла, 1896) аноды, отлитые из нечистого З., подвешивают в ванне, содержащей солянокислый раствор AuC1 3, катодом служит лист чистого З. При прохождении тока примеси выпадают в осадок (анодный ил, шлам), а на катоде отлагается З. чистотой не менее 99,99%.
Читать дальшеИнтервал:
Закладка:
