БСЭ БСЭ - Большая Советская Энциклопедия (РЕ)
- Название:Большая Советская Энциклопедия (РЕ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (РЕ) краткое содержание
Большая Советская Энциклопедия (РЕ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Рёнжи
Рёнжи(Rungis), город во Франции, в департаменте Валь-де-Марн, пригород Парижа. Население 8 тыс. чел. (1968). В 1969 в Р. открыт центральный продовольственный оптовый рынок (бывший Les Halles) Большого Парижа. Торговый комплекс занимает площадь 625 га (в т. ч. рынок 204 га ) , имеет свои производственные цехи, склады, ж.-д. станции (здесь постоянно работает до 12 тыс. чел., 1972).
Рени Гвидо
Ре'ни(Reni) Гвидо (4.11.1575, Кальвенцано, Эмилия-Романья, — 18.8.1642, Болонья), итальянский живописец. Основополагающим для Р. стало воздействие братьев Карраччи, изучал также произведения Рафаэля, Караваджо и античное искусство. Работал преимущественно в Риме (с 1605), а также в Болонье (с 1622). В зрелом творчестве сочетал изящество гармонически-ясных, нередко рельефообразных композиций с колоритом, построенным на градациях тёплых золотистых или высветленных серебристых тонов (фреска «Аврора» в Палаццо Паллавичини-Роспильози в Риме, около 1610). В болонский период в произведениях Р. усиливаются черты элегантной и холодной идеализации («Аталанта и Гиппомен», см. илл. ) или слащавой сентиментальности, благодаря которым имя Р. в последующие эпохи нередко считалось синонимом академизирующего искусства.
Лит.: Щербачева М. И., Картины Гвидо Рени в собрании Эрмитажа, в книга: Труды государственного Эрмитажа, т. 1, М., 1956, с. 73—80: Gnudi С., Cavalli G. С., Guido Reni, [Firenze, 1955].
Г. Рени. «Аврора». Фреска в Палаццо Паллавичини-Роспильози в Риме. Около 1610.

Г. Рени. «Аврора». Фреска в Палаццо Палавичини-Роспильози в Риме. Около 1610.

Г. Рени. «Аталанта и Гиппомен». Национальные музей и галереи Каподимонте. Неаполь.
Рени (город в Одесской области)
Рени',город, центр Ренийского района Одесской области УССР. Расположен на р. Дунай. Торговый порт. Ж.-д. станция. 21,3 тыс. жителей (1974). Предприятия ж.-д. транспорта и пищевой промышленности.
Рений
Ре'ний(Rhenium), Re, химический элемент VII группы периодической системы Менделеева, атомный номер 75, атомная масса 186,207. Светло-серый металл. В природном Р. два изотопа: стабильный 185Re (37,07%) и слаборадиоактивный 187Re (с периодом полураспада T 1 /2= 10 11лет).
В 1871 Д. И. Менделеев предсказал существование элемента с атомным весом 190 — аналога марганца — и назвал его «тримарганцем». В последующие годы появлялось много недостоверных сообщений об открытии этого элемента. Но лишь в 1925 нем. химики И. и В. Ноддак обнаружили его спектральным методом в минерале колумбите. Название Р. происходит от латинского наименования р. Рейн (Rhenus) в Германии.
Распространение в природе. Р. — типичный рассеянный элемент . Среднее содержание его в земной коре 7×10 8% по массе. Известны три минерала Р. — окисел, сульфид и сульфоренат меди CuReS 4(минерал джезказганит). Как примесь Р. встречается в минералах других[ элементов; его повышенные концентрации отмечены в колумбитах, танталитах, цирконатах, минералах редких земель, сульфидах меди и особенно в молибдените MoS 2(от 0,1 до 10 -5%). Связь Р. с молибденитом обусловлена изоморфизмом MoS 2и ReS 2. Важный источник Р. — некоторые медные сульфидные концентраты (0,002—0,005% Re).
Физические и химические свойства. Р. кристаллизуется в гексагональной плотноупакованной решётке ( а = 2,760 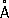 , с = 4,458
, с = 4,458 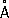 ). Атомный радиус 1,373
). Атомный радиус 1,373 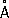 , ионный радиус Re 7 +0,56
, ионный радиус Re 7 +0,56 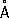 . Плотность 21 , 03 г/см 3, t пл = 3180 ± 20 °С, t kип = 5900 °С. Удельная теплоёмкость 153 дж/ ( кг × К ) , или 0,03653 кал/ ( г × град ) (0—1200 °С). Термический коэффициент линейного расширения 6,7×10 -6(20—500 °С). Удельное объёмное электрическое сопротивление 19,3×10 -6 ом × см (20 °С). температура перехода в состояние сверхпроводимости 1,699 К; работа выхода 4,80 эв, парамагнитен.
. Плотность 21 , 03 г/см 3, t пл = 3180 ± 20 °С, t kип = 5900 °С. Удельная теплоёмкость 153 дж/ ( кг × К ) , или 0,03653 кал/ ( г × град ) (0—1200 °С). Термический коэффициент линейного расширения 6,7×10 -6(20—500 °С). Удельное объёмное электрическое сопротивление 19,3×10 -6 ом × см (20 °С). температура перехода в состояние сверхпроводимости 1,699 К; работа выхода 4,80 эв, парамагнитен.
По тугоплавкости Р. уступает лишь вольфраму. В отличие от вольфрама, Р. пластичен в литом и рекристаллизованном состоянии и деформируется на холоду. Модуль упругости Р. 470 Гн/м 2, или 47 000 кгс/мм 2 (выше, чем у других металлов, за исключением Os и Ir). Это обусловливает высокое сопротивление деформации и быстрый наклёп при обработке давлением. Р. отличается высокой длительной прочностью при температурах 1000—2000 °С.
У атома Re семь внешних электронов; конфигурация высших энергетических уровней 5d 56s 2. На воздухе при обычной температуре Р. устойчив. Окисление металла с образованием окислов (ReOs, Re 2O 7) наблюдается начиная с 300 °С и интенсивно протекает выше 600 °С. С водородом Р. не реагирует вплоть до температуры плавления. С азотом не взаимодействует вообще. Р., в отличие от других тугоплавких металлов, не образует карбидов. Фтор и хлор реагируют с Р. при нагревании с образованием ReFe и ReCl 5, с бромом и йодом металл непосредственно не взаимодействует. Пары серы при 700—800 °С дают с Р. сульфид ReS 2.
Р. не корродирует в соляной и плавиковой кислотах любых концентраций на холоду и при нагревании до 100 °С. В азотной кислоте, горячей концентрированной серной кислоте, в перекиси водорода металл растворяется с образованием рениевой кислоты. В растворах щелочей при нагревании Р. медленно корродирует, расплавленные щёлочи растворяют его быстро.
Для Р. известны все валентные состояния от +7 до —1, что обусловливает многочисленность и разнообразие его соединений. Наиболее устойчивы соединения семивалентного Р. Рениевый ангидрид ReO 7— светло-жёлтое вещество, хорошо растворимое в воде. Рениевая кислота HReO 4— бесцветная, сильная; сравнительно слабый окислитель (в отличие от марганцевой HMnO 4). При взаимодействии HReO 4с щелочами, окислами или карбонатами металлов образуются её соли — перренаты. Соединения иных степеней окисления Р. — оранжево-красная трёхокись ReO 3, тёмно-коричневая двуокись ReO2, легколетучие хлориды и оксихлориды ReCI 5, ReOCl 4, ReO 3CI и др.
Получение и применение. Основным источником Р. служат молибденитовые концентраты (с содержанием Re 0,01—0,04%) и медные концентраты некоторых месторождений меди (с содержанием Re 0,002—0,003%). При окислительном обжиге молибденитовых концентратов (см. Молибден ) Р. удаляется с печными газами в виде Re 2O 7( t кип 360 °С), которая концентрируется в продуктах пылеуловительных систем (шламах, растворах). На различных стадиях производства черновой меди из концентратов Р. также удаляется с газами. Если печные газы направляются в производство серной кислоты, Р. концентрируется в промывной кислоте электрофильтров. Для извлечения Р. из пылей и шламов применяют выщелачивание слабой H 2SO 4с добавкой окислителя — пиролюзита. Из полученных растворов, а также из промывной серной кислоты Р. извлекают сорбцией или экстракцией. Конечным продуктом является перренат аммония NH 4ReO 4. Восстанавливая его водородом, получают порошок P., превращаемый затем в компактные заготовки методом порошковой металлургии. Применяют также плавку Р. в электроннолучевых печах. Как тугоплавкий металл P., а также сплавы W с Re используют в производстве электронных приборов. Кроме того, из Р. и его сплавов с W изготавливают термопары для измерения температур до 2500 °С, электроконтакты и детали точных приборов. Сплавы Re с W, Mo, Ta отличаются высокой жаропрочностью. Они применяются в авиа- и космической технике. Р. и его соединения используются в качестве эффективных катализаторов при крекинге нефти.
Читать дальшеИнтервал:
Закладка:
