БСЭ БСЭ - Большая Советская Энциклопедия (СК)
- Название:Большая Советская Энциклопедия (СК)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (СК) краткое содержание
Большая Советская Энциклопедия (СК) - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Векторы а и b можно рассматривать как кватернионыa 1i + a 2j + a 3 k и b 1i + b 2j + b 3k. Тогда их С. п. равно взятой с обратным знаком скалярной части произведения этих кватернионов (а векторное произведение — векторной части).
Скалярный потенциал
Скаля'рный потенциа'л,см. Потенциалы электромагнитного поля.
Скамоцци Винченцо
Скамо'цци(Scamozzi) Винченцо (1552, Виченца, — 7.8.1616, Венеция), итальянский архитектор. Помимо самостоятельных работ (дворец Триссино в Виченце, 1577, и др.), С. принадлежат достройки сооружений, начатых Я. Сансовино (Библиотека Сан-Марко в Венеции, завершена в 1583) и Палладио (театр Олимпико в Виченце, 1580—85). С. стремился придать архитектурным правилам (в т. ч. теории ордеров) значение «вечной нормы», тем самым повлияв на зарождение классицизма.
Соч.: L'ldea dell'architettura universale, pt 1—2, Veiietiis, 1615.
Скамья оптическая
Скамья' опти'ческая,установка для испытания оптических приборов и отдельных деталей. В С. о. на массивные направляющие насаживают штативы, называемые рейтерами, которые несут различные подставки и столики с укрепленными на них испытуемыми и регистрирующими приборами и деталями. Рейтеры можно перемещать вдоль С. о. и неподвижно закрепить в любом месте по всей длине направляющих. Механические перемещения рейтеров строго параллельны оптическим и визирным осям установленных на С. о. приборов. Длина С. о. может достигать нескольких м.
Скандагупта
Скандагу'пта, правитель в 455—467 Северной Индии из династии Гуптов. В начале царствования С., по-видимому, отразил вторжение племён пушьямитров (Западная Индия), начавшееся ещё при его предшественнике Кумарагупте 1. Тяжёлую войну С. пришлось вести с эфталитами, вторгшимися в Северо-Западную Индию. Хотя С. одержал победу над эфталитами и сумел сохранить свои владения, ресурсы империи были истощены, о чём, в частности, свидетельствует порча гуптских монет в середине 5 в.
Скандербег Георг Кастриоти
Скандербе'г(Scanderbeg, Skenderbeu) Георг Кастриоти (Kastrioti) (около 1405 — 17.1.1468), руководитель освободительной борьбы албанского народа против османских завоевателей, национальный герой Албании. Происходил из влиятельного феодального княжеского рода Кастриоти. Ребёнком был отдан в заложники тур. султану Мураду II, впоследствии служил в его войсках. За талант военачальника получил титул бея и в честь Александра Македонского имя Искендер (отсюда Искендер-бей, или в искажённом произношении — С.). Исподволь готовился к борьбе против султана, поддерживал отношения с его внутренними и внешними противниками, вел переговоры с Я. Хуньяди. После победоносного для венгерских войск сражения с султанскими войсками под Нишем (3 ноября 1443) С. с отрядом в 300 всадников покинул турецкий лагерь и прибыл в Дибру. Опираясь на свободное крестьянство, поддержавшее его призыв к освободительному антитурецкому восстанию, начал поход, направленный на изгнание турок из албанских земель. Через несколько дней вступил в Крую и 28 ноября был провозглашен главой княжества Кастриоти. Изгнал турецкие гарнизоны из крепостей Петреля, Петральба, Стелюши, Торчан, Светиград. Предпринял шаги к объединению албанских феодалов, преобразовал народный ополчение в регулярную армию, состоявшую преимущественно из крестьян. Под руководством С. албанский народ в течение 24 лет отражал попытки османских завоевателей восстановить свою власть. С. обладал незаурядным талантом государственного деятеля, преодолевал большие внутри- и внешнеполитические затруднения, вызванные сепаратизмом албанских феодалов, корыстной политикой Венеции и папского престола. Умер в Леже. В НРА учрежден орден Скандербега.
Лит.: Георги Кастриоти-Скендербег. 1468—1968, София, 1970.

Скандербег.
Скандий
Ска'ндий(лат. Scandium), Sc, химический элемент III группы периодической системы Менделеева: атомный номер 21, атомная масса 44,9559; лёгкий металл с характерным жёлтым отливом, который появляется при контакте металла с воздухом. Известен один природный стабильный изотоп 45Sc. Из 10 искусственных радиоактивных изотопов важнейший 46Sc с периодом полураспада 84 сут. С. был предсказан Д. И. Менделеевым в 1870 и выделен в 1879 Л. Ф. Нильсоном из минералов гадолинита и эвксенита, найденных в Скандинавии (лат. Scandia), отсюда и название элемента.
Распространение в природе. Среднее содержание С. в земной коре (кларк) 2,2×10 -3% по массе. В горных породах содержание С. различно: в ультраосновных 5×10 -4, в основных 2,4×10 -3, в средних 2,5×10 -4, в гранитах и сиенитах 3 .10 -4; в осадочных породах (1—1,3) .10 -4. С. концентрируется в земной коре в результате магматических, гидротермальных и гипергенных (поверхностных) процессов. Известно два собственных минерала С. — тортвейтит и стерреттит; они встречаются чрезвычайно редко. В целом С. — типичный рассеянный элемент, слабый мигрант (см. также Рассеянных элементов руды ) . Содержание С. в морской воде 4×10 -5 г/л.
Физические и химические свойства. С. существует в двух кристаллических модификациях: a и b; при обычной температуре устойчива a - модификация с гексагональной решёткой (а = 3,3080 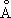 и с = 5,2653
и с = 5,2653 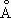 ), выше 1350 °С — b-модификация с кубической объёмноцентрированной решёткой. Плотность С. в а-форме при 25 °С 3,020 г/см 3, атомной радиус 1,64
), выше 1350 °С — b-модификация с кубической объёмноцентрированной решёткой. Плотность С. в а-форме при 25 °С 3,020 г/см 3, атомной радиус 1,64 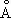 , ионный радиус 0,75
, ионный радиус 0,75 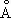 , t пл 1539 ± 5 °С, t kип 2700 °C, выше 1600 °С летуч. При 25 °С удельная теплоёмкость 25,158 кдж/ ( кг . К ) [6,01 ккал/ ( г ×°С)], удельное электрическое сопротивление (54—70,7) .10 -6 ом × см, С. слабый парамагнетик, его атомная магнитная восприимчивость 236-10 -6(20 °С). Sc — первый переходный элемент с одним 3d электроном; конфигурация внешних электронов атома 3d 14s 2.
, t пл 1539 ± 5 °С, t kип 2700 °C, выше 1600 °С летуч. При 25 °С удельная теплоёмкость 25,158 кдж/ ( кг . К ) [6,01 ккал/ ( г ×°С)], удельное электрическое сопротивление (54—70,7) .10 -6 ом × см, С. слабый парамагнетик, его атомная магнитная восприимчивость 236-10 -6(20 °С). Sc — первый переходный элемент с одним 3d электроном; конфигурация внешних электронов атома 3d 14s 2.
С.— мягкий металл, в чистом состоянии легко поддаётся обработке — ковке, прокатке, штамповке.
По хим. поведению сходен с др. переходными элементами в степени окисления +3 (например, Ti 3+, Fe 3+, Мп 3+), элементами подгруппы Al, Be, а также элементами иттриевой подгруппы, вместе с которыми его иногда относят к редкоземельным элементам. На воздухе покрывается защитной окисной плёнкой толщиной до 600Ǻ, заметное окисление начинается при 250 °С. При взаимодействии с водородом (450 °С) образуется гидрид ScH 2, с азотом (600—800 °С) — нитрид ScN, с галогенами (400—600 °С) — соединения типа ScCI 3; С. реагирует также с бором и кремнием при температуре выше 1000 °С. Металл легко растворяется в соляной, азотной и серной кислотах (с понижением концентрации кислоты скорость растворения С. резко падает и с 0,001 н. растворами он не реагирует). Соли соляной, серной, азотной, роданистоводородной и уксусной кислот хорошо растворяются в воде, а соли фосфорной, щавелевой и плавиковой кислот мало растворимы; некоторой летучестью обладают ацетилацетонат и его фторпроизводные. На С. практически не действуют разбавленные растворы NaOH (10%) и смесь концентрированных HNO 3и HF (1: 1). В воде соединения С. заметно гидролизуются с образованием основных солей. Ионы Sc 3+склонны к полимеризации, образованию комплексных ионов различного типа, состав которых зависит от природы аниона и pH среды, например Sc (CO 3) - 2, Sc (SO 4) 3- 3. Основные соли в растворе легко переходят в аморфную гидроокись.
Читать дальшеИнтервал:
Закладка:
