БСЭ БСЭ - Большая Советская Энциклопедия (СЕ)
- Название:Большая Советская Энциклопедия (СЕ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (СЕ) краткое содержание
Большая Советская Энциклопедия (СЕ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
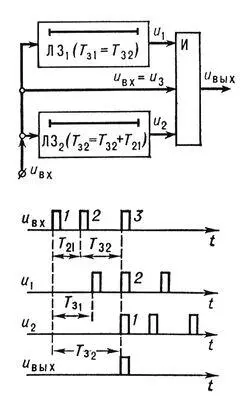
Рис. 3. Схема селекции кодированной серии импульсов (следующих с заданными временными интервалами) и соответствующие диаграммы сигналов: ЛЗ — линия задержки; И — логический элемент на 3 входа; u вх— входной сигнал; u вых— выходной сигнал; T 21, T 32— интервалы между импульсами; Т 31, Т 32— время задержки сигналов в ЛЗ 1и ЛЗ 2; 1, 2, 3 — порядковые номера импульсов.
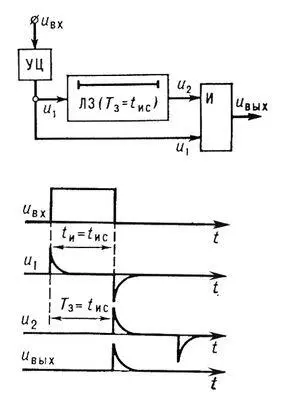
Рис. 2. Схема селекции импульсов заданной длительности и соответствующие диаграммы сигналов; УЦ — устройство дифференцирования импульса («укорачивающая» цепь); ЛЗ — линия задержки; И — логический элемент на 2 входа; u вх— входной сигнал; u вых— выходной сигнал; t ис— заданная длительность сигнала; t и— длительность импульса; Т 3— время задержки сигнала в ЛЗ.
Селемджа
Селемджа',река в Амурской области РСФСР, левый самый крупный приток Зеи. Длина 647 км, площадь бассейна 68,6 тыс. км 2. Берёт начало на стыке хребтов Ям-Алинь и Эзон; в верховьях — горная река (ниже поселка Экимчан долина расширяется); в низовьях река течёт по северной окраине Зейско-Буреинской равнины. Главные притоки: Ульма (слева), Нора (справа). Питание преимущественно дождевое. Средний расход воды 715 м 3/сек, наибольший (июль) 10300 м 3/сек, наименьший (март) 5 м 3/сек. Замерзает в начале ноября, вскрывается в начале мая. Судоходна от устья р. Норы, в высокую воду от Экимчана. В верхнем течении С. — месторождения золота.
Селен
Селе'н(Selenium), Se, химический элемент VI группы периодической системы Менделеева; атомный номер 34, атомная масса 78, 96; преимущественно неметалл. Природный С. представляет собой смесь шести устойчивых изотопов (%) — 74Se (0,87), 76Se (9,02), 77Se (7,58), 78Se (23,52), 80Se (49,82), 82Se (9,19). Из 16 радиоактивных изотопов наибольшее значение имеет 75Se с периодом полураспада 121 сут. Элемент открыт в 1817 И. Берцелиусом (название дано от греч. selene — Луна).
Распространение в природе. С. — очень редкий и рассеянный элемент, его содержание в земной коре (кларк) 5×10 -6 % по массе. История С. в земной коре тесно связана с историей серы. С. обладает способностью к концентрации и, несмотря на низкий кларк, образует 38 самостоятельных минералов — селенидов природных, селенитов, селенатов и др. Характерны изоморфные примеси С. в сульфидах и самородной сере.
В биосфере С. энергично мигрирует. Источником для накопления С. в живых организмах служат изверженные горные породы, вулканические дымы, вулканические термальные воды. Поэтому в районах современного и древнего вулканизма почвы и осадочные породы нередко обогащены С. (в среднем в глинах и сланцах — 6×10 -5 % ) .
Физические и химические свойства. Конфигурация внешней электронной оболочки атома Se 4s 24p 4; у двух р-электронов спины спарены, а у остальных двух — не спарены, поэтому атомы С. способны образовывать молекулы Se 2или цепочки атомов Se n. Цепи атомов С. могут замыкаться в кольцевые молекулы Se 8. Разнообразие молекулярного строения обусловливает существование С. в различных аллотропических модификациях: аморфной (порошкообразный, коллоидный, стекловидный) и кристаллический (моноклинный a-и b-формы и гексагональный g-формы). Аморфный (красный) порошкообразный и коллоидный С. (плотность 4,25 г/см 3 при 25 °С) получают при восстановлении из раствора селенистой кислоты H 2SeO 3, быстрым охлаждением паров С. и др. способами. Стекловидный (чёрный) С. (плотность 4,28 г/см 3 при 25 °С) получают при нагревании любой модификации С. выше 220 °С с последующим быстрым охлаждением. Стекловидный С. обладает стеклянным блеском, хрупок. Термодинамически наиболее устойчив гексагональный (серый) С. Он получается из других форм С. нагреванием до плавления с медленным охлаждением до 180—210 °С и выдержкой при этой температуре. Решётка его построена из расположенных параллельно спиральных цепочек атомов. Атомы внутри цепей связаны ковалентно. Постоянные решётки а = 4,36 Å, с = 4,95 Å, атомный радиус 1,6 Å, ионные радиусы Se 2-1,98 Å и Se 4+0,69 Å, плотность 4,807 г/см 3при 20 °С, t пл217 °С, t kип685 °С. Пары С. желтоватого цвета. В парах в равновесии находятся четыре полимерные формы Se 8 Û Se 6Û Se 4Û Se 2. Выше 900 °С доминирует Se 2. Удельная теплоёмкость гексагонального С. 0,19—0,32 кдж/ ( кг × К ) , [0,0463—0,0767 кал/ ( г ×°С)] при —198 — +25 °С и 0,34 кдж/ ( кг × К ) [0,81 кал/ ( г × °С )] при 217 °С; коэффициент теплопроводности 2,344 вт/ ( м × К ) [0,0056 кал/ ( см × сек × °С )] , температурный коэффициент линейного расширения при 20 °С: гексагонального монокристаллического С. вдоль с -оси 17,88×10 -6, перпендикулярно с -оси 74,09×10 -6, поликристаллического 49,27×10 -6; изотермическая сжимаемость b 0=11,3× 10 -3 кбар -1, коэффициент электрического сопротивления в темноте при 20 °С 10 2 — 10 12 ом см. Все модификации С. обладают фотоэлектрическими свойствами. Гексагональный С. вплоть до температуры плавления — примесный полупроводник с дырочной проводимостью. С. — диамагнетик (пары его парамагнитны). На воздухе С. устойчив; кислород, вода, соляная и разбавленная серная кислоты на него не действуют, хорошо растворим в концентрированной азотной кислоте и царской водке, в щелочах растворяется с окислением. С. в соединениях имеет степени окисления —2, +2, +4, +6. Энергия ионизации Se 0®Se 1+®Se 2+®S 3+соответственно 0,75; 21,5; 32 эв.
С кислородом С. образует ряд окислов: SeO, Se 2O 5, SeO 2, SeO 3. Два последних являются ангидридами селенистой H 2SeO 3и селеновой H 2SeO 4к-т (соли — селениты и селенаты). Наиболее устойчив SeO 2. С галогенами С. даёт соединения SeF 6, SeF 4, SeCl 4, SeBr 4, Se 2Cl 2и др. Сера и теллур образуют непрерывный ряд твёрдых растворов с С. С азотом С. даёт Se 4N 4, с углеродом — CSe 2. Известны соединения с фосфором P 2Se 3, P 4Se 3, P 2Se 5. Водород взаимодействует с С. при t ³ 200 °С , образуя H 2Se; раствор H 2Se в воде называется селеноводородной кислотой. При взаимодействии с металлами С. образует селениды. Получены многочисленные комплексные соединения С. Все соединения С. ядовиты.
Получение и применение. С. получают из отходов сернокислотного, целлюлозно-бумажного производства и анодных шламов электролитического рафинирования меди. В шламах С. присутствует вместе с серой, теллуром, тяжёлыми и благородными металлами. Для извлечения С. шламы фильтруют и подвергают либо окислительному обжигу (около 700 °С), либо нагреванию с концентрированной серной кислотой. Образующийся летучий SeO 2улавливают в скрубберах и электрофильтрах. Из растворов технический С. осаждают сернистым газом. Применяют также спекание шлама с содой с последующим выщелачиванием селената натрия водой и выделением из раствора С. Для получения С. высокой чистоты, используемого в качестве полупроводникового материала, черновой С. рафинируют методами перегонки в вакууме, перекристаллизации и др.
Читать дальшеИнтервал:
Закладка:
