БСЭ БСЭ - Большая Советская Энциклопедия (ХИ)
- Название:Большая Советская Энциклопедия (ХИ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (ХИ) краткое содержание
Большая Советская Энциклопедия (ХИ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Электронная структура атомов.Электронам в атоме приписываются различные орбитали, которые характеризуются главным квантовым числом n , орбитальным квантовым числом l и магнитным квантовым числом m l (см. Квантовые числа , Квантовая химия ). Имеется одна наиболее устойчивая орбиталь с n = 1, образующая К -оболочку. L -Оболочка с n = 2 включает одну орбиталь с l = 0 и m l = 0 и три с l = 1 и m l = —1, 0 и +1. Их называют 1 s -орбиталь, 2 s -орбиталь и три 2 р -орбитали. М -Оболочка состоит из 3 s -орбитали, трёх 3 р -орбиталей и пяти 3 d -орбиталей. Электрон имеет спин со спиновым квантовым числом s = 1/ 2, который может ориентироваться относительно определённого направления двумя различными путями — с компонентами, даваемыми магнитным спиновым квантовым числом m s , равным + 1/ 2или — 1/ 2. В атоме не может быть двух электронов с одинаковыми значениями всех квантовых чисел. Следовательно, 1 s -орбиталь, образующая К -оболочку, может быть занята только одним электроном с положительным или отрицательным спином или же двумя электронами (электронной парой), одним — с положительным спином, другим — с отрицательным.
Заполнение определённых оболочек и подоболочек приводит к особой устойчивости атомов, наблюдающейся у атомов инертных газов. В этих устойчивых структурах электронная конфигурация заполненной оболочки гелия 1 s 2 , неона 2 s 2 2 p 6 , аргона 3 s 2 3 p 6 , криптона 3 d 10 4 s 2 4 p 6 , ксенона 4 d 10 5 s 2 5 p 6 , радона 4 f 14 5 d 10 6 s 2 6 p 6 , эка-радона 5 f 14 6 d 10 7 s 2 7 p 6 . [О заполнении электронных оболочек см. также Атом , Периодическая система элементов .]
Ковалентная связь.В 1927 датский физик О. Бурро выполнил квантовомеханический расчёт молекулярного нона водорода и показал, что единственный электрон в этом ионе На занимает орбиталь, называемую молекулярной орбиталью, которая простирается вокруг обоих протонов. Теоретический расчёт энергии связи этого молекулярного иона, т. е. разности между суммарной энергией отдельного атома и протона и энергией иона в его основном состоянии, привёл к значению 255 кдж × моль -1 , прекрасно согласующемуся с экспериментом. Вскоре было отмечено, что электронную структуру молекулярного иона водорода можно рассмотреть, используя волновую функцию основного состояния атома водорода. По мере сближения атома водорода и протона появляется возможность выхода электрона из области, окружающей одно ядро, в область, окружающую второе ядро, причём в каждом случае электрон занимает 1 s -орбиталь. Молекулярная орбиталь, образованная как сумма этих двух 1 s -орбиталей, является хорошим приближением к молекулярной орбитали, полученной Бурро путём решения волнового уравнения Шрёдингера. Если образовать волновую функцию как разность двух 1 s -орбиталей, то это, как было показано, отвечает не притяжению, а отталкиванию. Первая волновая функция является симметричной линейной комбинацией двух 1 s -функций и отвечает устойчивому состоянию, образованию одноэлектронной ковалентной связи, тогда как вторая функция, являющаяся антисимметричной линейной комбинацией тех же 1 s -функций, отвечает неустойчивому состоянию. Иногда говорят, что образование одноэлектронной ковалентной связи в молекуле водорода соответствует резонансу данного электрона между двумя атомными орбиталями или между двумя атомами водорода.
В том же году (1927) было выполнено два квантовомеханических расчёта Х. с. в молекуле водорода. Американский физик Э. У. Кондон использовал метод молекулярных орбиталей, приписав молекуле водорода структуру, в которой за основу была принята орбиталь H 2 +, рассчитанная Бурро, причём к этой орбитали были отнесены оба электрона с противоположными спинами. Немецкие физики В. Гейтлер и Ф. Лондон отнесли один электрон, с положительным спином, к 1 s -орбитали одного атома водорода, а второй, с отрицательным спином, к 1 s -орбитали др. атома водорода. Волновая функция для данной молекулы была суммой этой функции и функции, в которой два электрона менялись местами — электрон с положительным спином относился ко второму атому, а с отрицательным — к первому атому. Оба расчёта, как Кондона, так и Гейтлера и Лондона, привели к выводу об устойчивости молекулы водорода с энергией связи, превышающей приблизительно в 1,7 раза энергию связи в молекулярном ионе водорода. Связь между двумя атомами водорода в молекуле водорода — прототип связи с поделенной электронной парой по Льюису, обычно называют ковалентной связью.
На основании формальных результатов квантовомеханического рассмотрения Х. с. можно сделать следующий простой вывод: атомы могут образовывать ковалентную связь (осуществляемую парой электронов) за счёт каждой стабильной орбитали, занятой первоначально одним электроном; при этом образуется связь такого типа, как описанная выше для молекулы водорода, а её стабильность может быть связана с тем же самым явлением резонанса. Иными словами, для образования ковалентной связи необходимо наличие двух электронов с противоположными спинами и по одной стабильной орбитали у каждого из двух связываемых атомов.
Атом водорода с единственной стабильной орбиталью (1 s ) может образовывать лишь одну ковалентную связь. Атом углерода и другие атомы второго периода (бор, азот, кислород) могут образовывать не более четырёх ковалентных связей с использованием четырёх орбиталей L -оболочки. Квантовомеханическое рассмотрение приводит также к выводу, что каждая дополнительная связь, образующаяся в молекуле, в общем случае ведёт к дальнейшей стабилизации молекулы, а следовательно, наиболее устойчивы такие электронные структуры молекулы, в которых все стабильные орбитали атомов либо использованы для образования связей, либо заполнены неподелёнными парами электронов.
Метану CH 4, например, приписывается следующая структура валентных связей:
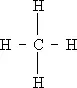
Чёрточки означают поделенные электронные пары. Можно сказать, что поделенная электронная пара занимает 1 s -орбиталь каждого атома водорода и одну из четырёх орбиталей L -оболочки атома углерода. Атомы водорода, т. о., комплектуют завершенную К -оболочку (как в атоме гелия), а атом углерода, который также имеет неподелённую пару 1 s -электронов, комплектует завершенную L -оболочку (как в атоме неона).
Представление о гибридных орбиталях, формирующих связи, даёт решение проблемы, волновавшей химиков и физиков в ранний период квантовой теории. Четыре орбитали L -оболочки делятся на два вида — 2 s -орбиталь и три 2 р -орбитали, а четыре связи атома углерода, как показывают химические свойства соединений углерода, оказываются одинаковыми. В действительности вместо 2 s -орбитали и трёх 2 р -орбиталей может образовываться набор эквивалентных sp 3 -гибридных орбиталей, называется тетраэдрическими орбиталями; они направлены к вершинам правильного тетраэдра и обладают большей силой связи, чем s -орбиталь или р -орбиталь (Л. Полинг , 1931).
Читать дальшеИнтервал:
Закладка:
