Андрей Шляхов - Биология для тех, кто хочет понять и простить самку богомола
- Название:Биология для тех, кто хочет понять и простить самку богомола
- Автор:
- Жанр:
- Издательство:АСТ
- Год:2020
- Город:Москва
- ISBN:978-5-17-120369-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Андрей Шляхов - Биология для тех, кто хочет понять и простить самку богомола краткое содержание
У биологии очень необычная история. С одной стороны, знания о живой природе человечество начало накапливать с момента своего появления. Первые люди уже разбирались в ботанике и зоологии – они знали, какие растения съедобны, а какие нет, и изучали повадки животных для того, чтобы на них охотиться. С другой стороны, в отдельную науку биология выделилась только в начале XIX века, когда ученые наконец-то обратили внимание на то, что у всего живого есть нечто общее, ряд общих свойств и признаков.
О том, чем отличает живое от неживого, о том, как появилась жизнь и многом другом расскажет эта книга.
Биология для тех, кто хочет понять и простить самку богомола - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
По содержанию в клетке белки стоят на втором месте после воды. Примерно 50 % от сухого остатка клеточных веществ приходится на долю белков.
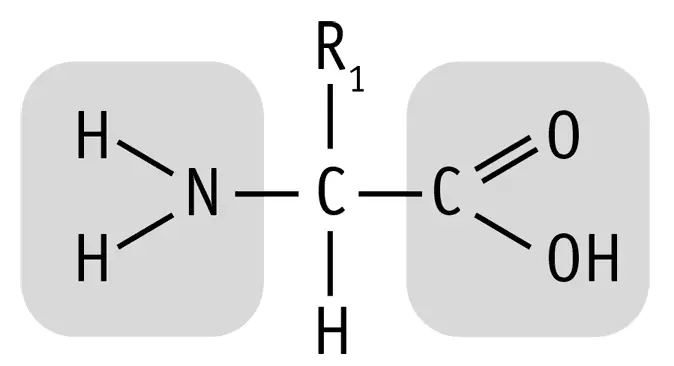
Общая структура молекулы аминокислоты
Давайте вспомним из курса химии, что аминокислотами называются органические вещества, которые содержат карбоксильную группу (–СООН), аминогруппу (–NH 2) и радикал или R-группу (это остальная часть молекулы). Особенности физических и химических свойств аминокислот обусловлены присутствием в их молекулах двух противоположных по свойствам функциональных групп: кислотной карбоксильной группы и основной аминогруппы.
В зависимости от того, могут ли аминокислоты вырабатываться в организме человека или животных, их разделяют на заменимые аминокислоты, которые могут вырабатываться, и незаменимые аминокислоты, которые вырабатываться не могут. Условием нормальной жизнедеятельности организма является поступление незаменимых аминокислот вместе с пищей. А вот растения вырабатывают все виды аминокислот.
Не надо путать незаменимые аминокислоты с витаминами – веществами, которые ускоряют или делают возможными определенные обменные реакции. Витамины – это катализаторы, а аминокислоты – строительный материал и источник энергии.
Аминокислот известно с полтысячи, но в образовании большинства белков задействовано только 20.
Белки состоящие только из аминокислот, называются простыми белками. Если белок помимо аминокислот содержит еще и какой-то не аминокислотный компонент – металл, углевод, липид, нуклеиновую кислоту, – то такой белок называют сложным. Примерами сложных белков являются металлопротеины, гликопротеины, липопротеины, нуклеопротеины. Обратите внимание на то, что название неаминокислотного компонента всегда ставится первым. «Протеинолипид» – неграмотное название.
Химики называют белки «пептидами» или «полипептидами».
Пептиды – это вещества, молекулы которых построены из двух и более остатков аминокислот, соединенных в цепь пептидными связями – C(O)NH–.
Пептид, молекула которого содержит до 20 остатков аминокислот, называется олигопептидом, а от 21 остатка начинаются полипептиды. Для того, чтобы полипептид считался белком, в составе его молекулы должно присутствовать более 50 аминокислотных остатков.
Клетке энергетически невыгодно (можно сказать – неудобно) держать белки в развернутой форме, в виде длинной-предлинной полипептидной цепочки. Поэтому полипептидные цепи подвергаются пространственной организации – укладке с приобретением определенной трехмерной структуры.
Различают четыре уровня пространственной организации белков.
Первичная структура белка – полипептидная цепь.
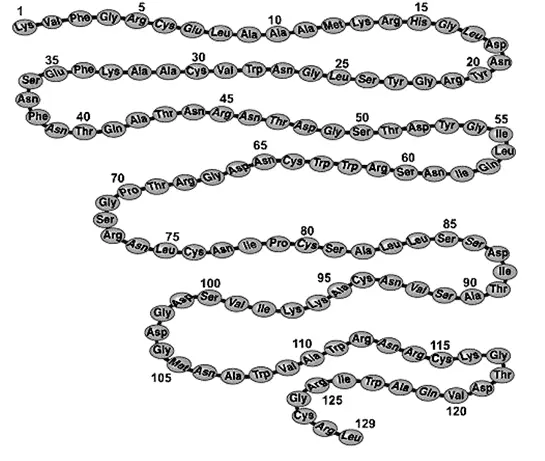
Первичная структура белка
Первичная структура белковой молекулы – самая «главная». Именно первичная структура – расположение атомов в молекуле белка – определяет свойства молекулы и ее пространственную конфигурацию.
Вторичная структура белка представляет собой упорядоченное свертывание полипептидной цепи в спираль, которая имеет вид растянутой пружины. Витки спирали укрепляются водородными связями, [32] Водородная связь (или «Н-связь») – это взаимодействие между двумя электроотрицательными атомами одной или разных молекул посредством атома водорода. Положительно заряженный протон (атом водорода), соединенный с одним электроотрицательным атомом ковалентной связью (это химическая связь, возникающая за счет образования общей пары электронов), притягивает к себе другой электроотрицательный атом. Для возникновения водородных связей в молекулах вещества должны присутствовать атомы водорода, связанные с небольшими электроотрицательными атомами, например – с атомами кислорода, азота или фтора. При этом на атомах водорода создается заметный частичный положительный заряд. Вторым условием возникновения водородных связей является наличие у электроотрицательных атомов не поделенных электронных пар, с которыми будет взаимодействовать атом водорода.
возникающими между карбоксильными группами (СО-) и аминогруппами (NH-).
Водородные связи слабые, но, многократно повторяясь, они придают спирали белковой молекулы устойчивость и жесткость. На уровне вторичной структуры существуют такие белки, как, например, коллаген (сухожилия) или кератин (волосы, ногти).
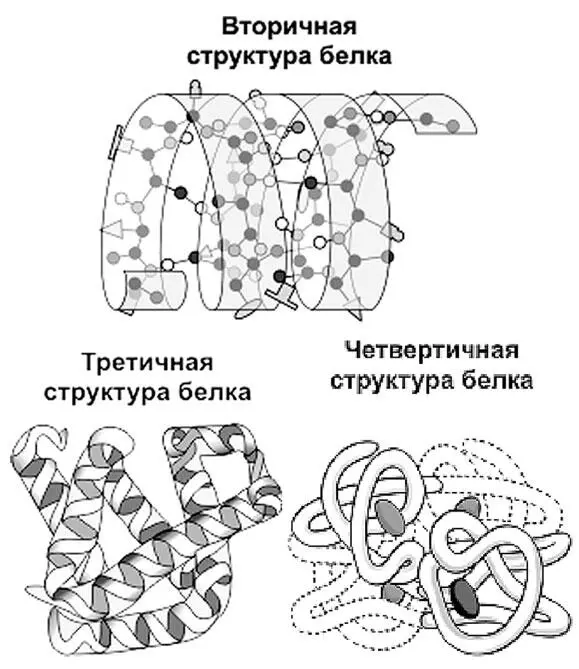
Третичная структура белка представляет собой укладку полипептидных цепей в «клубки» – глобулы, возникающая в результате возникновения различных химических связей.
На уровне третичной структуры существуют ферменты, антитела, некоторые гормоны.
Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами, соединенными какими-то химическими связями. Наиболее известным белком, имеющим четвертичную структуру, является белок крови гемоглобин, молекула которого образована четырьмя «клубками». Клубки связывает вместе общее для всех железосодержащее «ядро», называемое гемом. «Гема» в переводе с греческого означает «кровь», «глобус» – это «шар» на латыни. Гемоглобин – кровяной шар.
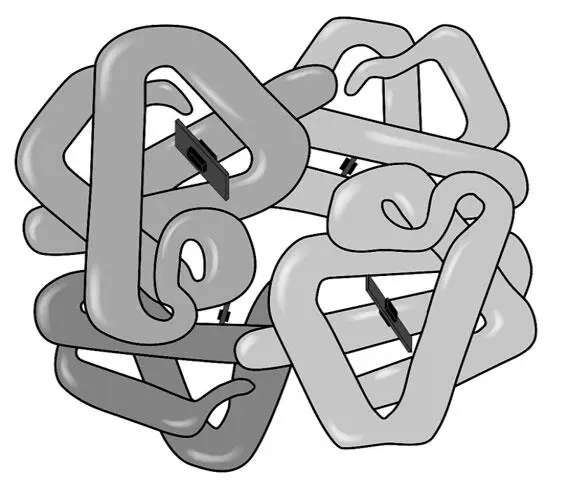
Молекула гемоглобина
Что случается с белком куриного или какого-то другого птичьего яйца при нагревании? Он сначала начинает загустевать, а затем твердеет, потому что тепловая энергия вызывает разрыв связей, удерживающих молекулу белка в свернутом виде. Молекула «расправляет плечи». Сначала утрачивается четвертичная структура, затем – третичная, затем – вторичная и молекула белка становится нитевидной. Нитевидной молекуле расправляться больше некуда, но она может распасться на несколько составных частей.
Процесс утраты трехмерной конформации, присущей данной молекуле белка, называют денатурацией (денатурация – потеря природной структуры). Изменение пространственной конфигурации молекулы приводит к изменению ее свойств и делает невозможным выполнение присущих ей биологических функций. Если денатурация не сопровождается разрушением первичной структуры, то она может быть обратимой – ниточка снова свернется в клубочек и займется своим делом. Процесс восстановления структуры белка после денатурации называется ренатурацией.
Читать дальшеИнтервал:
Закладка:










