Вильгельм Штрубе - Пути развития химии. Том 2. От начала промышленной революции до первой четверти XX века
- Название:Пути развития химии. Том 2. От начала промышленной революции до первой четверти XX века
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1984
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Вильгельм Штрубе - Пути развития химии. Том 2. От начала промышленной революции до первой четверти XX века краткое содержание
Пути развития химии. Том 2. От начала промышленной революции до первой четверти XX века - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
В начале XX в. производство соды полностью перешло на метод Сольве. Уже с конца 80-х годов XIX в. в Германии 75% соды получали именно этим способом.
Производство соды в 1869 г. достигало: в Англии — около 5,1 млн. немецких центнеров [214](255 000 т); во Франции — около 2,3 млн. немецких центнеров (115 000 т); в Германском Таможенном союзе — около 1,5 млн. немецких центнеров (75 000 т).
Цена 1 т кристаллической соды упала от 60 фунтов стерлингов в 1814 г. до 4 фунтов стерлингов в 1865 г. В Англии 60 фабрик, производящих в 1869 г. соду, выдавали, кроме того ежегодно свыше 350 000 т серной кислоты [171, с. 49].
Метод Сольве
Уже с начала XIX в. химики пытались найти способ получения соды путем превращения хлорида натрия в карбонат натрия без использования серной кислоты. В 1810 г. А. Фреснель получил соду действием аммиака и углекислого газа на раствор поваренной соли, однако его метод не стал промышленным. По этому же пути пошли в 30-е годы Д. Хэмминг и Г. Дьар. Они тоже пропускали аммиак и углекислый газ в водный раствор поваренной соли. При этом выпадал плохо растворимый бикарбонат натрия NaHCО 3, переходивший при нагревании в соду. Для промышленности этот метод оказался нерентабельным, так как не был найден способ регенерации аммиака.
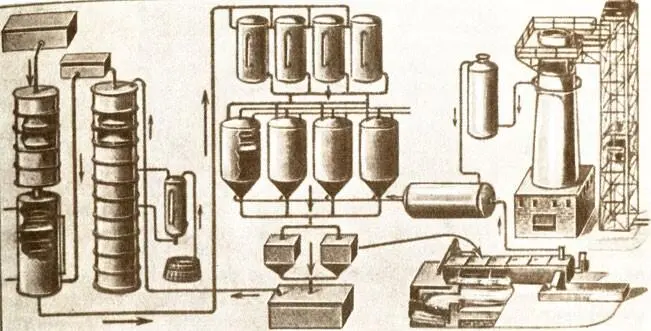
Схема производства соды по методу Сольве (Брокгауз, 1934 г.)
Наконец, Эрнесту Сольве удалось найти способ регенерации аммиака и некоторого количества углекислого газа и сделать весь процесс непрерывным. Сольве сконструировал новое оборудование и машины. В результате многолетних экспериментов он установил оптимальные условия для получения высоких выходов бикарбоната натрия.

Эрнест Сольве (1838-1922)
Отец Эрнеста Сольве был владельцем каменоломни и солеварни в г. Ребеке (около Брюсселя). Эрнест родился в 1838 г. В юности он много болел и свою мечту — занятия химией — вынужден был осуществить только путем самообразования. Позднее Сольве работал на заводе по производству газа, принадлежавшему его дяде, и пытался найти способы утилизации вредных побочных продуктов, образующихся при получении газа (в частности, аммиачной воды). Кроме того, Сольве искал способ получения соды из раствора поваренной соли, аммиака и углекислого газа.
Преимущества разработанного Сольве аммиачного способа получения соды были очевидны. Во-первых, этот метод требовал значительно более низких температур и тем самым обеспечивал экономию угля. Во-вторых, вместо очищенной поваренной соли в этом методе можно было использовать рассолы, стоимость которых была значительно ниже. В-третьих, метод Сольве включал меньше стадий и, что очень важно, при этом не нужна была серная кислота [103, с. 470]. И наконец, метод Сольве не вызывал загрязнения окружающей среды и давал соду очень высокой чистоты. Сравним основные стадии обоих методов.
Производственные стадии по методу Леблана:
1. 2NaCl + H 2 SO 4 = Na 2 SO 4 + 2НСl (при температуре темно-красного каления).
2. Na 2 SO 4 + ЗС + СаО = Na 2 CO 3 + CaS + 2CO (температура до 960° С).
3. Выщелачивание.
4. Выпаривание и кристаллизация Nа 2 СО 3 * 10Н 2 О.
5. Кальцинирование с образованием Na 2 CO 3 .
6 Частичная регенерация серы из сульфида кальция.
Производственные стадии по методу Сольве.
1. NaCl + NH 3 + СO 2 + Н 2 0 = NaHCO 3 + NH 4 Cl (образование NаНСО 3 происходит в водном растворе при 30-40° С).
2. Кальцинирование с образованием соды: 2NaHCO 3 = NагСО 3 + СО 2 + Н 2 О (СО 2 частично остается в замкнутом процессе).
3. Регенерация аммиака: 2NH 4 Cl + СаО = СаСl 2 + Н 2 O + 2NH 3 .
Несмотря на преимущества метода Сольве, его автор вначале испытывал большие трудности. Основанная им в 1863 г. вблизи г. Шарлеруа (Бельгия) фабрика истощила все семейные капиталы. Только после создания в 1865 г. акционерного общества "Сольве и К°" продукция, получаемая этим методом, могла успешно конкурировать с предприятиями, работавшими по методу Леблана, а затем и победить их на международном рынке. Вскоре почти во всех странах возникли заводы по производству соды методом Сольве: в Англии (1871 г.), Франции (1874г.), Германии, вблизи Вилена в Бадене (1880 г.) и окрестностях Бернбурга (1883 г.), США (1881г.), России (1883 г.). Подобно Альфреду Нобелю (см. ниже), Сольве стал одним из самых богатых и влиятельных людей в мире. Он основал прекрасно оборудованный исследовательский институт, на своих заводах ввел в 1908 г. трехсменный график работы с восьмичасовым рабочим днем. Монопольное положение владельцев этих предприятий обеспечивало им колоссальные прибыли. Концерн Сольве стал одной из самых могущественных химических компаний.
Взрывчатые вещества
Нитроцеллюлоза, динамит, баллистит
Взрывчатые вещества, созданные впервые химиками во второй половине XIX в., стали одним из важнейших продуктов химического производства. Нитроцеллюлоза была получена в 1846 г. независимо двумя химиками — Христианом Шёнбейном и Рудольфом Бёттгером. Действие азотной кислоты на целлюлозу приводило к образованию смеси сложных эфи-ров — нитратов целлюлозы. При обработке их спиртоэфирной смесью часть из них (низконитрованная целлюлоза) растворялась, превращаясь в коллодий, а высоконитрованная целлюлоза, не растворяющаяся в этой смеси, и представляла собой собственно нитроцеллюлозу. Вскоре стало известно важное практическое значение этого вещества. Из нитроцеллюлозы выделялось в три раза больше газообразных веществ, чем из черного пороха, а скорость сгорания ее была в 500 раз выше. Кроме того, горение нитроцеллюлозы было бездымным. Военные и промышленники способствовали разработке на основе нитроцеллюлозы высокоэффективных взрывчатых веществ. Однако после того, как в 1848 г. взлетел на воздух завод в Ле Бурже (около Парижа), а вскоре такие же несчастные случаи произошли в Англии и Австрии, производство нитроцеллюлозы было приостановлено.
Тем временем Асканио Собреро впервые получил нитроглицерин — азотнокислый эфир глицерина. Это было жидкое вещество, чрезвычайно взрывчатое и очень чувствительное к толчкам, ударам или быстрому нагреву. Ядовитое и вязкое, это вещество вначале не показалось пригодным для практических целей. Но А. Нобель сразу обратил на него внимание [215]. Он смешал черный порох с нитроглицерином и получил взрывчатую смесь, которую можно было взрывать только с помощью специального взрывателя. "Огнепроводный" шнур из черного пороха был для этих целей не пригоден. Тогда Нобель вспомнил об изученной Либихом "гремучей ртути", которая легко воспламенялась и была пригодна в качестве запала не только для смеси нитроглицерина с черным порохом, но также и для других взрывчатых веществ.
Читать дальшеИнтервал:
Закладка:


![Жорж Вигарелло - История тела Том 2 [От Великой французской революции до Первой мировой войны]](/books/1081096/zhorzh-vigarello-istoriya-tela-tom-2-ot-velikoj-fran.webp)







