Михаил Ермолаев - Биологическая химия
- Название:Биологическая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1974
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Ермолаев - Биологическая химия краткое содержание
В учебнике нашли отражение последние научные данные о ферментах, белках, гормонах, обмене веществ и энергии и т. д. Особое внимание обращено на значение и использование данных биохимии в медицине, в связи с чем расширены разделы, посвященные патологии разных видов обменов и их исследованиям в клинике Включены материалы по наследственным заболеваниям, связанным с нарушением синтеза белка и ферментов.
Учебник написан по программе, утвержденной Министерством здраво" хранения СССР, и предназначен для учащихся фельдшерско-лаборантских отделениях медицинских училищ.
Биологическая химия - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Эти основные функции белков достаточно четко характеризуют их значение для организма.
Элементарный состав белков
При химическом анализе белков были определены важнейшие элементы, входящие в их состав, и их количественные соотношения.
Элементарный состав белков в процентах будет следующим: углерод — 50-54,4%, водород — 6,5-7,3%, кислород — 21,5-23,5%, азот — 15- 17%, сера — 0,3-2,5%.
В составе белков обнаружены также фосфор, йод, железо и другие минеральные вещества.
Как было установлено, наибольшим постоянством в составе белка отличается азот, количество которого составляет в среднем 16%, поэтому было предложено определить содержание белка по количеству входящего в него азота по следующей формуле:
Кол-во азота×6,25 г = кол-во белка в %, где 6,25 г белка соответствует 1 г азота.
При изучении химической структуры белка было установлено, что основной его структурной единицей — мономером — является аминокислота. Таким образом, белки определяются как высокомолекулярные органические, N-содержащие вещества, состоящие в основном из аминокислот и находящиеся в клетках в коллоидном состоянии.
Свойства белков
Молекулярный вес белков
Определение молекулярного веса белков проводилось различными методами (криоскопическим, осмометрическим и др.). Наиболее точным оказался предложенный Т. Сведбергом метод седиментации , который проводится в ультрацентрифуге с ускорением до 900 000 g. Он основан на различной скорости оседания белков, в зависимости от их молекулярного веса: белки с высоким молекулярным весом оседают при меньшей скорости вращения центрифуги, а белки с малым весом — при высоких скоростях. По определенной формуле рассчитывают молекулярный вес. Изучение различных белков показало, что все они являются высокомолекулярными соединениями.
Приведем молекулярный вес следующих белков: инсулина — 5700 (11 500), рибонуклеазы — 12 700, миоглобина 4 — 17 000, гемоглобина — 65 000, каталазы — 250 000, уреазы 4-480 000, гемоцианина — 5 000 000 — 6 000 000.
Белки-коллоиды
Белки вследствие своего высокого молекулярного веса обладают свойствами коллоидов.
Как известно, все растворы в зависимости от величины растворенных частиц подразделяются на истинные и коллоидные. К истинным относятся такие растворы, величина частиц которых меньше 1 ммк (10 -7см); величина частиц коллоидных растворов составляет от 1 мк до 1 ммк (10 -4-10 -7см). Для отличия истинных от коллоидных растворов пользуются в основном двумя методами — изучением "эффекта Тиндаля" и диализом.

Рис. 9. 'эффект Тиндаля'. Сосуд, ближайший к свету, содержит концентрированный раствор сахара. Второй сосуд содержит коллоидную дисперсию. Пучок света виден во втором сосуде, но проходит через первый сосуд нерассеянным
Сущность "эффекта Тиндаля" заключается в следующем: при пропускании пучка света через истинный раствор его рассеивания не происходит, т. е. частицы истинного раствора настолько малы, что они не могут стать преградой для луча света и отклонить его в сторону. Если же пучок света направить на коллоидный раствор, то произойдет его рассеивание, которое будет наблюдаться в виде светящегося конуса. Это объясняется тем, что частицы коллоидного раствора, как более крупные, будут служить препятствием на пути луча света, в результате чего последний несколько отклонится (рис. 9).
Сущность явления диализа заключается в способности частиц раствора задерживаться или проходить в зависимости от их величины через полупроницаемые перепонки — мембраны, имеющие определенный размер отверстий — поры. К полупроницаемым мембранам относятся целлофан, коллоидная пленка, стенка бычьего пузыря и т. д. Если величина частиц раствора меньше размера пор такой мембраны, то они свободно проходят через них, если же размер частицы больше, чем поры, то частица задержится" В первом случае мы имеем дело с истинными растворами, которые свободно фильтруются (проходят) через полупроницаемые мембраны. Во втором случае — частицы коллоидных растворов задерживаются и не проходят через такие же мембраны.
Это свойство широко используется в медицине и химии для получения хорошо очищенных от посторонних примесей белковых препаратов. Например, для получения лечебных сывороток, γ-глобулинов. Явление диализа лежит в основе действия аппарата "искусственная почка", который в настоящее время широко используется в клиниках при лечении острой и хронической почечной недостаточности.
Белки — амфотерные электролиты
При изучении химического состава белка было установлено, что в его молекуле имеются свободные аминные (NH 2) и карбоксильные (СООН) группы, которые в растворе находятся в виде NH 3и СООН. Следовательно, белки в растворе обладают амфотерными свойствами (амфолит, амфион). При пропускании электрического тока белки будут передвигаться в зависимости от заряда белковой молекулы к катоду или аноду (рис. 10).
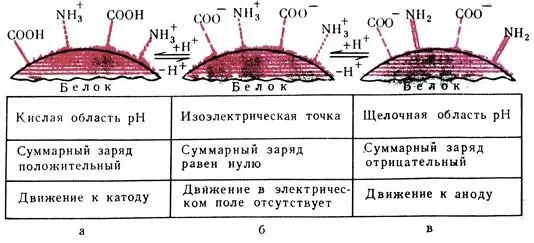
Рис. 10. Белки — амфотерные соединения. а — в кислом растворе суммарный заряд белка положительный и белок становится катионом; б — изоэлектрическая точка белка; суммарный заряд белковой молекулы равен нулю; в — в щелочной среде подавлена диссоциация аминных групп. Заряд белковой молекулы становится отрицательным и белок передвигается к аноду (белок играет роль аниона)
В щелочных растворах белок играет роль аниона: например, при действии едкого натра происходит потеря Н +из NH + 3:
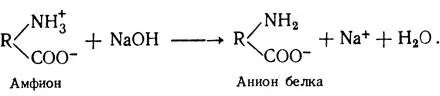
В кислых растворах, наоборот, белок играет роль катиона, как в случае с соляной кислотой:
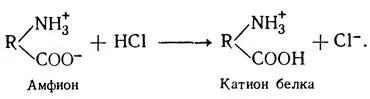
Таким образом, фактором, определяющим поведение белка как аниона или катиона, является концентрация водородных ионов, или значение рН среды. При повышении концентрации водородных ионов (среда кислая — рН 0-7) белок становится катионом, при ее понижении (среда щелочная- рН 7 -14), наоборот, белковые частицы становятся анионами. Такая способность белка проявлять или кислотные, или щелочные свойства характеризует его как амфотерное соединение.
Однако при определенных значениях рН число положительных зарядов белка будет равно числу отрицательных и заряд молекулы в целом будет практически равен нулю. Белковая молекула не будет перемещаться в электрическом поле. При этих условиях белок находится в изоэлектрическом состоянии; рН раствора, при котором белок находится в изоэлектрическом состоянии, называется изоэлектрической точкой.Изоэлектрическая точка большинства природных белков лежит в слабокислой среде (рН 4,8-5,4). Молекула таких белков содержит больше карбоксильных групп, чем аминных. Это свидетельствует о том, что в их составе содержится больше дикарбоновых аминокислот (см. Аминокислоты ). В изоэлектрической точке белок находится в наименее устойчивом состоянии и при незначительных изменениях рН среды в кислую или щелочную сторону он легко выпадает в осадок.
Читать дальшеИнтервал:
Закладка:






