Вячеслав Тарантул - Имя ему СПИД: Четвертый всадник Апокалипсиса
- Название:Имя ему СПИД: Четвертый всадник Апокалипсиса
- Автор:
- Жанр:
- Издательство:Языки славянской культуры
- Год:2004
- Город:Москва
- ISBN:5-9551-0050-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Вячеслав Тарантул - Имя ему СПИД: Четвертый всадник Апокалипсиса краткое содержание
Вячеслав Залманович Тарантул. Имя ему СПИД: Четвертый всадник Апокалипсиса. М: Языки славянской культуры, 2004 — 400 с.
О новом заболевании — синдроме приобретенного иммунодефицита (СПИД) — мир узнал чуть менее четверти века назад. Сегодня слово СПИД уже известно почти всем. Однако мало кто знает о причине этого смертельного заболевания, об истории его возникновения, о путях распространения, о средствах лечения и других многочисленных аспектах, связанных со СПИДом. Обо всем этом и идет речь в настоящей книге, написанной в научно-популярной форме.
Книга предназначена для самого широкого круга читателей: для медицинского персонала и врачей всех специальностей, для учителей, студентов и преподавателей вузов медицинского и биологического профиля, для молодых людей, вступающих в жизнь, и вообще для всех образованных людей, желающих больше знать о себе и об опасностях, которые их окружают.
В оформлении обложки использована гравюра А. Дюрера «Четыре всадника Апокалипсиса».
Имя ему СПИД: Четвертый всадник Апокалипсиса - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Большинство экспертов сходится во мнении, что терапия малыми двунитевыми РНК вряд ли станет панацеей от вирусов и других заболеваний. Однако создание на ее базе пусть даже не радикального, но все же действенного лекарственного средства будет очень важным шагом на пути разработки методов генной терапии.
Вполне возможно, что для борьбы с ВИЧ может быть использовано давно уже известное явление интерференции, происходящее иногда между вирусами. Еще в 1935 г., изучая инфекцию, вызываемую двумя штаммами (вариантами) вируса желтой лихорадки у обезьян, англичанин М. Хоскинс описал защитный эффект, не обусловленный иммунной реакцией. Суть интерференции заключается в том, что если в клетке уже есть какой-либо вирус, то другому вирусу туда проникнуть уже значительно сложнее.
B связи с этим сегодня определенные надежды связывают с вирусом по имени GBV–C. Недано было обнаружено, что ВИЧ-инфицированные, зараженные вирусом GBV–C, умирают в три раза реже, чем мужчины, не зараженные этой вторичной инфекцией. Вирус GBV–C известен около 10 лет, и первоначально подозревали, что он вызывает заболевание печени, так как очень похож по своей структуре на вирус гепатита C. Однако обследование большого числа пациентов не выявило взаимосвязи этого вируса с заболеваниями печени и других органов. И вот теперь оказывается, что вирус GBV–C может быть мощной защитой от ВИЧ подобно некоторым другим генетическим факторам, замедляющим развитие СПИДа. Механизм такого действия пока неясен, и на его выяснение теперь направлены силы многих ученых. Возможно, здесь сказывается известный принцип «вирус против вируса», т. е. та же интерференция.
Аптамеры
B борьбе с ВИЧ ученые возлагают определенные надежды еще на одну новую технологию, которая была разработана молекулярными генетиками для проведения фундаментальных молекулярно-генетических исследований, но, как и многие другие, теперь может быть использована в практических целях. Суть этой технологии, которая была названа аптамерной (еще одно название — SELEX, но оно сложно расшифровывается), заключается в следующем. B пробирке искусственно синтезируются короткие однонитевые РНК, состоящие из трех частей: по краям последовательности нуклеотидов у всех молекул РНК одинаковы, а вот центральная часть (длиной около 20–30 нуклеотидов) у всех РНК вариабельная. Как показывает расчет, из 20–30 нуклеотидов можно создать астрономическое число отличающихся друг от друга нуклеотидных последовательностей — порядка 10 15—10 17. Выяснилось, что в таком гигантском наборе разнообразных коротких РНК (его называют комбинаторной библиотекой) практически всегда найдется один или даже несколько вариантов молекул, которые способны специфически связываться с белком-мишенью и подавлять его биологическую активность. единственную РНК, которая способна взаимодействовать со строго определенным индивидуальным белком, назвали аптамером. Работа по отбору аптамера весьма кропотливая и непростая (рис. 34). Набор коротких однонитевых РНК пропускают через колонку, на которой «пришиты» те белки, на которые надо найти аптамер. Те из молекул РНК, которые имеют определенное сродство с этими белками, соединяются с ними. При этом могут связаться с белками и случайные молекулы РНК. Поэтому процедуру повторяют несколько раз (число циклов обычно равно 6—10). А чтобы материал не потерялся, после каждого цикла его «размножают» вновь с помощью уже упоминавшегося метода ПЦР. После отбора молекул РНК (реже ДНК), которые специфически связываются с определенным вирусным белком, проводят еще одну селекцию: отбирают те аптамеры, которые не только соединяются с белком, но и подавляют его активность. В случае успеха исследователи получают в свои руки мощный и очень специфический агент, направленный на единственную мишень. Будучи привнесенным в клетку, такой аптамер не окажет ни на что никакого влияния (т. е. он не вызовет никаких побочных эффектов), кроме как на тот единственный белок-мишень, на который он был предварительно отобран.
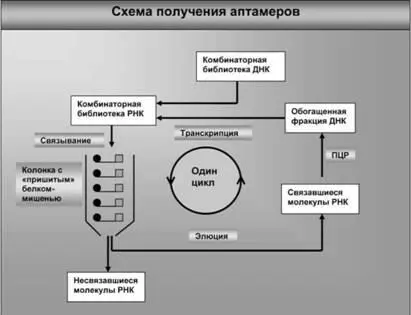
Рис. 34. Исходной базой для аптамерной технологии служит набор (библиотека) коротких РНК (ДНК), состоящий из огромного разнообразия по нуклеотидным последовательностям молекул. Специфическое взаимодействие с белком-мишенью единичных молекул из этого набора позволяет отбрать их, а потом размножить в пробирке с помощью ПЦР. После этого надо определить, какие из отобранных аптамеров подавляют активность белка-мишени. Аптамерная технология постепенно приближается к решению задач практической медицины и, в частности, к проблеме борьбы со СПИДом
И сегодня такие аптамеры уже получены на ряд белков ВИЧ. В клеточных системах показано, что аптамер, направленный, например, на вирусный белок по имени tat (он очень важен для жизненного цикла вируса), специфически подавляет размножение ВИЧ. Пока еще в медицинской практике нет препаратов на базе аптамеров. Но работа в этом направлении продолжается, и в скором времени от нее можно ожидать практических результатов.
Химеры
Создаваемые генными инженерами рекомбинантные ДНК иногда называют химерными в честь Химеры — легендарного изрыгающего пламя существа древнегреческих мифов, у которого голова и тело льва, на спине покоится голова козла, а вместо хвоста — змея. Такое название особенно подходит в тех случаях, когда рекомбинантные «конструкты» состоят из генов или их фрагментов, принадлежащих разным видам организмов. Подобные «химеры» были созданы для самых разнообразных целей, в том числе и для целенаправленого воздействия на ВИЧ. В последние годы число научных работ в этом направлении очень велико, поэтому отметим лишь некоторые из них (рис. 35).
Одна из испытанных схем с использованием химерных ДНК заключалась в следующем (рис. 35А). К гену, кодирующему белок-рецептор CD4, «подшили» другой ген, который обеспечивает синтез растительного белка рицина. Рицин, еще в Средние века использовался в качестве сильнейшего яда. Попадая в клетку, он блокирует синтез белка в цитоплазме, тем самым убивая ее. После внесения в клетки такой рекомбинантной ДНК в конечном итоге происходит образование химерного белка. Та его часть, которая соответствует белку-рецептору, обеспечивает строго специфическое связывание химеры с клетками, на поверхности которых содержится вирусный белок CD4. Другая же представляет собой яд рицин и уничтожает клетки, с которыми связывается химерная молекула. Таким образом, одна часть химеры обеспечивает направленный поиск в организме клеток, зараженных вирусом, а другая ее часть убивает их. Схема довольно проста и эффективна. В качестве «убийцы» можно использовать не только ген рицина, но и некоторые другие гены.
Читать дальшеИнтервал:
Закладка:










