Николай Юшкин - Оптический флюорит
- Название:Оптический флюорит
- Автор:
- Жанр:
- Издательство:Наука
- Год:1983
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Юшкин - Оптический флюорит краткое содержание
Оптический флюорит - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Флюорит оптически изотропен, т. е. все его оптические свойства не зависят от направления в кристалле. Он характеризуется относительно низким показателем преломления (n), который имеет (при 19° С) следующие значения для различных длин волн (λ):
| n | λ, мкм | n | λ, мкм |
|---|---|---|---|
| 1,6421 | 1,1311 | 1,47635 | 0,2288 |
| 1,5152 | 0,1819 | 1,30756 | 9,724 |
Показатель преломления мало зависит от длины волны (рис. 1), для него характерен типичный для щелочно-галоидных кристаллов ход частной дисперсии. Температурный коэффициент показателя преломления (dn/dt) варьирует от —6,2∙10 -6/°С для λ = 0,2288 мкм до —5,6∙10 -6/°С для λ = 9,724 мкм; минимальное значение установлено для λ = 0,852 мкм и равно —10,6∙10 -6/°С.
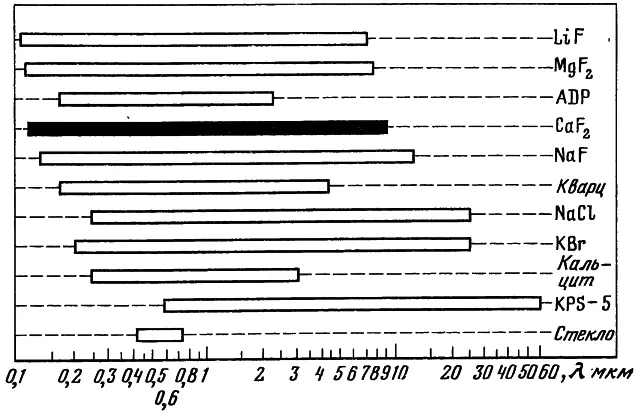
Рис. 3. Границы спектрального пропускания различных оптических материалов
Особенно важным свойством флюорита является его высокая прозрачность в широком спектральном диапазоне: от 0,125 мкм в вакуумной ультрафиолетовой (УФ) (шумановской) до 11 мкм в инфракрасной (ИК) областях спектра (рис. 2). На рис. 3 приведены сравнительные данные о диапазонах пропускания. Среди различных оптических материалов нет ни одного, для которого так удачно, как для флюорита, сочетались бы оптические характеристики. Только немногие искусственные кристаллы имеют более коротковолновую границу пропускания — это кристаллы фтористого лития LiF, фтористого магния MgF 2, дигидрофосфата аммония NH 4H 2PO 4(ADP). Но они либо имеют двойное лучепреломление, либо характеризуются низкой твердостью, либо водо- и кислотонеустойчивы (табл. 1), что ограничивает их применение в оптическом приборостроении. Ряд материалов, имеющих в ИК-области более длинноволновую границу пропускания, чем у фтористого кальция, уступают ему по пропусканию в УФ-диапазоне и могут использоваться исключительно в спектральных приборах для ИК-области. Это бромистый калий KBr, бромистый цезий CsBr, йодистый калий KI, KRS-5 (состава TlBr — TlI).
Таблица 1. Оптические характеристики некоторых кристаллов
| Кристалл | Показатель преломления n D | Твердость, кг/мм 2 | Растворимость в воде, г/100 г | Коэффициент линейного расширения α∙10 6 |
|---|---|---|---|---|
| CaF 2 | 1,4338 | 120 | 1,31∙10 -3 | 19,5 |
| NaF | 1,336 | 60 | 4,2 | — |
| NaCl | 1,54432 | 18 | 26,0 | 42 |
| LiF | 1,3915 | 99 | 0,27 | 41 |
| MgF 2 | n 0= 1,3777 | 415 | 7,6∙10 -3 | 11 |
| n e= 1,3895 |
Все оптические характеристики флюорита высокостабильны. Эти особые свойства определяют незаменимость оптического флюорита при создании высококорректированных оптических систем (апохроматов, планапохроматов), обеспечивающих высокое качество изображения и ограничение хроматических аберраций. Вместе с тем прозрачность и достаточно большая дисперсия флюорита в УФ-области спектра обусловливают его использование в объективах современных ультрафиолетовых микроскопов и при изготовлении призменной оптики в вакуумных приборах (спектрографах, монохроматорах и др.).
Благоприятные механические, технические и эксплуатационные характеристики кристаллов флюорита в сочетании с прозрачностью в широком спектральном диапазоне, высокой оптической однородностью, отсутствием двойного лучепреломления, люминесценции, высокой радиационной устойчивостью и лучевой прочностью определяют и ряд новых его практических применений в тепловидении и фурье-спектроскопии, астрономии, космической технике, в квантовой и силовой оптике и т. д.
Области практического применения оптического флюорита непрерывно расширяются, в связи с чем энергично возрастают и потребности в этом уникальном оптическом материале.
Свойства флюорита, в том числе и оптические, определяются его конституцией, т. е. химическим составом и кристаллической структурой.
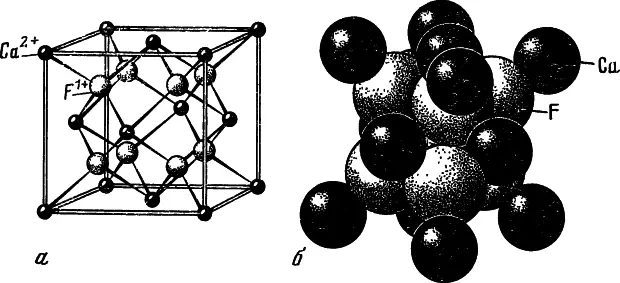
Рис. 4. Различные модели кристаллической структуры флюорита
Объяснение в тексте
Флюорит (по химической номенклатуре — фтористый кальций CaF 2) состоит из атомов кальция (51,33%) и фтора (48,67%), закономерно упакованных по принципу гранецентрированной кубической кристаллической решетки. Это значит, что если мы соединим мысленно все взаимодействующие друг с другом атомы по кратчайшим расстояниям между ними прямыми линиями, то получим регулярную пространственную решетку, которая состоит из бесконечного множества совершенно одинаковых элементарных ячеек, как бы размножающихся в пространстве. Кристаллохимики называют такие ячейки параллелепипедами повторяемости.
Элементарная ячейка флюорита представляет собой куб, разделенный на восемь маленьких кубиков — октантов. Ионы кальция (Ca 2+) располагаются по вершинам большого куба и по центрам каждой из его граней, а ионы фтора (F -) — в центрах каждого октанта. Каждый ион фтора оказывается, таким образом, окруженным четырьмя ионами кальция (FCa 4), располагающимися по вершинам тетраэдра, который называется координационным, а каждый ион кальция находится внутри координационности куба, образованного восемью ионами фтора (CaF 8).
Если изобразить ионы кальция и фтора разноцветными шариками, то элементарная ячейка флюорита будет выглядеть так, как показано на рис. 4, а. На первый взгляд кажется, что в ней слишком много ионов кальция. Но нужно учесть, что каждый ион кальция в вершинах ячейки принадлежит восьми ячейкам, а располагающийся на грани — двум ячейкам. Так что «собственных» ионов кальция здесь всего (1 : 8∙8+1 : 2∙6), ионов фтора — восемь, а число формульных единиц CaF 2в ячейке z — четыре. Если шарики, изображающие ионы, «раздуть» до их истинных размеров, характеризуемых эффективными радиусами (Са 2+= 1,04 Å, F -= l,33 Å), то получим более близкую к реальной, хотя и менее наглядную модель структуры флюорита (см. рис. 4, б). Структуру флюорита можно изобразить также в виде анионных полиэдров — Ca-кубов или катионных F-тетраэдров. Размер ребра элементарной ячейки α 0= 5,46295±0,00010 Å.
Рассмотренная схема кристаллической структуры флюорита является идеальной. Реальная структура несколько сложнее, и это связано прежде всего с тем, что во флюорит, кроме кальция и фтора, в тех или иных количествах входят атомы некоторых других элементов. Ионы F -могут частично замещаться кислородом О 2-, но основные вариации химического состава связаны с изоморфными замещениями Са 2+на Ag +, Cd 2+, Ge 2+, Cu +, Hg 2+, In 3+, Mn 2+, Sn 2+, Sr 2+, Sb 3+, Tl 3+, Pb 4+, Th 4+, U 4+и особенно на двух- и трехвалентные ионы редкоземельных элементов — TR 2+(Sm 2+, Eu 2+, Yb 2+и др.) и TR 3+(Y 3+, Се 3+, La 3+, Lu 3+и др). Элементы-примеси присутствуют во флюорите обычно в незначительных количествах, однако содержание редких земель иногда может достигать десятков процентов. Максимально возможное содержание TRF 3во флюорите, не разрушающее его структуру, 50%. Механизм замещения двухвалентного кальция трехвалентным иттрием или другими редкими землями довольно своеобразный. Ионные радиусы этих элементов близки друг другу (Y 3+= 0,97 Å, Са 2+= 1,04 Å), и при вхождении YF 3в структуру CaF 2иттрий занимает места ионов кальция. При этом две трети ионов фтора заполняют все тетраэдрические позиции, которые им и положено занимать, а одна треть их входит в октаэдрические пустоты между катионами кальция, бывшие в CaF 2незаполненными. В результате такого изоморфизма «с заполнением пространства» плотность и показатель преломления иттрофлюорита по сравнению с флюоритом повышаются, увеличивается параметр элементарной ячейки до α 0= 5,50 Å. При замещении кальция трехвалентными ионами редкоземельных элементов происходит компенсация избыточного заряда эквивалентными количествами ионов О 2-, Na +и других элементов по схемам
Читать дальшеИнтервал:
Закладка:




