Roger Orrit - У атомов тоже есть сердце. Резерфорд. Атомное ядро.
- Название:У атомов тоже есть сердце. Резерфорд. Атомное ядро.
- Автор:
- Жанр:
- Издательство:Де Агостини
- Год:2015
- Город:М.
- ISBN:2409-0069
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Roger Orrit - У атомов тоже есть сердце. Резерфорд. Атомное ядро. краткое содержание
Эрнесту Резерфорду наука обязана доказательством существования атомного ядра, которое ученый определил как «муху» внутри «собора» атома. Несмотря на ничтожный размер, в ядре сконцентрирована большая часть массы атома, а значит, и энергии. Резерфорд считается лучшим экспериментатором своей эпохи: он оценил возраст Земли на основе радиоактивного распада, и за раскрытие этой тайны в 1908 году ему присудили Нобелевскую премию в области химии. Он первым добился искусственного превращения одного элемента в другой, воплотив в жизнь тысячелетнюю мечту химиков. После смерти Крокодил, как за сильный характер прозвали его коллеги и ученики, был похоронен в Вестминстерском аббатстве. Новозеландец покоится рядом с великими деятелями английской науки.
У атомов тоже есть сердце. Резерфорд. Атомное ядро. - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
В отношении атомов Дальтон настаивал, что они неделимы, что их невозможно ни создать, ни уничтожить, то есть в химических процессах происходит лишь изменение комбинаций атомов. Он выяснил, что каждый элемент состоит из атомов одного типа, схожих между собой и различающихся с атомами других элементов. Одна из отличительных характеристик, которые Дальтон установил для них, относилась к атомному весу. Он также утверждал, что атомы комбинируются при создании химических соединений.
Его убежденность в том, что атомы невозможно разрушить, привела его к отстаиванию закона о сохранении материи (ранее предложенного Лавуазье): "Мы могли бы с таким же успехом попытаться внести в Солнечную систему новую планету или уничтожить одну из уже существующих, как и создать или уничтожить частицу водорода". Тем не менее труды Резерфорда, которые мы рассмотрим в следующей главе, позволили доказать, что представление Дальтона было неполным.
В XIX веке многие ученые полагали, что переход от макроскопического к микроскопическому миру, понимание которого основывалось на научном эксперименте, неприемлем ввиду невозможности непосредственного наблюдения микроскопического мира. Критики атомизма нашли много аргументов, отстаивая свою позицию в рамках позитивизма. Для основателя этого философского движения, французского социолога Огюста Конта (1798-1857), наука опиралась на констатацию фактов. Любое утверждение, касающееся окружающей реальности, не подпитанное фактами, расценивалось как метафизическое размышление и отвергалось наукой. С точки зрения позитивизма атомизм обладал всеми чертами метафизического пустословия.
Одним из наиболее настойчиво противостоявших атомизму ученых был Жан-Батист Дюма (1800-1884):
"Что остается от амбициозного экскурса, совершенного нами в сферу атомов? Похоже, ничего основательного. Разве только убеждение, что химия сбивается с пути всякий раз, когда оставляет дорогу эксперимента и пытается продвигаться в потемках [...]. Если бы я мог, я бы вычеркнул слово "атом" из науки, потому что убежден: это понятие выходит далеко за пределы экспериментов".
Критика атомов наталкивалась на полярное к ним отношение других химиков, например Уильяма Праута, который в 1815 году пришел к выводу, что все атомы на самом деле являются соединениями атомов водорода (что напрямую связано с доказательством Резерфорда).
Кто-нибудь когда-нибудь видел молекулу газа или атом?
Марселен Бертло (1827-1907), французский химик и историк
Появлялось все больше свидетельств существования атомов, но из-за отсутствия возможности прямой проверки ученые предпочитали отвергать гипотезу, стремясь исключить из науки чисто умозрительные измышления, к тому же многие из них считали прямую проверку чем-то выходящим за пределы человеческих возможностей.

Согласно кинетической теории газов газ состоит из атомов и молекул, находящихся в постоянном движении, сталкивающихся между собой и со стенками сосуда. При большем количестве накопленной энергии частицы двигаются быстрее, столкновений больше, а температура увеличивается.
Острая полемика, возникшая в химической науке, распространилась и на физику. Теперь сторонники атомов включили в обсуждение термодинамику и изучение теплоты. Если в отношении теплоты еще можно отметить, что физики сконцентрировались на изучении макроскопических факторов и наблюдаемых в действительности явлений, то открытия Джеймса Клерка Максвелла и Людвига Больцмана перевернули данное представление. Оба ученых исследовали известные понятия с позиции движения атомов, при этом они не ограничились индивидуальной траекторией отдельного атома, а попытались рассчитать статистическое поведение множества атомов.
Согласно этой теории газ состоит из множества атомов, которые сталкиваются между собой и со стенками сосуда, в котором находится газ, как бильярдные шары (см. рисунок). Максвелл и Больцман установили, что средняя энергия отдельного атома газа в постоянном движении связана с давлением и температурой.
Так же как это происходило в химической науке, многие физики с недоверием относились к атомной теории. Тому имелось множество причин, среди которых, например, принцип экономии мысли. Объяснять то, что можно наблюдать, и отказываться от того, что наблюдать нельзя, многим ученым (в их числе австрийцу Эрнсту Маху) представлялось ошибкой.
В 1906 году Больцман, всю жизнь защищавший атомизм, совершил самоубийство, незадолго до того, как Резерфорд вторгся в мир атомов.
Сомнения и конфронтации относительно атомов начали ослабевать в тот момент, когда были открыты составляющие внутренней структуры атома: сначала электроны, позже протоны, несколько десятилетий спустя — нейтроны. От химиков работа перешла в руки физиков (хотя часто сферы исследования обеих дисциплин пересекаются). Французский физик и философ науки Анри Пуанкаре (1854-1912) так охарактеризовал поворот, произошедший в отношении атомов:
"Атомная гипотеза в последнее время стала такой основательной, что больше не кажется гипотезой: атомы — не просто полезная выдумка, мы можем сказать, что видим их, так как способны их подсчитать".
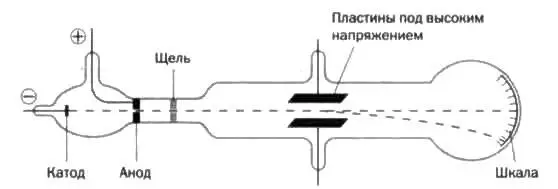
РИС .6
В 1897 году появилась возможность измерить удельный заряд электрона. Британский физик Джозеф Джон Томсон (1856-1940) впервые обнаружил отрицательно заряженные частицы, которые получили название электронов. Открытие их природы и основной характеристики стало большим достижением.
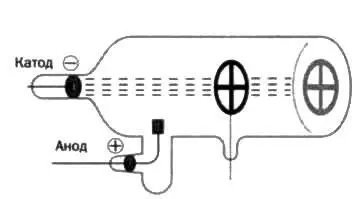
РИС. 7
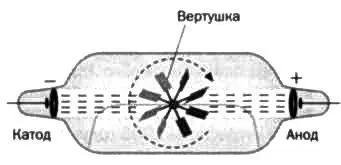
РИС . 8
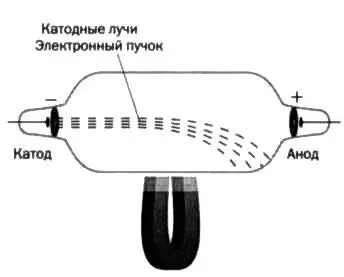
РИС . 9
Этот прорыв оказался возможным благодаря катодным лучам, представляющим собой электронные пучки, то есть поток электронов, испускаемых трубкой Крукса с небольшим количеством разреженного газа и впаянными в нее анодом и катодом (см. рисунок 6). При разности потенциалов появляются катодные лучи (электронные пучки), дающие зеленоватый флуоресцентный свет при прохождении через край стеклянной трубки. Их основная характеристика — прямолинейное перемещение — была обнаружена, когда посередине трубки установили объект и на дальней стенке появилась его тень (см. рисунок 7).
Читать дальшеИнтервал:
Закладка:








