Паоло Пелоси - Обоняние [Увлекательное погружение в науку о запахах]
- Название:Обоняние [Увлекательное погружение в науку о запахах]
- Автор:
- Жанр:
- Издательство:Литагент Аттикус
- Год:2020
- Город:Москва
- ISBN:978-5-389-19087-0
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Паоло Пелоси - Обоняние [Увлекательное погружение в науку о запахах] краткое содержание
«Мы часто не обращаем внимания на запахи и почти всегда их недооцениваем. Между тем они тайно влияют на наше настроение, предопределяют выбор и вообще делают жизнь куда более приятной. Наш нос непрерывно бомбардируют разнообразные молекулы, даже если мы ничего не нюхаем специально. Агрессивные запахи нас отталкивают и нередко спасают от потенциально опасных ситуаций, приятные кажутся неодолимо привлекательными, и зачастую все это происходит исподволь, так, что мы ничего не осознаем. Ароматы вызывают эмоции и внезапно возвращают к жизни воспоминания, давно спрятанные в глубинах памяти» (Паоло Пелоси).
Обоняние [Увлекательное погружение в науку о запахах] - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Органические соединения, к которым относится большинство молекул, составляющих живой организм, основываются на несущих конструкциях из атомов углерода, связанных друг с другом в ту или иную трехмерную структуру. Среди девяноста двух природных химических элементов, встречающихся на Земле, только углерод способен создавать стабильные связи между собственными атомами и благодаря этому сооружать комплексные структуры: линейные или разветвленные цепочки, кольца и даже трехмерные фигуры. Их можно рассматривать как скелеты, на которых затем строятся более сложные молекулы.
Бывает, что в скелет включаются также атомы кислорода, азота, реже серы и других элементов. К этому каркасу, который нам пока еще удобно представлять в виде шариков и палочек, нужно добавить еще атомы водорода в количестве, достаточном, чтобы насытить валентности углерода. Чтобы построить модель, соответствующую реальной молекуле, необходимо насытить валентности всех атомов, то есть установить все возможные связи между ними. Для этого нужно только запомнить, что атом углерода образует четыре связи (выражаясь более научно, валентность углерода – 4), азот – три, кислород – две, а водород – только одну.
Еще один важный фактор – размер молекулы, как в плане занимаемого ею места, так и в плане массы. Часто молекулярная масса молекулы принимается за показатель размера: этот параметр легко вычислить, сложив атомные массы отдельных атомов. Чтобы еще упростить себе задачу, мы пользуемся относительными измерениями, принимая атомную массу водорода, самого маленького атома, за единицу и отсчитывая массы других атомов от нее. Масса атома углерода эквивалентна массе 12 атомов водорода; азота – 14; кислорода – 16. Соответственно, мы говорим, что атомная масса углерода – 12 и т. д. Выходит, что вклад самих атомов водорода в общий размер молекулы сравнительно невелик, и поэтому химики иногда упрощают модель и вовсе игнорируют их присутствие.
Связи между атомами (и черточки между их химическими символами) образуют топологию молекулы и позволяют построить ее трехмерную модель. Записывая структуру какой-нибудь сложной молекулы, мы нередко опускаем символы углерода и водорода и даже сами связи между их атомами. Это емкое, синтетическое обозначение показывает фактически только скелет молекулы, но все равно содержит всю информацию, необходимую для построения полной модели. На рисунке 2 показаны структуры трех разных молекул: открытая цепочка, кольцевая и ароматическая. Каждая представлена тремя разными способами, от синтетической структурной нотации до пространственной модели, довольно точно отображающей реальную форму и размер молекулы.
Первая структура – это 1-деканол, дециловый спирт. Его молекула выглядит как длинная цепочка из атомов углерода со спиртовой группой на одном конце. В виде модели она похожа на гусеницу и, подобно гусенице, очень гибка, способна принимать самую разную форму – и прямую, и свернутую, и волнообразную. Вторая – циклогексанол. Здесь спиртовая группа прикреплена к циклической структуре из шести атомов углерода. Такая молекула тоже довольно гибка и обычно имеет форму стульчика. Третий пример – ароматическая молекула, фенол. Ее кольцо плоское и жесткое, что объясняется свойствами некоторых электронов, связывающих атомы углерода друг с другом. Каждый из углеродных атомов кольца использует один электрон, чтобы присоединиться к следующему атому углерода, а другой при этом включается во что-то вроде заряженного облака, равномерно охватывающего всю структуру. У всех соединений, которые мы называем ароматическими, плоская форма и особые химические свойства.
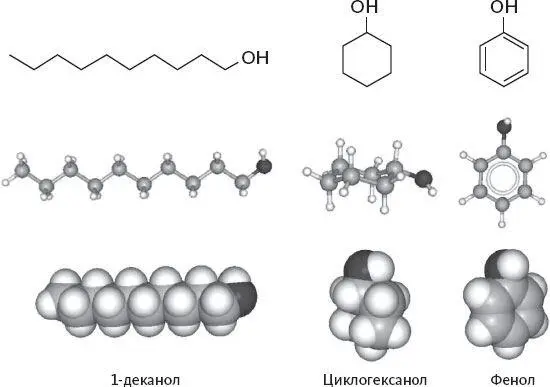
Рисунок 2.Разные способы отображения молекулярной структуры. Вверху: сокращенная структура. Каждый угол соответствует атому углерода; атомы водорода не показаны; представлены только связи между основными атомами. В середине: модель из шариков и палочек. Все атомы водорода показаны. Внизу: трехмерная модель, довольно реалистично передающая размер и форму молекулы.
Вернемся теперь к нашему первому вопросу: можно ли предсказать, как будет пахнуть химическое вещество, просто посмотрев на его молекулярную структуру? И наоборот, можно ли создать молекулу с конкретным желаемым ароматом?
На оба вопроса можно ответить кратко: нет. Чарльз Селл, химик, занимающийся созданием новых ароматов, много раз получал такие задания и в конце концов суммировал свои выводы в статье с совершенно недвусмысленным названием: «О непредсказуемости запахов». Его аргументация сводится к чрезвычайной сложности ольфакторного кода, которая не дает ученым анализировать и воспроизводить запахи со сколько-нибудь заметной точностью [1].
Однако, если выдвинуть более скромные требования и ограничить запрос определенным типом запаха или группой химических структур, ситуация окажется более оптимистичной: мы сможем воспроизвести натуральный, природный запах с помощью молекул, придуманных и синтезированных в лабораторных условиях. Крупные исследовательские группы (в том числе и организованная Чарльзом Селлом) потратили немало времени и средств на синтез новых химических веществ с заданным запахом, но при этом более простых в производстве, более экономичных или менее токсичных, чем те, которые встречаются в природе [2].
Проблема в том, что обонятельная система оказалась гораздо более сложной, чем полагали ранее, а потому все исследования в этой области идут медленно и с трудом. Чтобы изучать такую хитрую систему, приходится строить упрощенные модели, подчас довольно далекие от реальной биологической картины и дающие очень грубые и ограниченные результаты. Но результаты хотя бы есть, и это уже хорошо.
Простые одоранты
Возможно, у читателя уже появилось ощущение, что мы задаем слишком много вопросов и вообще вот-вот заблудимся в лабиринте, из которого уже не выберемся.
Стало быть, самое время вернуться к эмпирике, к тем простым, знакомым ольфакторным явлениям, из-за которых утренняя чашка кофе так вкусна и бодряща, открытые двери кондитерской так заманчивы, а какой-нибудь старый кларет хочется пить с закрытыми глазами, погрузившись в мечты. Впрочем, само собой, обонятельный опыт бывает и неприятным – зато он помогает нам обходить маленькие подарочки, оставленные на тротуаре чьей-то собакой, и предупреждает, что холодильник пора почистить (и сделать это стоило еще позавчера).
Давайте соотнесем каждый такой опыт с той или иной молекулярной структурой и попробуем прочесть запахи, пользуясь языком химии. Для этого нам придется максимально упростить входящие данные и выбрать ряд конкретных запахов и молекул. Проблема, однако, в том, что большинство воспринимаемых нами запахов порождаются сочетаниями множества разных молекул, каждая из которых воздействует на наши хемосенсорные нейроны по-своему, вызывая в них комплексные реакции. Так обстоит дело почти со всеми ароматами, с которыми мы сталкиваемся во время приготовления и употребления пищи, да и в целом в окружающей среде. Всякий такой запах рождается от множества разных химикатов, которые формируют перцептивные картины и эмоции только сообща и только в данной относительной пропорции: примерно так же звуки разных инструментов в оркестре образуют симфонию.
Читать дальшеИнтервал:
Закладка:
![Обложка книги Паоло Пелоси - Обоняние [Увлекательное погружение в науку о запахах]](/books/1061157/paolo-pelosi-obonyanie-uvlekatelnoe-pogruzhenie-v.webp)



![Паоло Бачигалупи - Орудие войны [litres с оптимизированной обложкой]](/books/1094305/paolo-bachigalupi-orudie-vojny-litres-s-optimiziro.webp)



