Ольга Шестова - 30 Нобелевских премий: Открытия, изменившие медицину [litres]
- Название:30 Нобелевских премий: Открытия, изменившие медицину [litres]
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2020
- Город:Москва
- ISBN:978-5-0013-9245-3
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ольга Шестова - 30 Нобелевских премий: Открытия, изменившие медицину [litres] краткое содержание
Открытия объединены по темам и собраны в шести главах, посвященных физиологии, генетике, патогенам, медицинским методам и фармакологии. Чтение можно начать с любой главы – с той темы, которая вам кажется самой интересной.
30 Нобелевских премий: Открытия, изменившие медицину [litres] - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Открытие Ландштейнера сначала не нашло в научном сообществе должного отклика – возможно, из-за скромного, «кабинетного» характера первооткрывателя. Это привело к тому, что группы крови еще несколько раз «переоткрыли». В 1907 году чех Ян Янский назвал группы крови I, II, III и IV по частоте, с которой они встречались. А американец Уильям Мосс из Балтимора в 1910 году описал четыре группы крови в обратном порядке – IV, III, II и I. Номенклатура Мосса широко использовалась, например, в Англии, и когда она встречалась с номенклатурой Янского, это приводило к серьезным проблемам.
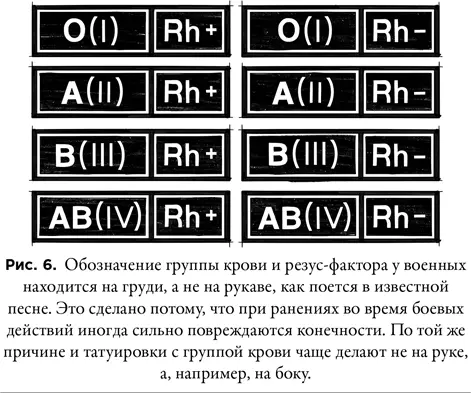
Путаница прекратилась, когда в 1937 году на съезде Международного общества переливания крови в Париже была принята нынешняя терминология «АВ0», в которой группы крови именуются 0 (I), A (II), B (III), AB (IV). Собственно, это и есть терминология Ландштейнера, к которой добавилась четвертая группа.
Это открытие кардинально повлияло на многие сферы жизни. Во-первых, оно свело к минимуму риск при переливании крови и спасло множество жизней – особенно во время войны. Заблаговременное определение группы крови возможного донора и реципиента предупреждало трансфузии несовместимой крови и смерти солдата.
Во-вторых, криминалисты получили новый полезный инструмент для расследования. Оказалось, что определение группы возможно даже в незначительном количестве засохшей крови, оставленной на месте преступления. Это стало серьезным подспорьем для судебной медицины.
В-третьих, как только исследователи поняли, что группы крови наследуются из поколения в поколение, открытие Ландштейнера взяли на вооружение антропологи. Они стали выяснять, как распределение групп крови варьируется по географическим зонам, и делать выводы о происходивших в доисторические времена перемещениях народов. А эпидемиологи нашли прямую зависимость между группой крови, распространенной в той или иной зоне, и стойкостью иммунитета к инфекционным заболеваниям, таким как чума и оспа.
В-четвертых, стало возможным с определенной долей достоверности определение отцовства. Сравнивая группу крови ребенка (Х) и предполагаемого отца (Y), можно дать один из двух ответов: «Y может быть отцом Х» или «Y не может быть отцом Х». Более точный и развернутый ответ дают результаты сравнения ДНК ребенка и предполагаемого отца, но это стало возможным только в последние десятилетия, и метод из-за его дороговизны применяют редко.
Сегодня изучены и охарактеризованы десятки групповых антигенных систем крови, таких как системы Даффи, Келл, Кидд, Льюис, Лютеран и др. Их количество постоянно растет, однако основной по-прежнему остается классификация группы крови, предложенная Карлом Ландштейнером.
Сам Ландштейнер уже после своего открытия продолжал работать над совершенствованием классификации крови. В 1939 году, в возрасте 70 лет, он получил звание «Почетный профессор в отставке», продолжил исследовательскую деятельность и через год вместе с коллегами-учениками Александром Винером и Филиппом Левиным открыл резус-фактор крови человека. Параллельно исследователи выявили связь между ним и развитием гемолитической желтухи у новорожденных: резус-положительный плод может вызывать у матери выработку антител против резус-фактора, а это приводит к гемолизу эритроцитов, превращению гемоглобина в билирубин и развитию желтухи. Раньше такие дети чаще всего погибали. Чтобы спасти их, акушеры-гинекологи и неонатологи принимают превентивные меры, применяя полное заместительное переливание крови.
С чего начинается пищеварение
Кристиан де Дюв
Альбер Клод
Джордж Паладе
Некоторые книги могут повлиять на наш профессиональный или жизненный путь. Так, для одного из авторов этого издания стала решающей встреча с «Путешествием в мир живой клетки» известного бельгийского биолога, лауреата Нобелевской премии Кристиана де Дюва. Эту книгу Ольга Шестова прочитала еще в школе. Автор предлагал читателям вообразить, как они сжимаются до размера, меньшего самой мелкой органеллы клетки. Далее Кристиан де Дюв советовал мысленно надеть защитный костюм – нечто среднее между скафандром, формой пожарника и снаряжением водолаза, – протиснуться сквозь отверстия в мембране клетки и оказаться в ее цитоплазме, чтобы совершить путешествие, полное опасностей. Особенно Ольгу поразило приближение к лизосомам, грозящим растворить «чужаков» в своем содержимом – едком, наполненном ферментами, разлагающими белки на составные части. Связь клеточной биологии и медицины, описанная в книге де Дюва, так увлекла юную Ольгу, что она поступила на биологический факультет МГУ, а позже защитила диссертацию на медицинскую тему.
Книга Кристиана де Дюва была основана на его открытии. Вместе со своими коллегами Альбером Клодом и Джорджем Паладе он получил за него в 1974 году Нобелевскую премию: «За открытия, касающиеся структурной и функциональной организации клетки».
Клетку начали пристально изучать с середины XIX века, но силы светового микроскопа, который имелся тогда в распоряжении биологов, было недостаточно, чтобы в подробностях познакомиться со структурой и функциями ее частей. Перелом наступил в середине 1940-х годов с появлением двух новых технологий. Во-первых, электронный микроскоп с высоким разрешением, изобретенный несколькими годами ранее, позволил изучить клеточные структуры. Во-вторых, была разработана методика химического анализа веществ, которые можно было увидеть под электронным микроскопом. Для этого гомогенизированные ткани или клетки с помощью центрифуги разделяли на компоненты, сходные по размеру и весу. Дифференциальное центрифугирование дополнило структурные исследования с помощью электронного микроскопа.
Альбер Клод, работавший в 1930–40-х годах в Рокфеллеровском университете в Нью-Йорке, был лидером в обеих прорывных технологиях: и в работе с электронным микроскопом для исследования клеток животных, и в совершенствовании дифференциального центрифугирования. Первые электронно-микроскопические снимки клеток и их компонентов, содержащие новую и актуальную биологическую информацию, были получены примерно в 1945 году. До сих пор этот метод с некоторыми усовершенствованиями остается одним из важнейших в клеточной биологии.
Молодые коллеги Клода продолжили его дело. Джордж Паладе начал с морфологического, описательного изучения области клетки, окружающей ядро, – цитоплазмы. Джордж изучал сеть мембран, которую первоначально обнаружил Клод. Такие мембраны еле заметны в световой микроскоп: это – эндоплазматический ретикулум. Исследователи показали, что ретикулум больше всего похож на пустой и многократно сложенный мешок, занимающий большую часть цитоплазмы. Палладе обнаружил и описал мелкие гранулированные компоненты (рибосомы) на наружной части складок этого мешка и открыл, что они производят (синтезируют) белок в клетке. В серии работ Паладе и его коллеги показали множество увлекательных деталей процесса производства белка. Например, то, каким образом белки, синтезируемые в клетках на рибосомах, находящихся снаружи ретикулума, попадают в пространство между его мембранами и мигрируют далее в специальную органеллу – аппарат Гольджи.
Читать дальшеИнтервал:
Закладка:
![Обложка книги Ольга Шестова - 30 Нобелевских премий: Открытия, изменившие медицину [litres]](/books/1066631/olga-shestova-30-nobelevskih-premij-otkrytiya-izm.webp)





![Ольга Шестова - Красивое долголетие [10С против старения] [litres]](/books/1076254/olga-shestova-krasivoe-dolgoletie-10s-protiv-star.webp)



