Сергей Титов - Естествознание. Базовый уровень. 10 класс
- Название:Естествознание. Базовый уровень. 10 класс
- Автор:
- Жанр:
- Издательство:Array Литагент «Дрофа»
- Год:2013
- Город:Москва
- ISBN:978-5-358-13589-5
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Сергей Титов - Естествознание. Базовый уровень. 10 класс краткое содержание
Учебник объединяет сведения об основных законах и закономерностях, наиболее важных открытиях и достижениях в области химии, физики, астрономии, что формирует у учащихся представление о природе как целостной системе, а также о взаимосвязи человека, природы и общества.
Современное оформление, многоуровневые вопросы и задания, дополнительная информация и возможность параллельной работы с электронным приложением способствуют эффективному усвоению учебного материала.
Учебник адресован учащимся 10 класса.
Естествознание. Базовый уровень. 10 класс - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
1. Изобразите схематично строение нуклеотида ДНК.
2. Какими связями соединены между собой две цепочки ДНК?
3. Назовите моносахариды, из которых состоит большинство биологических полисахаридов.
4. Какой полисахарид служит запасающим веществом в растительном организме, а какой – в животном организме?
5. Сравните строение молекул ДНК и РНК.
6. Достаточно ли знать, какой моносахарид входит в состав нуклеотидов, чтобы понять, о какой нуклеиновой кислоте идёт речь?
1. Используя знания, полученные при изучении биологии растений, объясните, почему в растительных организмах углеводов значительно больше, чем в животных.
2. Участок одной из цепочек ДНК имеет вид ГГЦАТТЦГАА. Как будет выглядеть комплементарная ей цепочка ДНК?
§ 58 Соединения, необходимые для существования жизни: белки, липиды
Одними из наиболее важных биополимеров, без которых невозможно представить себе существование жизни, являются белки. Мономеры белков – это аминокислоты. Аминокислота обязательно имеет в своём составе карбоксильную группу (—СООН) и аминогруппу (—NH 2) (рис. 152). R – это радикал, который может быть просто атомом водорода, а может представлять собой сложное органическое соединение. В состав белков живого организма входит двадцать аминокислот, отличающихся по строению радикала.
В молекуле белка аминокислоты соединены пептидной связью, которая образуется между карбоксильной группой одной аминокислоты и аминогруппой другой (см. рис. 152). При образовании такой связи от карбоксильной группы отщепляется гидроксил, от аминогруппы – атом водорода, а освободившиеся валентные связи углерода и азота соединяют остатки двух аминокислот. Гидроксильная группа и водород взаимодействуют друг с другом, образуя молекулу воды. Таким образом, синтез белка – это реакция поликонденсации. Вещество, состоящее из последовательности аминокислот, соединённых пептидными связями, называют пептидом. Молекула из двух аминокислотных остатков – это дипептид, из трёх – трипептид и т. д. Если аминокислотных остатков в пептиде много, его называют полипептидом. Число аминокислотных остатков в молекуле белка может варьировать от нескольких сотен до нескольких тысяч. Какой бы длинной ни была полипептидная цепь, она никогда не разветвляется и всегда начинается с аминогруппы (N-конец цепи), а заканчивается карбоксильной группой (C-конец цепи).
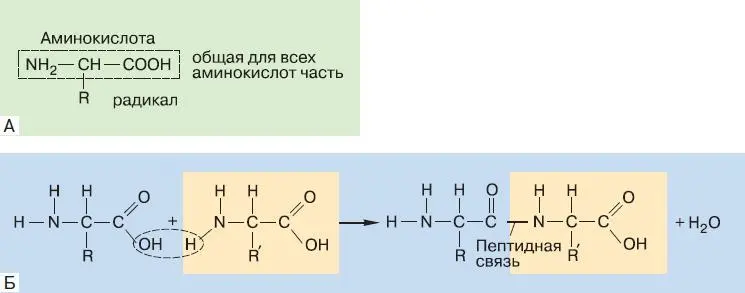
Рис. 152. Общая структурная формула аминокислот, входящих в состав белков (А), и образование пептидной связи (Б)
Линейная последовательность аминокислот в белковой цепи – это первичная структура белка (рис. 153). Она уникальна для любого типа белка и определяет форму его молекулы, свойства и функции. Цепочка из аминокислотных остатков либо складывается зигзагом, либо сворачивается в спираль, формируя вторичную структуру. Эта структура возникает в результате образования связей между группами = С=О и H – N = разных аминокислотных остатков полипептидной цепи.
Складчатая или спиральная молекула сворачивается дальше, образуя третичную структуру. Прочность третичной структуры обеспечивается ионными, водородными, дисульфидными и другими связями. Свёрнутую спираль полипептида обычно называют глобулой (от лат. globulus – шарик). В форме третичной структуры белок уже может выполнять свои функции.
Некоторые белки имеют ещё и четвертичную структуру, которая образуется при соединении нескольких глобул. Например, гемоглобин человека представляет собой комплекс из четырёх таких субъединиц.
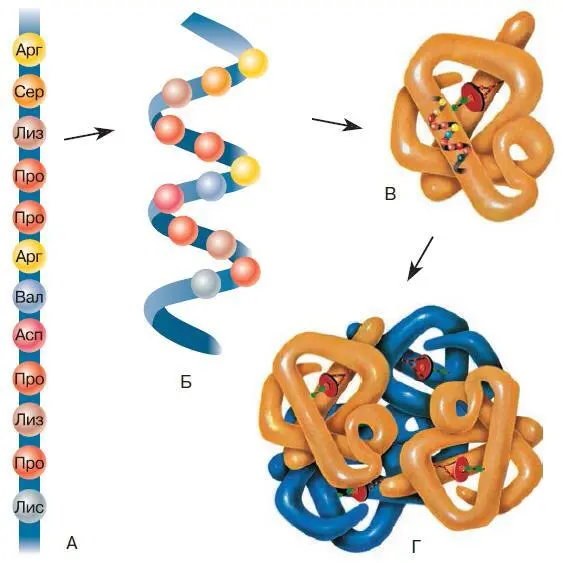
Рис. 153. Первичная (А), вторичная (Б), третичная (В) и четвертичная (Г) структуры белка
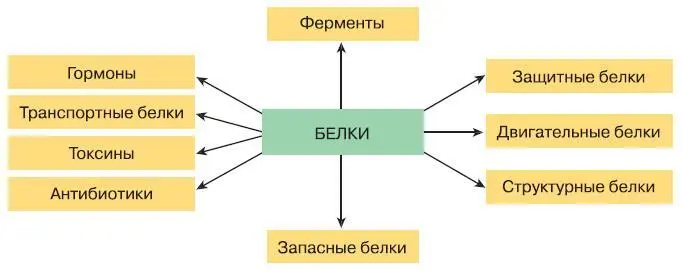
Рис. 154. Функции белков
Огромное разнообразие белковых молекул подразумевает столь же широкое разнообразие их функций (рис. 154). Около 10 000 белков– ферментов служат катализаторами химических реакций. Вторая по величине группа белков выполняет структурную и двигательную функции. Белки участвуют в образовании всех мембран и органоидов клетки. Белок коллаген входит в состав межклеточного вещества соединительной и костной ткани, а основным компонентом волос, рогов и перьев, ногтей и копыт является белок кератин. Сократительную функцию мышц обеспечивают белки актин и миозин. Транспортные белки связывают и переносят различные вещества и внутри клетки, и по всему организму. Белки-гормоны обеспечивают регуляторную функцию.
При попадании в организм человека чужеродных белков, вирусов или бактерий на защиту встают иммуноглобулины – защитные белки. Фибриноген и протромбин обеспечивают свёртываемость крови, предохраняя организм от кровопотери. Белками являются сильные микробные токсины, например ботулиновый, дифтерийный, холерный.
При нехватке пищи в организме животных начинается активный распад белков до конечных продуктов, и тем самым реализуется энергетическая функция этих веществ.
Утрату белковой молекулой своей структурной организации: четвертичной, третичной, вторичной, а при более жёстких условиях – и первичной структуры называют денатурацией (рис. 155). В результате денатурации белок теряет способность выполнять свою функцию. Причинами денатурации могут быть, например, нагревание, ультрафиолетовое излучение.
Денатурация может быть обратимой и необратимой. Если при воздействии денатурирующих факторов разрушения первичной структуры молекулы не произошло, при наступлении благоприятных условий денатурированный белок может вновь восстановить свою трёхмерную форму.
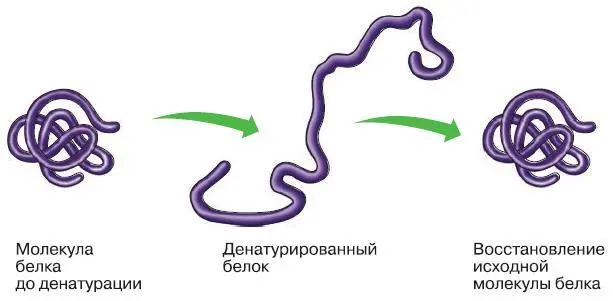
Рис. 155. Денатурация белка
Этот процесс называют ренатурацией ,и он убедительно доказывает, что третичная структура белка зависит от последовательности аминокислотных остатков, т. е. от его первичной структуры.
Среди низкомолекулярных органических соединений, входящих в состав живых организмов, важную роль играют липиды. К этой группе относят жиры, воски и различные жироподобные вещества. Это гидрофобные соединения, нерастворимые в воде. Жиры по химическому строению представляют собой соединение трёхатомного спирта – глицерина с остатками жирных кислот (рис. 156). Жирные кислоты могут быть ненасыщенными или насыщенными, в зависимости от того, имеют они в структуре своей молекулы двойную связь или нет. Соответственно, образованные ими жиры тоже делятся на ненасыщенные и насыщенные. Ненасыщенные жиры при комнатной температуре находятся в жидком состоянии. Из жиров, употребляемых человеком в пищу, к ним относятся растительные масла (подсолнечное, кукурузное, оливковое и др.). Насыщенные жиры при такой температуре находятся в твёрдом состоянии, в чём легко убедиться на примере сливочного масла и сала. Если через ненасыщенное растительное масло пропустить при определённых условиях водород, он присоединится по месту двойной связи в остатке жирной кислоты, и жир станет насыщенным. Подобным образом из растительного масла получают маргарин.
Читать дальшеИнтервал:
Закладка:










