Владимир Антонов - Эфир. Русская теория.
- Название:Эфир. Русская теория.
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Владимир Антонов - Эфир. Русская теория. краткое содержание
Эфир. Русская теория. - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
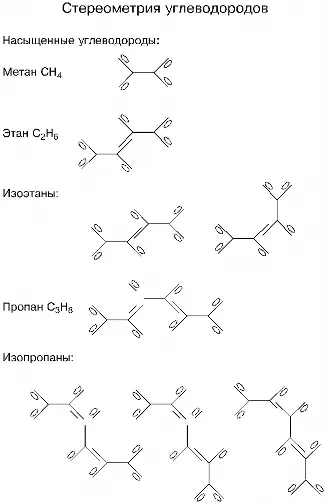
Стереометрия позволяет ответить на вопрос: почему некоторые углеводороды газообразны, другие в нормальных условиях являются жидкостями, а третьи — твердыми? Отметим, что газообразны мелкомолекулярные углеводороды: метан, этан, пропан, бутан; жидкостями являются углеводороды с более крупными молекулами, начиная с пентана, молекулы которого содержат по пять атомов углерода, — и кончая углеводородом с шестнадцатью атомами углерода в молекуле; и наконец, твердыми являются парафины, молекулы которых содержат более девятнадцати атомов углерода; наиболее твердые парафины — их называют церезинами —имеют молекулы, содержащие более тридцати семи атомов углерода, и мелкокристаллическую структуру.
Ответ на поставленный вопрос будем искать все в той же пушистости. Атомы углерода сами по себе не имеют противоборствующих участков и поэтому не пульсируют. Пульсируют и очень интенсивно атомы водорода — мы об этом знаем. Так вот, в соединениях тех и других, то есть в углеводородах, углерод не подавляет колебания водородных атомов, и те создают вокруг него стоячие тепловые поля; плотность их вокруг молекулы может быть такой, что она вся превратится в пушистую частицу; а это уже — главный признак газообразности. Получается так, что атомы водорода своим порханием и своим стремлением поднять атом углерода в воздух напоминают сказочных пташек, уносящих с собой в высь прицепившуюся лягушку. Если у этих пташек — у водородных атомов — хватает сил, они делают молекулу газообразной; если не хватает, то — жидкостной; а уж если совсем не будет сил, то молекула останется прилипшей к твердому телу.
Кроме того пушистость углеводородной молекуле придают петлевые соединения атомов углерода; каждое такое соединение можно приравнять в этом смысле к одному атому водорода. Сказываются также расположение атомов водорода в молекулах углеводородов, конфигурация молекул, разумеется — температура и другие факторы.
Если учитывать только отношение количества атомов водорода плюс количество петлевых соединений к количеству атомов углерода в молекулах (назовем такое отношение коэффициентом пушистости), то у газообразных насыщенных углеводородов оно изменяется в пределах от 4 у метана (температура кипения минус 164,5 градуса Цельсия) до 3,25 у бутана (температура кипения минус 0,5 градуса); у жидкостных этот коэффициент колеблется от 3,2 у пентана (кипение при 36,1 градуса) до 3,063 у углеводорода с шестнадцатью атомами углерода; у парафинов — 3,053 до 3,029, а у церезинов — от 3,027 до 3,019.
Можно отметить еще такую закономерность: атомы водорода, располагающиеся на наружных сторонах петель углерода, создают большую пушистость, чем те, что располагаются на внутренних. Так у бутана, имеющего четыре наружных водорода, температура кипения равна минус 0,5 градуса, а у изобутана с пятью наружными водородами температура кипения еще ниже и составляет минус 11,7 градуса. То же самое наблюдается у жидкостей: пентан с шестью наружными водородами закипает при 36,1 градуса Цельсия, а изопентан с семью наружными водородами при 27,9 градуса.
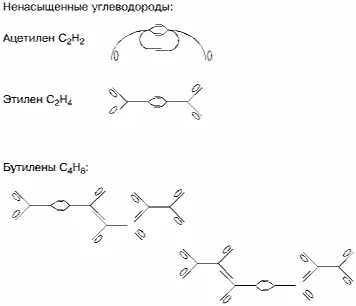
Стереометрия ненасыщенных углеводородов — несколько сложнее. Возьмем для примера ацетилен, молекула которого состоит из двух атомов углерода и двух атомов водорода. Он получается при реагировании карбида кальция с водой или из метана при пропускании через него электрических разрядов. Отличительной особенностью стереометрии ацетилена является тройная связь атомов углерода в его молекулах. Это означает, что, во-первых, петли с внутренними присасывающими сторонами одного атома углерода охватывают петли с наружными присасывающими сторонами второго атома, и во-вторых, из оставшихся петель две, по одной от каждого атома, загнуты навстречу друг другу и образуют накладку типа той, что есть у атома гелия; и только оставшиеся незамкнутыми остальные две петли соединены с атомами водорода.
Позволим себе предположить, как возникает молекула ацетилена в момент проскакивания электрического разряда в метане. Разряд превращает метан в плазму; по-просту говоря, он срывает с атомов углерода атомы водорода. Освободившиеся атомы углерода соединяются между собой по-парно максимально возможным образом, то есть тремя петлями, как было сказано выше. Те петли, что образуют гелиевую накладку, стягиваясь, изогнут вновь образованную молекулу так, что две оставшиеся незамкнутыми петли не смогут дотянуться друг до друга и вынуждены будут поймать и присосать к себе находящиеся поблизости атомы водорода.
Характерной чертой стереометрии ненасыщенных углеводородов является двойная связь атомов углерода, когда петли с внутренними присасывающими сторонами одного атома охватывают петли с наружными сторонами другого атома; назовем такое соединение скобою. Она наблюдается и у ацетилена, и у этилена, и у бутилена, и у всех других ненасыщенных углеводородов; благодаря ей количеств атомов водорода в молекулах таких углеводородов уменьшается.
Скоба сильно пульсирует; ее пушистость можно оценить приблизительно в 3,1 тепловых поля атомов водорода. С учетом этого коэффициент пушистости этилена оказывается равным 3,55, и он по газообразности располагается между метаном (4) и этаном (3,5); температура вскипания этилена (минус 103,8 градуса Цельсия) выше чем у метана (минус 164,5 градуса), но ниже чем у этана (минус 88,6 градуса). Коэффициент пушистости бутилена с учетом действия скобы составляет 3,275, и бутилен со своей температурой кипения минус 6,3 градуса располагается между пропаном (коэффициент пушистости 3,33, температура кипения минус 42,1 градуса) и бутаном (коэффициент 3,25, температура минус 0,5).
Особая пушистость — у ацетилена; эта особенность вызвана его оригинальной стереометрией. Если оценить пушистость гелиевой накладки в 1,7 водородных тепловых поля, то коэффициент пушистости ацетилена составит 3,4, и он со своей температурой кипения минус 75 градусов займет место между этаном и пропаном.
Завершая разговор об углеводородах, отметим их бесцветность; она объясняется все тем же: атомы в молекулах углеводородов не имеют таких длин прямолинейных участков шнуров, которые колебались бы («звучали») на видимых человеческим глазом частотах.
Стереометрия и топология карбидов
Карбиды, то есть соединения углерода с металлами (и некоторыми неметаллами, например с кальцием), имеют свою особую стереометрию; она характерна тем, что атомы в них соединяются не петлями, как в углеводородах, а желобами; при этом конфигурация атомов сильно видоизменяется, то есть стереометрия карбидов сопрягается с топологией атомов в них. Некоторое изменение форм атомов углерода наблюдалось, как мы видели, и в аллотропических модификациях, и в молекулах углеводородов; но там это выражалось в основном в развороте или отгибе концевых петель; но стволы атомов, состоящие из спаренных желобов, сохранялись почти неизменными. В карбидах атомы углерода могут трансформироваться до неузнаваемости.
Читать дальшеИнтервал:
Закладка: