В. Рачков - Чудесные кристаллы
- Название:Чудесные кристаллы
- Автор:
- Жанр:
- Издательство:Воениздат
- Год:1962
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
В. Рачков - Чудесные кристаллы краткое содержание
Автор брошюры рассказывает о том, как было открыто пьезоэлектричество, какова физическая сущность этого явления, какими свойствами обладают пьезокристаллы.
В брошюре говорится об устройстве пьезоэлектрических приборов и их применении в различных областях науки и техники. Особое внимание уделено применению этих приборов в военном деле
Брошюра рассчитана на широкий круг читателей.
Чудесные кристаллы - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Чем же руководствовались братья Кюри в своем открытии? Какие свойства кристаллов их интересовали?
Чтобы ответить на эти вопросы, необходимо вспомнить строение вещества и рассказать о свойствах кристаллов.
В МИРЕ КРИСТАЛЛОВ
Известно, что окружающие нас тела состоят из мельчайших невидимых глазом частиц — атомов. Размеры атомов чрезвычайно малы: они составляют стомиллионные доли сантиметра. Атомы объединяются в молекулы, более крупные частицы.
Молекулы бывают однородными и разнородными. Однородные молекулы состоят из одинаковых атомов, а разнородные — из самых различных. Вещество, состоящее из однородных молекул, простое, его нельзя разложить на какие-либо другие вещества. Если же в состав вещества входят молекулы, построенные из разных атомов, то такие вещества называются сложными. Вода, например, сложное вещество: она состоит из кислорода и водорода, которые уже нельзя разложить на другие вещества.
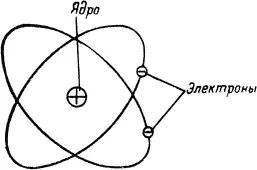
Сами атомы имеют сложное строение и состоят из электрически заряженных частиц. В центре атома находится положительно заряженное ядро, вокруг которого вращаются отрицательно заряженные частицы — электроны (рис. 1). При этом положительный заряд ядра уравновешен отрицательным зарядом электронов, и в своем обычном состоянии атом электрически нейтрален.
Если же изменить число электронов в атоме, то он выйдет из состояния равновесия. Если, например, удалить один или несколько электронов, то положительный заряд атома станет больше отрицательного и весь атом в целом окажется заряженным положительно. Такой атом называется положительным ионом. Или наоборот, если добавить один или несколько электронов, то атом приобретет отрицательный заряд и превратится в отрицательный ион.
Как располагаются атомы в веществе? Расположены ли они в определенном порядке или беспорядочно, хаотично? Ответить на этот вопрос было трудно. Ведь атомы и молекулы настолько малы, что их невозможно увидеть даже в самый мощный микроскоп. Но ученые обошлись и без этого. Им помогли рентгеновские лучи, которые показали, как расположены атомы в разных веществах.
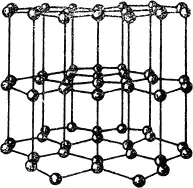
В кристаллических веществах частицы расположены геометрически правильно, по строгим законам. Если бы мы могли уменьшить свой рост до величины атома и проникнуть внутрь кристалла, то увидели бы, что вокруг нас во все стороны, не только вправо и влево, вперед и назад, но и вверх и вниз тянутся ровные бесконечные ряды атомов. Эти правильные ряды атомов в пространстве называются пространственными решетками , так как они действительно напоминают решетки (рис. 2).
С помощью рентгеновских лучей люди узнали, что у разных кристаллических веществ пространственные решетки разные. Каждое кристаллическое вещество можно отличить от другого кристаллического вещества по его пространственной решетке. В одних кристаллах очень простые решетки, в других — сложные.
Теперь мы можем сказать, что кристаллы — это тела, в которых атомы (молекулы, ионы) расположены в пространственных решетках строгой геометрической формы.
Рентгеновские лучи обнаружили кристаллическое строение не только в известных до того времени кристаллах, но и во многих других телах. Даже сажа, человеческий волос, шерсть, шелк и т. п. оказались построенными из кристаллов.
Но во всех ли веществах атомы расположены геометрически правильно? Конечно, нет. Существуют и такие твердые тела, в которых атомы расположены в беспорядке, как в газе или в жидкостях. Подобные тела называются аморфными, что означает в переводе с греческого «бесформенный». К такой группе тел относятся стекло, смола, столярный клей.
Однако и в аморфных телах атомы с течением времени могут в одном месте или сразу в нескольких местах собраться в правильную решетку. Тогда в этих местах появляются микроскопически маленькие кристаллики. Постепенно они вырастают и заполняют всю массу тела: аморфное тело закристаллизовалось. Так можно наблюдать помутнение старого стекла. Оно становится мутным, потому что в нем образуется множество мелких непрозрачных кристаллов.
Кристаллические тела бывают двух видов. Кристаллы, имеющие природную форму многогранников — кубов, параллелепипедов, призм, пирамид, называются монокристаллами или просто кристаллами. Тела, не имеющие многогранной формы, а состоящие из множества мелких, сросшихся между собой кристалликов, называются поликристаллами.
Кристаллы различных веществ отличаются друг от друга по форме (рис. 3). Кристаллы кварца имеют форму шестигранных призм, алмаза — восьмигранника, а граната — двенадцатигранника. Столбики берилла никогда не спутаете с пластинками слюды. Самая простая форма у кристаллов поваренной соли — форма куба.
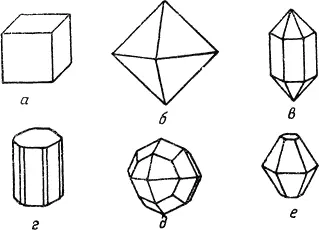
Но в природе редко встречаются кристаллы в виде правильных многогранников, чаще они неправильной формы. Это объясняется тем, что от действия воды, ветра, морозов кристаллы растрескиваются; в твердых породах кристаллы мешают друг другу расти; различные растворы разъедают кристаллы. Но все-таки свойства кристаллов остаются прежними. А что самое замечательное — остаются постоянными углы между одними и теми же гранями кристалла. Это свойство кристаллов называется законом постоянства углов, который объясняется внутренним строением кристаллов, т. е. тем, что частицы вещества расположены в геометрически правильной пространственной решетке. От ее формы и зависит форма кристалла. Чтобы убедиться в этом, рассмотрим ячейку пространственной решетки кристалла поваренной соли (рис. 4). Этот кристалл состоит измолекул, каждая из которых содержит положительный ион натрия и отрицательный ион хлора. Поскольку разноименно заряженные тела притягиваются друг к другу, а одноименно заряженные отталкиваются, молекулы поваренной соли группируются так, чтобы расстояния между одноименными ионами были как можно большими, а между разноименными — как можно меньшими.
Читать дальшеИнтервал:
Закладка:










