Аркадий Курамшин - Элементы: замечательный сон профессора Менделеева
- Название:Элементы: замечательный сон профессора Менделеева
- Автор:
- Жанр:
- Издательство:АСТ
- Год:2019
- ISBN:978-5-17-113353-5
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Аркадий Курамшин - Элементы: замечательный сон профессора Менделеева краткое содержание
Истории открытия, появления названия, самые интересные свойства и самые неожиданные области применения ста восемнадцати кирпичиков мироздания — от водорода, ключевого элемента нашей Вселенной, до сверхтяжёлых элементов, полученных в количестве нескольких атомов.
И тот, кто уже давно знает и любит химию, и тот, кто ещё только хочет сделать первые шаги в ней, найдут в книге что-то интересное и полезное для себя.
Элементы: замечательный сон профессора Менделеева - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
11. Натрий
Когда я был студентом, у нас была доставшаяся от предшественников традиция — в майские праздники нагружаться рюкзаками, палатками и спальниками, садится в поезд Казань-Йошкар-Ола и отправляться на 100 километров от Казани праздновать День Химика у марийской реки Юшута в месте, известном как «Большая химическая поляна».
Однажды, на рубеже восьмидесятых и девяностых годов прошлого века, когда старые запреты уходили в прошлое, а новые ещё не появлялись, к поляне, где уже разбили свой лагерь студенты, аспиранты и молодые преподаватели химфака Казанского университета, в сумерки пришвартовалось несколько байдарок, и высадившиеся из них в стиле викингов из современных сериалов бывалые туристы (тм) заявили, что это поляна их, и нам, туристам-салагам, стоит сняться с бивака и найти себе новое место. Нас было больше раза в три, уступать поляну мы не хотели, и в результате переговоров стороны решили, что «места всем хватит», и бывалые туристы уже начали разгружать свои суда. Именно тут у берега оказался наш профорг, который в момент переговоров ходил за валежником, и с криком: «Ну что, начинаем праздновать», — бросил что-то в воду. Сумерки марийской лесной реки озарились вспышками, вниз по течению поплыли ярко-жёлтые огоньки, которые не тушила вода, и в свете этих огней байдарки с туристами довольно резво поплыли вверх по течению — трюк, для исполнения которого на быстрых реках марийской тайги требуется хорошая физическая подготовка вкупе с резким выбросом адреналина. Так бывалые туристы (тм) познакомились с реакцией между натрием и водой. Дело в том, что традиционным ритуалом Дней химика в те времена было стравливание в речной воде кусочков натрия, оставшихся в лабораториях химфака после очистки растворителей и синтезов. Студенты и аспиранты начинали готовиться к этому «фейерверку» с сентября месяца, и чем выше было пламя, тем более удавшимся считался очередной День химика. От той же традиции и пошла кричалка: « Не хотите быть калекой? Киньте дальше натрий в реку ».
Как это часто бывает в химии, металлический натрий опасен, если работать с ним без предосторожности, а его соединения есть на каждой кухне — ионы натрия являются важными для жизнедеятельности всех живых организмов. Высокая химическая активность натрия, в частности та самая его способность активно реагировать с водой и другими веществами приводит к тому, что в земной коре натрий встречается только в виде соединений и никогда — в свободном виде. Натрий достаточно распространён в Земной коре — он составляет 2.6 % от её массы. Наиболее распространёнными соединениями натрия в природе являются хлорид натрия (каменная или поваренная соль) и цеолиты.
Человечество давно применяет соединения натрия — во времена палеолита наши предки начали использовать каменную соль, не ставшую ещё поваренной (поваренное искусство еще не появилось), в качестве консерванта охотничьи трофеев. В Древнем Египте появляется первое письменное упоминание о производных натрия — появляется иероглиф, который читается как «натар» и обозначает смесь поваренной соли и кристаллической соды (десятиводного карбоната натрия Na 2CO 3×10H 2O). В Египте натар применялся как мыло, а также был обязательной частью составов для бальзамирования и мумификации — натар хорошо поглощает воду, а его щелочная среда позволяла истреблять бактерии. Нетрудно заметить, что международное латинское название натрия, равно как и современное его название в русском и ряде других языков восходит к древнеегипетскому термину. Английское название натрия — sodium , тоже имеет восточные корни, но уже арабские. В средневековой Европе карбонат натрия использовали для врачевания головной боли, это снадобье называлось «соданум», а этот термин, в свою очередь, происходил от арабского «суда» — головная боль. В нашем языке арабский корень остался в названиях различных форм карбонатов натрия — сод и даже натриевой щёлочи — каустической соды, хотя, конечно, в наши дни последнее название безнадёжно устарело. Именно при пропускании постоянного электрического тока через расплавленную каустическую соду сэр Хэмфри Дэви впервые выделил металлический натрий — расплавленной натриевой щёлочи (NaOH). Процесс разрушения веществ с помощью электрического тока получил название «электролиз», и Дэви с его помощью смог получить также и другие активные металлы — калий, кальций, магний и барий.
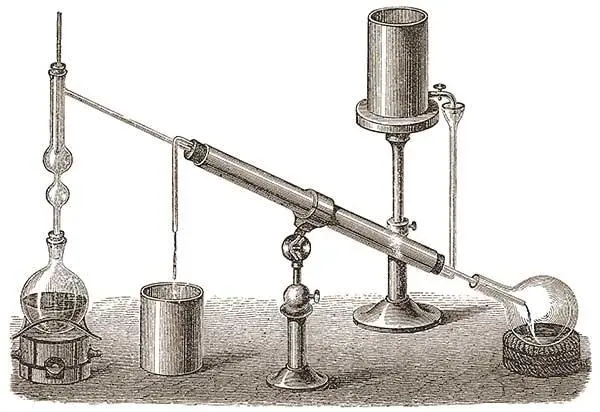
Металлический натрий, как и большинство металлов, серебристо-белый, его легко можно разрезать ножом или столь популярным в наших лабораториях скальпелем. Однако блестящим и серебристым натрий остается недолго — он быстро окисляется на воздухе и загорается при контакте с водой, ну а выделяющийся при этом водород, взрываясь, добавляет зрелищу красочности и звуковых эффектов. Способность натрия реагировать с водой применяется в лабораториях для очистки от воды некоторых органических растворителей, просто кипятя растворитель над кусочками натрия (главное, чтобы сам органический растворитель не реагировал с натрием, и воды в нём было не так уже много). Если мы очищаем от воды, например, бензол нам приходится нарезать кусочек натрия на тонкие-тонкие пластинки, а если толуол, такой необходимости нет. В чем причина? Металлический натрий «ловит» воду только поверхностью, а его шинковка увеличивает площадь поверхности, следовательно, увеличивая эффективность реакции. Однако, натрий очень легкоплавкий, его температура плавления равна +98 °C, то есть в растворителях с более высокой температурой кипения (у толуола температура кипения +110.6 °C) кусочки натрия все равно расплавятся и сольются в почти идеально шарообразную каплю натрия, рабочая поверхность которой постоянно будет очищаться. Как и другие свои родственники — щелочные металлы, натрий и его соединения можно определить по цвету пламени — при внесении соли натрия в бесцветное пламя газовой горелки пламя окрашивается в интенсивный жёлто-оранжевый цвет — в интернете можно найти немало красочных роликов-демонстраций на эту тему.
Натрий и его соединения применяются в столь разнообразных областях, что вряд ли можно перечислить их все даже в отдельной книге. Из наиболее интересных можно привести в пример применение натрия для охлаждения ядерных реакторов — он достаточно легко плавится, как и все металлы отличается хорошей теплопроводностью и, если вода закипает через два градуса после того, как натрий переходит в жидкое состояние, натрий начинает кипеть при температуре 883 °C, оставаясь жидким теплоносителем в широком интервале температур. Наш домашний реактор-лаборатория тоже не обходится без натрия — при готовке мы применяем пищевую соду или гидрокарбонат натрия. Очень часто мы используем это вещество для бездрожжевой выпечки — при 70 °C пищевая сода разлагается с выделением углекислого газа, который и заставляет бездрожжевое тесто подниматься.
Читать дальшеИнтервал:
Закладка:





![Петр Дружинин - Загадка «Таблицы Менделеева» [История публикации открытия Д.И.Менделеевым Периодического закона]](/books/1063991/petr-druzhinin-zagadka-tablicy-mendeleeva-istori.webp)
![Урсула Ле Гуин - Дома профессора [Два дома профессора]](/books/1071142/ursula-le-guin-doma-professora-dva-doma-professor.webp)



