Виктор Михайлов - Физические основы получения атомной энергии
- Название:Физические основы получения атомной энергии
- Автор:
- Жанр:
- Издательство:Военное Издательство Министерства обороны Союза ССР
- Год:1958
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Виктор Михайлов - Физические основы получения атомной энергии краткое содержание
2 0
/i/53/718753/Grinya2003.png
0
/i/53/718753/CoolReader.png
Физические основы получения атомной энергии - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Важнейшими открытиями, доказавшими сложность атома и тем самым подтвердившими взгляды Ф. Энгельса и подготовившими создание современной теории атома, явились открытия электрона(1897 г.) и радиоактивности(1896–1898 гг.).
Обобщая результаты науки начала XX столетия и критикуя старое метафизическое понимание атома как неизменной и неделимой частицы вещества, Ленин говорил, что диалектический материализм признает неисчерпаемость атома и утверждает, что «электрон так же неисчерпаем, как и атом, природа бесконечна…» [5] В. И. Ленин. Соч., т. 14, стр. 249.
Ленинское учение о неисчерпаемости материи во всех ее частях и проявлениях, полностью подтвержденное последующим развитием науки, имеет важное значение для прогресса современной атомной физики.
По современным представлениям, в формировании которых большую роль сыграли работы великого английского физика Э. Резерфорда, атом состоит из тяжелого положительно заряженного ядра, обладающего очень малыми размерами, и легких электронов, движущихся вокруг ядра в обширной области, получившей название электронной оболочки(рис. 2).
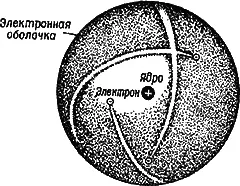
Диаметр ядра в несколько десятков тысяч раз меньше диаметра атома. Если представить себе атом увеличенным до размеров высотного здания Московского университета на Ленинских горах, то ядро представится тогда в виде вишни средней величины.
Электрон — мельчайшая частица вещества, обладающая зарядом отрицательного электричества. Вес (масса) электрона очень мал; он примерно в 1840 раз меньше веса легчайшего из всех атомов — атома водорода. Электрический заряд, меньший чем у электрона, никогда не наблюдался. Поэтому в атомной физике принято все заряды измерять в зарядах электрона.
Число электронов в электронной оболочке атома равно числу положительных зарядов в его ядре. Благодаря одинаковому числу положительных и отрицательных зарядов атом в целом нейтрален, то есть электрически не заряжен.
Положительный заряд ядер атомов различных химических элементов не одинаков: заряд ядра, а следовательно, и число обращающихся вокруг него электронов равны порядковому номеру элемента Z в периодической системе Менделеева. Так, например, атом водорода состоит из ядра, имеющего один заряд положительного электричества и движущегося вокруг него одного электрона. Соответственно этому водород стоит на первом месте в периодической системе. Атом гелия состоит из ядра, имеющего двойной положительный заряд, и движущихся вокруг него двух электронов. Гелий расположен в периодической системе на втором месте. В атоме кислорода имеется 8 положительных зарядов в ядре и 8 электронов в оболочке. Соответственно этому кислород занимает в системе Менделеева восьмое место.
Открытие того, что порядковый номер (положение) элемента в периодической системе, от которого зависят химические свойства элемента, равен как раз числу положительных зарядов в ядре данного атома, вскрыло глубокий смысл системы Менделеева. Нельзя не удивляться гениальной прозорливости великого русского химика, сумевшего за сорок лет до открытия самого существования атомных ядер правильно определить место каждого элемента в открытой им периодической системе.
Строя свою систему, Менделеев располагал элементы в порядке возрастания их атомных весов, так как атомный вес был в то время главным отличительным признаком разных элементов. Но, учитывая все другие свойства аргона, калия, кобальта, никеля, иода и теллура, Менделеев разместил эти элементы с нарушением постепенного возрастания их атомных весов. Так, например, элемент теллур (атомный вес 127,6) Менделеев поставил на 52 место, а иод (атомный вес 126,9) — на 53-е, хотя их следовало бы расположить в обратном порядке, если руководствоваться атомным весом. Многочисленные измерения электрического заряда ядер атомов аргона, калия, кобальта, никеля, иода, теллура и всех других элементов показали, что число «элементарных» зарядов в ядрах атомов элементов точно совпадает с тем порядковым номером, который им дал Менделеев в своей периодической системе.
Таким образом, место элементов в периодической системе объективно обусловлено положительным зарядом их атомных ядер. Тем самым было установлено, что число «элементарных» зарядов в ядре (число Менделеева Z) является самой главной и существенной характеристикой атома, полностью определяющей его химические свойства.
Между положительно заряженным ядром атома и его электронами, как и между всякими разноименно заряженными телами, действуют силы электрического притяжения, удерживающие электроны в обширной оболочке атома. Электроны обращаются в атоме на разных расстояниях от ядра, располагаясь несколькими слоями. В каждом слое может находиться лишь вполне определенное количество электронов. Первый слой, ближайший к ядру, получил название K -слоя; в нем может находиться не более двух электронов. Далее следует второй слой ( L -слой), имеющий не более 8 электронов, третий слой ( M -слой), содержащий не более 18 электронов, и т. д. Под действием сил притяжения со стороны ядра электроны стремятся расположиться в ближайших к ядру слоях. Поэтому при построении электронной оболочки атома сперва заполняется слой K , затем L, М и т. д. Если число электронов в атоме, равное, как мы знаем, Z , меньше того их количества, которое необходимо для заполнения слоев, то последний (верхний) слой остается незаполненным. Строение электронной оболочки некоторых атомов схематически дано на рис. 3. Каждый слой условно изображен окружностью, на которых точками показаны электроны.
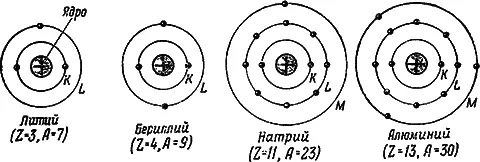
В каждой клетке таблицы Менделеева (см. рис. 1), помимо атомного номера и атомного веса, приведены колонки цифр, указывающих распределение электронов по слоям. Для алюминия, например, найдем следующие цифры (снизу вверх): 2, 8, 3, дающие число электронов соответственно в слоях K, L и М; для меди — 2, 8, 18, 1 и т. д.
Первоначально ученые считали, что электроны в атоме вращаются вокруг ядра совершенно так же, как планеты, в том числе и наша Земля, обращаются вокруг Солнца. Атом рассматривали как солнечную систему в миниатюре.
Однако развитие науки показало, что наряду с некоторым сходством между атомом и солнечной системой существует громадное качественное различие. Движение электронов в атоме значительно сложнее, и поэтому, строго говоря, уподоблять атом солнечной системе нельзя.
Читать дальшеИнтервал:
Закладка:










