Лев Ландау - Физика для всех. Молекулы
- Название:Физика для всех. Молекулы
- Автор:
- Жанр:
- Издательство:Наука
- Год:1984
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Лев Ландау - Физика для всех. Молекулы краткое содержание
Во второй из четырех книг 'Физики для всех' рассказано о строении вещества, о физических явлениях и процессах, которые происходят в реальных кристаллах и определяют их свойства. Читатель знакомится с различными фазовыми состояниями вещества, со структурой и свойствами жидких и твердых растворов, структурой кристаллов и молекул, с основными законами термодинамики.
Физика для всех. Молекулы - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Рис. 3.1
На рис. 3.1 построены векторы импульсов до и после удара, а также вектор приращения импульса Δ. Из подобия возникших при построении треугольников следует: 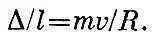 Вклад в силу со стороны одной молекулы примет вид
Вклад в силу со стороны одной молекулы примет вид
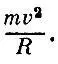
Так как длина хорды не вошла в формулу, то ясно, что молекулы, движущиеся по любой хорде, дают одинаковый вклад в силу. Конечно, изменение импульса при косом ударе будет меньше, но зато удары в этом случае будут чаще. Расчет показал, что оба эффекта в точности компенсируются.
Так как в сфере N молекул, то суммарная сила будет равна
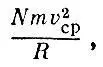
где v cp- средняя скорость молекул.
Давление ρ газа, равное силе, деленной на площадь сферы 4πR 2, будет равно
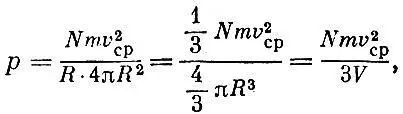
где V - объем сферы.
Таким образом,
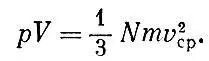
Это уравнение было впервые выведено Даниилом Бернулли в 1738 г.
Из уравнения состояния идеального газа следовало: ρV = const*T; из выведенного уравнения видим, что pV пропорционально v 2 cp. Значит,
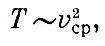
или
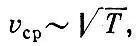
т. е. средняя скорость молекул идеального газа пропорциональна корню квадратному из абсолютной температуры.
Закон Авогадро
Пусть вещество представляет собой смесь различных молекул. Нет ли такой физической величины, характеризующей движение, которая была бы одинакова для всех этих молекул, например для водорода и кислорода, находящихся при одинаковой температуре?
Механика дает ответ на этот вопрос. Можно доказать, что одинаковыми у всех молекул будут средние кинетические энергии поступательного движения m v 2 ср/ 2.
Это означает, что при данной температуре средние квадраты скорости молекул обратно пропорциональны массе частиц:
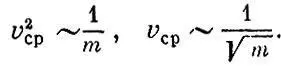
Вернемся теперь к уравнению 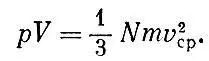 Так как при данной температуре величины m v 2 сpодинаковы для всех газов, то число молекул N, заключенных в данном объеме V при определенных давлении ρ и температуре Т, одинаково для всех газов. Этот замечательный закон был впервые сформулирован Авогадро.
Так как при данной температуре величины m v 2 сpодинаковы для всех газов, то число молекул N, заключенных в данном объеме V при определенных давлении ρ и температуре Т, одинаково для всех газов. Этот замечательный закон был впервые сформулирован Авогадро.
Сколько же молекул приходится на 1 см 3? Оказывается, в 1 см 3при 0°С и 760 мм рт. ст. находится 2,7*10 19молекул. Это огромное число. Чтобы вы почувствовали, сколь оно велико, приведем такой пример. Положим, что газ удаляется из маленького сосудика объемом 1 см 3с такой скоростью, что в каждую секунду уходит миллион молекул. Нетрудно подсчитать, что сосуд полиостью освободится от газа через миллион лет!
Закон Авогадро указывает, что при определенных давлении и температуре отношение числа молекул к объему, в котором они заключены, N/ V, есть величина, одинаковая для всех газов.
Так как плотность газа ρ = Nm/ V, то отношение плотностей газов равно отношению их молекулярных масс:
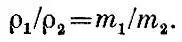
Относительные массы молекул могут быть поэтому установлены простым взвешиванием газообразных веществ. Такие измерения сыграли в свое время большую роль в развитии химии. Из закона Авогадро следует также, что для моля любого вещества, находящегося в состоянии идеального газа, ρV = k N AT, где к - универсальная постоянная (она носит имя замечательного немецкого физика Людвига Больцмана), равная 1,38.10 -16эрг/ К. Произведение R= k N Aназывают универсальной газовой постоянной.
Закон идеального газа записывают часто как
ρV = μRT,
где μ - количество вещества, выраженное в молях. Это уравнение часто используется на практике.
Скорости молекул
Теория указывает, что при одной температуре средние кинетические энергии молекул m v 2 ср/2 одинаковы. При нашем определении температуры эта средняя кинетическая энергия поступательного движения молекул газа пропорциональна абсолютной температуре. Комбинируя уравнение идеального газа и уравнение Бернулли, найдем
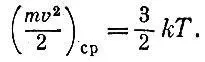
Измерение температуры термометром, заполненным идеальным газом, придает этой мере простой смысл: температура пропорциональна среднему значению энергии поступательного движения молекул. Поскольку мы живем в трехмерном пространстве, про точку, движущуюся как угодно, можно сказать: она имеет три степени свободы. Значит, на одну степень свободы движущейся частицы приходится кТ/ 2энергии.
Определим среднюю скорость молекул кислорода при комнатной температуре, которую мы для круглого счета примем в 27°С=300 К. Масса одной молекулы кислорода равна 32/ (6*10 23 ). Простое вычисление даст м ср= 4,8*10 4см/с, т.е. около 500 м/с. Существенно быстрее движутся молекулы водорода. Их массы в 16 раз меньше и скорости в 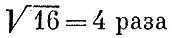 больше, т. е. при комнатной температуре составляют около 2 км/с. Прикинем, с какой тепловой скоростью движется маленькая? видимая в микроскоп частичка. Обычный микроскоп позволяет увидеть пылинку диаметром в 1 мкм (10 -4см). Масса такой частицы при плотности,; близкой к единице, будет что-нибудь около 5*10 -13г. Для ее скорости получим около 0,5 см/с. Неудивительно, что такое движение вполне заметно.
больше, т. е. при комнатной температуре составляют около 2 км/с. Прикинем, с какой тепловой скоростью движется маленькая? видимая в микроскоп частичка. Обычный микроскоп позволяет увидеть пылинку диаметром в 1 мкм (10 -4см). Масса такой частицы при плотности,; близкой к единице, будет что-нибудь около 5*10 -13г. Для ее скорости получим около 0,5 см/с. Неудивительно, что такое движение вполне заметно.
Скорость броуновского движения горошины с массой в 0,1 г будет уже всего только 10 -6см/с. Немудрено, что мы не видим броуновского движения таких частиц.
Мы говорим о средних скоростях молекулы. Но ведь не все молекулы движутся с одинаковыми скоростями, какая-то доля молекул движется быстрее, а какая-то медленнее. Все это, оказывается можно рассчитать. Приведем только результаты.
При температуре около 15°С, например, средняя скорость молекул азота равна 500 м/с, со скоростями от 300 до 700 м/с движется 59% молекул. С малыми скоростями - от 0 до 100 м/с - движется всего лишь 0,6% молекул. Быстрых молекул со скоростями свыше 1000 м/с в газе всего лишь 5,4% (см. рис. 3.2).
Читать дальшеИнтервал:
Закладка:








