Владимир Виноградов - Стресс и патология
- Название:Стресс и патология
- Автор:
- Жанр:
- Издательство:Array Литагент «Белорусская наука»
- Год:2007
- Город:Минск
- ISBN:978-985-08-0829-5
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Владимир Виноградов - Стресс и патология краткое содержание
Книга рассчитана на медиков и широкий круг специалистов, интересующихся проблемой коррекции кардио– и иммунопатологии стресса.
Стресс и патология - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Супероксидрадикал – это важнейший индуктор перекисного окисления липидов, резкая активация которого, а также фосфолипаз, плюс детергентное действие жирных кислот лизофосфатидов (липидная триада) являются основным патогенетическим механизмом повреждения кардиомиоцитов при стрессе [98].
Продукты взаимодействия О 2 -с белками, лейкотриены и другие обладают свойствами лейкотаксинов, стимулирующих миграцию лейкоцитов в зону ишемии. Уже через 1 ч после окклюзии коронарной артерии наблюдается адгезия нейтрофилов к эндотелию сосудов ишемизированной зоны. С началом реперфузии лейкоциты легко проникают в ткань миокарда, во множестве скапливаясь вокруг поврежденных клеток [277]. В активированных лейкоцитах резко повышается количество молекул индуцибельной синтетазы окиси азота за счет экспрессии соответствующего гена и начинается обвальный синтез больших (наномолярных) концентраций окиси азота из аргинина [274]. Поскольку активированные полиморфноядерные лейкоциты и макрофаги сами продуцируют значительные количества супероксиданиона, NO и О 2 -реагируют между собой с образованием еще более агрессивных радикалов ОNOO -и OH -, являющихся сильнейшими окислителями, которые определяют их валовый цитотоксический эффект [222].
Вновь образованный пероксинитрит (ОNOO -) подвергается протонированию (ONOOH) и через свои кислотные формы творит много вреда в клетке-мишени, нитрируя или окисляя ее биологически важные структуры. Единственной защитой клеток от агрессии является наличие в них достаточного количества быстрореагирующих SH-групп, которые способны нейтрализовать пероксинитрит через образование метаболически инертных S-нитрозотиолов. В случае дефицита тиолов пероксинитрит наносит удар и разрушает ткани, как это происходит при инфаркте миокарда, отеке легких или инсульте мозга [49].
Инфильтрация ишемизированного миокарда лейкоцитами и сопутствующая этому процессу лейкоцитарная деструкция поврежденных ишемией клеток миокарда, опосредованная супероксиданионом и пероксинитритом, способствует интенсификации ПОЛ. Важная роль свободнорадикальных процессов в развитии стрессорных кардиопатий уже сама по себе предопределяет наличие мощного кардиопротекторного потенциала у природных антиоксидантов [46].
Известно, что кардиотоксический эффект катехоламинов сопряжен с развитием окислительного стресса, когда чрезмерная генерация активных форм кислорода превышает физиологические возможности систем антиоксидантной защиты. Образование супероксиданиона имеет место при распаде (аутоокислении) самих катехоламинов в сердце, при активации ими цАМФ-зависимого свободнорадикального окисления в митохондриях или Са 2+-зависимой трансформации ксантиндегидрогеназы в ксантиноксидазу [193].
Исходя из идеологии окислительного стресса, т. е. отталкиваясь от очевидной необходимости нейтрализации активных форм кислорода, применение витамина С для коррекции и профилактики адренергических повреждений миокарда обосновано патогенетически. Но в связи с NO можно предполагать и другие возможности реализации кардиотропной активности аскорбиновой кислоты, обусловленные тем, что окись азота выступает в качестве активного компонента эндотелиального фактора релаксации сосудов, образующегося в эндотелиальных клетках сосудов и вызывающего их расслабление [196, 274].
В системе кровообращения непрерывное образование физиологических (пикомолярных) концентраций NO конституитивной нитрогеноксидсинтетазой в сосудистом эндотелии поддерживает тканевую перфузию на соответствующем уровне и регулирует артериальное давление крови [175]. NO легко диффундирует в соседние гладкомышечные клетки, где связывается с железопорфиринами, т. е. с простетической группой (гем или железосерные кластеры) соответствующих ферментов, вызывая их активацию или ингибирование [341]. При этом акцепция NO гемовой частью гуанилатциклазы ведет к стимуляции синтеза цГМФ – медиатора вазодилятации [230].
Источником NO в организме могут быть и нитратсодержащие лекарства. Органические нитраты (нитроглицерин, изосорбиддинитрат и его однонитратный метаболит – изосорбид-5-мононитрат) вызывают диастолу гладких мышц [336]. В малых дозах, главным образом, они являются фактором, расширяющим вены, а в больших —
расширяют как вены, так и артерии [93]. Механизм действия нитратов, инициирующий релаксацию гладких мышц, известен и связан с выделением окиси азота. Так, нитроглицерин и другие органические нитраты превращаются в неорганические нитраты и окись азота под влиянием восстановителей, например сульфгидрильных групп цистеина [215]. Среди витаминов сильным восстановителем является аскорбиновая кислота, поэтому было интересно использовать ее для потенцирования антиангинального действия NO-доноров.
2. Кардиопротекторные эффекты тиамина в эксперименте
2.1. Стрессорные кардиопатии
Стрессорная альтерация миокарда – причина гибели животных при иммобилизационном стрессе по Г. Селье.При моделировании иммобилизационного стресса одни авторы относят фатальный исход экспериментов за счет гиперпродукции стрессреализующих гормонов (катехоламины, кортикостероиды) [141], другие – стресслимитирующих (инсулин) [121].
В наших опытах отмечалась гибель 56 % крыс к 72 ч иммобилизации [27, 30], что не расходится с данными литературы. Практически в 100 % случаев наиболее вероятной причиной гибели животных при иммобилизационном стрессе является постепенно нарастающая стрессорная альтерация сердечной мышцы, приводящая к ее функциональной несостоятельности и развитию недостаточности кровообращения. Об этом свидетельствуют морфологические, а также биохимические признаки (нарушение окислительного фосфорилирования, активация ПОЛ, повышение текучести митохондриальных и микросомальных мембран кардиомиоцитов).
Тиамин, оптимизируя стресс-реакцию организма на действие неспецифических раздражителей, предотвращает гибель животных при иммобилизационном стрессе.
Из рис. I-1 видно, что у контрольных животных в стадии тревоги иммобилизационного стресса (1—12 ч) наблюдается резкий подъем содержания 11-ОКС в крови, который сохраняется на высоком уровне в течение 24 ч нервно-мышечного раздражения с последующим снижением в конце периода резистентности. В фазе истощения (48–72 ч) наблюдается новая волна стероидогенеза.
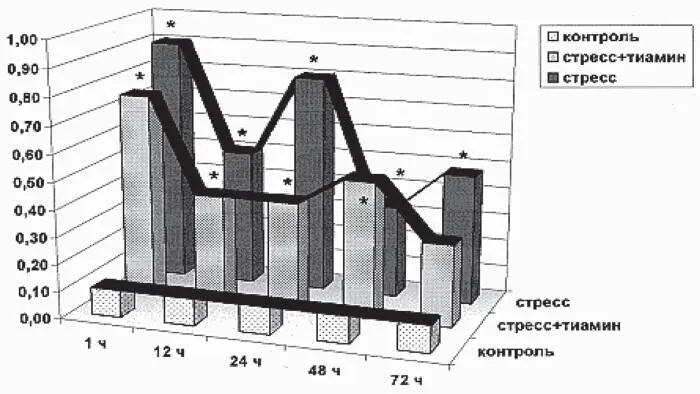
Рис. I-1. Стероидогенная реакция надпочечников в динамике хронического стресса до (черные столбики) и после (серые столбики) введения тиамина. Контроль – белые столбики. По оси абсцисс – срок наблюдения; по оси ординат – содержание 11-ОКС в крови, мкМ/л.
Читать дальшеИнтервал:
Закладка: