Ольгерт Ольгин - Чудеса на выбор, или химические опыты для новичков
- Название:Чудеса на выбор, или химические опыты для новичков
- Автор:
- Жанр:
- Издательство:Детская литература
- Год:1986
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ольгерт Ольгин - Чудеса на выбор, или химические опыты для новичков краткое содержание
Чудеса на выбор, или химические опыты для новичков - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Между прочим, чуть ли не в каждом магазине, где продают нужные в домашнем хозяйстве вещи, есть отдел химических товаров. Страшно и подумать, как наши далекие предки, не знавшие ни мыла, ни стиральных порошков, отмывали свою грязную одежду в речной воде…
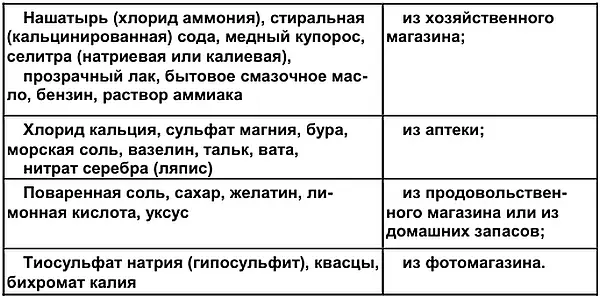
Нет, я не собираюсь учить тебя, как правильно стирать. Но коль скоро и стирка, и многое другое имеют прямое отношение к химическим чудесам, давай поставим опыты, которые помогут тебе понять, что же при этом происходит. И может быть, набравшись новых знаний, ты кое-что будешь делать лучше и быстрее…
Маленький кусочек хозяйственного мыла положи в пузырек с теплой водой, закрой пузырек пальцем и взболтай хорошенько. К мыльному раствору добавь несколько капель раствора фенолфталеина. Малиновый цвет, как ты помнишь, свидетельствует о том, что перед нами основание. Или, как часто говорят химики, у этого раствора щелочная реакция (щелочи — самые распространенные и очень активные основания; мы с ними напрямую стараемся дела не иметь, потому что они очень едкие).
Давно было известно, что мыло, растворяясь, взаимодействует с водой и образует пусть слабую, но щелочь. И думали, что именно поэтому мыло и снимает грязь с рук и белья. И стиральная сода тоже дает щелочной раствор, и она тоже неплохо отстирывает белье, особенно если прокипятить как следует…
Но все оказалось не так. Более того, все оказалось наоборот. Сода стирает потому, что она, соединяясь с загрязнениями (а это чаще всего бывает какой-нибудь жир), образует вещества наподобие мыла.
Так давай и мы с тобой получим мыло из соды, только не в тазу во время стирки, а заранее, в пробирке или в стакане.
Нагрей в кастрюльке немного воды и сыпь в нее порциями стиральную (кальцинированную) соду, постоянно размешивая. Когда сода перестанет растворяться, в твоем распоряжении будет крепкий, как говорят, концентрированный ее раствор. В горячем виде осторожно перелей его в небольшую, но обязательно тонкостенную склянку, лучше всего в пробирку. Пипеткой, каплю за каплей, добавляй растительное масло, пока оно не перестанет растворяться. Масло можно заменить растопленным воском, но тогда, понятно, пипеткой его уже не накапаешь.
В склянке образовалось мыло, но пока оно находится там в жидком виде. На мыловаренном заводе такое мыло высаливают, то есть добавляют в раствор соль (самую обычную, поваренную). Поступи точно так же. Одна-две щепотки соли — и твердое мыло всплывет на поверхность. Аккуратно сними его и испытай — как оно мылится, образует ли пену, что за реакция у него с фенолфталеином.
К сожалению, из тех веществ, что есть в нашем распоряжении, хорошего мыла, которым можно стирать и умываться, не сделать. Вот если только из стеарина…
Возьми несколько обломков от стеариновой свечки (бывают еще парафиновые свечки, они для этого опыта не годятся). Нагрей обломки в тонком стакане, поставленном в очень горячую воду. Когда стеарин расплавится, добавь крепкий раствор стиральной соды. Тут же появится белая масса. Это и есть мыло. Дай ему постоять еще несколько минут в горячей воде, а затем осторожно, чтобы не обжечься (надень рукавицы), вылей в спичечный коробок. Когда масса застынет, у тебя окажется кусочек мыла, которое можно использовать для стирки.
А можно поставить и опыт «наоборот»: из куска мыла приготовить свечу. Настругай ножом хозяйственного мыла, сложи стружки в хорошо вымытую консервную банку, влей воды и нагрей, лучше на водяной бане, не забывая все время перемешивать деревянной палочкой. Как только мыло растворится, добавь к нему уксус — и на поверхность всплывет белая масса. Это стеарин. Когда банка остынет, он соберется на поверхности. Собери его ложкой, переложи в чистую посуду, промой водой и заверни в салфетку или в фильтровальную бумагу, чтобы стеарин высох. Теперь приготовь из него свечку.
Возьми толстую нитку (например, от фитиля для керосинки) и опусти ее в подогретый и расплавленный стеарин. Вынь фитиль, дай стеарину затвердеть и опять опусти в расплавленную массу. Поступай так до тех пор, пока на фитиле не нарастет свечка. А можешь для простоты обмазать один раз фитиль только что приготовленной, еще теплой массой — и свеча из мыла готова.
Но вернемся к мылу. Отчего оно все-таки моет? Хитрость в том, что у молекулы мыла «голова» и «хвост» очень не похожи друг на друга. Один конец молекулы (пусть это будет «голова») легко соединяется с жирами и другими подобными веществами. А другой конец (то есть «хвост») питает такую же любовь к воде. Наскочив на частицу грязи, молекулы мыла прикрепляются к ней «головами», образуя нечто вроде ежиных иголок. А вода, ухватившись за «хвосты», растаскивает частицы грязи в разные стороны и уносит их с собой. Так грязное становится чистым.
Увы, молекулы глазом не разглядеть, так что придется тебе поверить мне на слово. Но кое-что мы все же увидим.
Например, вот что. Три одинаковых пузырька наполовину заполни водой, но разной: первый пузырек — дождевой или из растопленного снега (можно соскрести иней с морозильника), второй — обычной, водопроводной водой, третий — минеральной, из бутылки. Если минеральной воды не окажется, то в обычную воду добавь столовую ложку раствора хлорида кальция или половину чайной ложки горькой соли — смотря по тому, что у тебя осталось в запасе от старых опытов. Отдельно, в тонкостенном стакане, раствори немного мыла в горячей воде. Удобнее взять мыльные хлопья (примерно столовую ложку без верха на полстакана воды); если нет готовых хлопьев, настругай ножом с куска хозяйственного мыла. Размешай как следует, чтобы раствор был прозрачным.
Теперь сам опыт. По каплям добавляй в первый пузырек мыльный раствор. После каждой капли встряхивай как следует и следи, не появилась ли пена. Не забудь считать капли. Как только пена станет пышной и устойчивой, прекращай капать. Запиши число капель и переходи к следующему пузырьку. Ты увидишь, что водопроводной воде для образования пены требуется больше мыла, чем дождевой, а минеральной — еще больше.
Происходит это вот отчего. В дождевой (или снеговой) воде почти нет растворенных примесей, а в водопроводной и минеральной они есть, причем в минеральной их особенно много: они-то и придают ей лечебные свойства. Интересующие нас примеси — это соли, но не натрия, как поваренная соль, а кальция и магния. Воду с такими солями называют жесткой , без них — мягкой.
Считая капли одного и того же мыльного раствора, потраченные на получение пены, ты можешь сравнить жесткость воды из разных источников: например, из колодца, пруда, речки. Сравни также кипяченую воду с сырой: при кипячении жесткость воды уменьшается, но, к сожалению, не исчезает.
Читать дальшеИнтервал:
Закладка:









