БСЭ БСЭ - Большая Советская Энциклопедия (КВ)
- Название:Большая Советская Энциклопедия (КВ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (КВ) краткое содержание
Большая Советская Энциклопедия (КВ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
В 1913 Н. Бор применил идею квантования энергии к теории строения атома, планетарная модель которого следовала из результатов опытов Э. Резерфорда (1911). Согласно этой модели, в центре атома находится положительно заряженное ядро, в котором сосредоточена почти вся масса атома; вокруг ядра вращаются по орбитам отрицательно заряженные электроны. Рассмотрение такого движения на основе классических представлений приводило к парадоксальному результату — невозможности стабильного существования атомов: согласно классической электродинамике, электрон не может устойчиво двигаться по орбите, поскольку вращающийся электрический заряд должен излучать электромагнитные волны и, следовательно, терять энергию; радиус его орбиты должен уменьшаться, и за время порядка 10 –8 сек электрон должен упасть на ядро. Это означало, что законы классической физики неприменимы к движению электронов в атоме, т.к. атомы существуют и чрезвычайно устойчивы.
Для объяснения устойчивости атомов Бор предположил, что из всех орбит, допускаемых Ньютоновой механикой для движения электрона в электрическом поле атомного ядра, реально осуществляются лишь те, которые удовлетворяют определённым условиям квантования. Т. е. в атоме существуют (как в осцилляторе) дискретные уровни энергии. Эти уровни подчиняются определённой закономерности, выведенной Бором на основе комбинации законов Ньютоновой механики с условиями квантования, требующими, чтобы величина действия для классической орбиты была целым кратным постоянной Планка 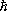 . Бор постулировал, что, находясь на определённом уровне энергии (т. е. совершая допускаемое условиями квантования орбитальное движение), электрон не излучает световых волн. Излучение происходит лишь при переходе электрона с одной орбиты на другую, т. е. с одного уровня энергии E i, на другой с меньшей энергией E k, при этом рождается квант света с энергией, равной разности энергий уровней, между которыми осуществляется переход:
. Бор постулировал, что, находясь на определённом уровне энергии (т. е. совершая допускаемое условиями квантования орбитальное движение), электрон не излучает световых волн. Излучение происходит лишь при переходе электрона с одной орбиты на другую, т. е. с одного уровня энергии E i, на другой с меньшей энергией E k, при этом рождается квант света с энергией, равной разности энергий уровней, между которыми осуществляется переход:
h n = E i- E k. (2)
Так возникает линейчатый спектр — основная особенность атомных спектров, Бор получил правильную формулу для частот спектральных линий атома водорода (и водородоподобных атомов), охватывающую совокупность открытых ранее эмпирических формул (см. Спектральные серии ).
Существование уровней энергии в атомах было непосредственно подтверждено Франка — Герца опытами (1913—14). Было установлено, что электроны, бомбардирующие газ, теряют при столкновении с атомами только определённые порции энергии, равные разности энергетических уровней атома.
Т. о., Н. Бор, используя квантовую постоянную h , отражающую дуализм света, показал, что эта величина определяет также и движение электронов в атоме (и что законы этого движения существенно отличаются от законов классической механики). Этот факт позднее был объяснён на основе универсальности корпускулярно-волнового дуализма, содержащегося в гипотезе де Бройля.
Успех теории Бора, как и предыдущие успехи квантовой теории, был достигнут за счёт нарушения логической цельности теории: с одной стороны, использовалась Ньютонова механика, с другой — привлекались чуждые ей искусственные правила квантования, к тому же противоречащие классической электродинамике. Кроме того, теория Бора оказалась не в состоянии объяснить движение электронов в сложных атомах (даже в атоме гелия), возникновение молекулярной связи и т.д. «Полуклассическая» теория Бора не могла также ответить на вопрос, как движется электрон при переходе с одного уровня энергии на другой. Дальнейшая напряжённая разработка вопросов теории атома привела к убеждению, что, сохраняя классическую картину движения электрона по орбите, логически стройную теорию построить невозможно. Осознание того факта, что движение электронов в атоме не описывается в терминах (понятиях) классической механики (как движение по определённой траектории), привело к мысли, что вопрос о движении электрона между уровнями несовместим с характером законов, определяющих поведение электронов в атоме, и что необходима новая теория, в которую входили бы только величины, относящиеся к начальному и конечному стационарным состояниям атома. В 1925 В. Гейзенбергу удалось построить такую формальную схему, в которой вместо координат и скоростей электрона фигурировали некие абстрактные алгебраические величины — матрицы ; связь матриц с наблюдаемыми величинами (энергетическими уровнями и интенсивностями квантовых переходов) давалась простыми непротиворечивыми правилами. Работа Гейзенберга была развита М. Борном и П. Иорданом. Так возникла матричная механика. Вскоре после появления уравнения Шрёдингера была показана математическая эквивалентность волновой (основанной на уравнении Шрёдингера) и матричной механики. В 1926 М. Борн дал вероятностную интерпретацию волн де Бройля (см. ниже).
Большую роль в создании К. м. сыграли работы Дирака, относящиеся к этому же времени. Окончательное формирование К. м. как последовательной физической теории с ясными основами и стройным математическим аппаратом произошло после работы Гейзенберга (1927), в которой было сформулировано неопределённостей соотношение— важнейшее соотношение, освещающее физический смысл уравнений К. м., её связь с классической механикой и другие как принципиальные вопросы, так и качественные результаты К. м. Эта работа была продолжена и обобщена в трудах Бора и Гейзенберга.
Детальный анализ спектров атомов привёл к представлению (введённому впервые Дж. Ю. Уленбеком и С. Гаудсмитом и развитому В. Паули ) о том, что электрону, кроме заряда и массы, должна быть приписана ещё одна внутренняя характеристика ( квантовое число ) — спин . Важную роль сыграл открытый В. Паули (1925) так называемый принцип запрета ( Паули принцип , см. ниже), имеющий фундаментальное значение в теории атома, молекулы , ядра, твёрдого тела.
В течение короткого времени К. м. была с успехом применена к широкому кругу явлений. Были созданы теории атомных спектров, строения молекул, химической связи, периодической системы Д. И. Менделеева , металлической проводимости и ферромагнетизма. Эти и многие др. явления стали (по крайней мере качественно) понятными. Дальнейшее принципиальное развитие квантовой теории связано главным образом с релятивистской К. м. Нерелятивистская К. м. развивалась в основном в направлении охвата разнообразных конкретных задач физики атомов, молекул, твёрдых тел (металлов, полупроводников), плазмы и т.д., а также совершенствования математического аппарата и разработки количественных методов решения различных задач.
Читать дальшеИнтервал:
Закладка:
