БСЭ БСЭ - Большая Советская Энциклопедия (СУ)
- Название:Большая Советская Энциклопедия (СУ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (СУ) краткое содержание
Большая Советская Энциклопедия (СУ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
ArN 2CI + SbCl 3® ArN 2CI · SbCl 3 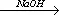 ArSb(ONa) 2O,
ArSb(ONa) 2O,
Несмеянова реакция, а также взаимодействие Li- или Mg -органических соединений с галогенидами Sb или галогенсодержащими С. с., например:
SbCl з+ 3RMgX ® R 2Sb + 3MgXCI
(C 6H 5) 3SbCl2 + 2C 6H 5Li ® (C 6H 5) 5Sb + 2LiCI.
С. с. алифатического ряда легко окисляются, ароматические С. с. более стабильны. Соли м- хлор- n- ацетиламинофенилстибиновой кислоты применяют для лечения лейшманиозов. См. также Металлоорганические соединения.
Б. Л. Дяткин.
Сурьмы галогениды
Сурьмы' галогени'ды,соединения сурьмы с галогенами типа SbX 3(где X — F, Сl, Вг, I) и SbX 5(где Х — только F и Сl). SbF 5и SbCl 5— жидкости; образуются при взаимодействии SbCl 3и SbF 3с хлором и фтором соответственно; промышленного применения SbF 5не имеет, а SbCl 5используется в органическом синтезе. SbCl 3— бесцветные гигроскопичные кристаллы; растворяются в соляной и серной кислотах при нагревании; получают хлорированием Sb или Sb 2S 3, а также растворением Sb или её окислов в соляной кислоте; применяют для получения чистой трёхокиси, а также в медицине и в текстильной промышленности. SbF 3— бесцветные кристаллы, хорошо растворимые в воде и в плавиковой кислоте; получают растворением SbCl 3или Sb 2(SO 4) 3в плавиковой кислоте; применяют в составе электролита при рафинировании сурьмы, а также в текстильной промышленности. SbBr 3— бесцветные кристаллы; практического применения не имеют. SbI 3встречается в трёх модификациях, наиболее распространена тригональная; получают растиранием сурьмы с йодом.
Лит. см. при ст. Сурьма.
О. Е. Крейн.
Сурьмы окислы
Сурьмы' о'кислы,соединения сурьмы с кислородом — Sb 2O 3, Sb 2O 4, Sb2O 5. Трёхокись — бесцветные, легковозгоняющиеся кристаллы; получают при дистилляционном обжиге сурьмяных руд; применяется в текстильной промышленности и в производстве красок. Пятиокись Sb 2O 5— светло-жёлтые кристаллы; получают при прокаливании xSb 2O 5× уН 2О; применяется в фармацевтической промышленности, в производстве стекла, керамики, красок, лаков, в текстильной промышленности.
Сурьмы сульфиды
Сурьмы' сульфи'ды,соединения сурьмы с серой — Sb 2S 3и Sb 2S 5. Сурьма трёхсернистая Sb 2S 3известна в аморфной и кристаллической модификациях; наиболее устойчива кристаллической, встречающаяся в природе в виде минерала антимонита; в промышленности получают зейгерованием из богатых сурьмяных руд ; применяется для получения сурьмы и её соединений и в пиротехнике. Сурьма пятисернистая Sb 2S 5— аморфный порошок оранжево-красного цвета; получают при разложении натриевых солей сурьмяной или тиосурьмяной кислот серной кислотой; применяется как пигмент.
Сурьмянистый водород
Сурьмя'нистый водоро'д,стибин, SbH 3, бесцветный легковоспламеняющийся газ с неприятным запахом; t кип-18 °С, t пл - 88 °С; получают действием атомарного водорода на соединения сурьмы или при действии кислот на антимониды магния или цинка. С. в. ядовит.
Сурьмяные руды
Сурьмя'ные ру'ды,природные минеральные образования, содержащие сурьму в таких соединениях и концентрациях, при которых их промышленное использование технически возможно и экономически целесообразно. В собственно С. р. главный минерал — антимонит (Sb 2S 3), содержащий до 71,4% Sb; в редких случаях С. р. представлены сложными сульфидами сурьмы, меди, ртути, свинца, железа (бертьерит, джемсонит, тетраэдрит, ливингстонит и др.), а также окислами и оксихлоридами (сенармонтит, надорит) сурьмы. Содержание Sb в пластовых рудных телах от 1 до 10%, в жильных — от 3 до 50%, среднее — 5—20%. Образуются при участии низкотемпературных гидротермальных растворов путём заполнения трещин в горных породах, а также вследствие замещения последних минералами сурьмы. Основное промышленное значение имеют два типа месторождений: пластовые тела, линзы, гнёзда и штокверки в выдержанных плащеобразных залежах, образующихся в результате метасоматического замещения кремнезёмом и соединениями сурьмы известняков под сланцевым экраном (в Китае — Сикуаншань, в СССР — Кадамджай, Терексай, Джижикрут в Средней Азии), и системы крутопадающих секущих кварцево-антимонитовых жил в сланцах (в СССР — Тургайское, Раздольнинское, Сарылах и др.; в Южной Африке — Гравелот и др.). Кварцево-антимонитовые руды практически монометальны; полисульфидные комплексные руды содержат иногда примеси флюорита и минералов Hg, Au, Ag, Cu, Pb, Zn, W, Sn, As. Запасы С. р. капиталистических и развивающихся стран оцениваются в 1,6—1,8 млн. т (1974). Добыча ведётся в основном подземным способом. Штуфные богатые руды жильных месторождений не требуют обогащения; более бедные подвергаются обогащению гравитационно-флотационным способом с получением концентрата с 30—55% Sb. Производство сурьмяного концентрата (в тысячах т Sb): Южная Африка (14—18), Боливия (11—14), Мексика (3—5), Турция (2—3), Марокко (1—2). Годовое производство сурьмы в капиталистических и развивающихся странах 40—50 тысяч т (1974), в том числе за счёт монометальных руд 90% (из них на долю пластовых залежей приходится 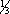 , а на долю секущих жил
, а на долю секущих жил 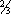 ) , комплексных руд 6% и сурьмусодержащих руд 4%. О получении и применении сурьмы см. в ст. Сурьма.
) , комплексных руд 6% и сурьмусодержащих руд 4%. О получении и применении сурьмы см. в ст. Сурьма.
Лит.: Федорчук В. П., Генетические и промышленные типы месторождений сурьмы, «Разведка и охрана недр», 1974, №8.
В. П. Федорчук.
Сурьмяный блеск
Сурьмя'ный блеск,то же, что антимонит
Сус (город в Тунисе)
Сус,город на восточном побережье Туниса, в заливе Хаммамет. 70 тыс. жителей (1973). Административный и промышленно-транспортный центр вилайета Сус. Порт (грузооборот 393 тысяч т в 1974). Узел шоссейных дорог. Ж.-д. станция. Предприятия текстильной, маслобойная, металлообрабатывающая промышленности. Автосборочный завод. Кустарное производство сафьяна. ТЭС. Курорт.
Основан финикийцами в начале 1-го тысячелетия до н. э. (Гадрумет); один из важных центров государства Карфаген. Во 2 в. до н. э. — 5 в. н. э. под властью Рима, затем — Византии. В конце 7 века завоёван арабами.
Сохранились многочисленные остатки античных построек, катакомбы. Средневековая часть С. окружена стенами (859). Среди памятников архитектуры — Большая мечеть (850) и др. Вне стен Старого С., у порта, с середины 20 в. растет Новый город. Археологический музей, Музей исламского искусства. Туризм.
Сус Николай Иванович
СусНиколай Иванович [1(13).6.1880, с. Огиевцы, ныне Волынской области, — 26.8.1967, г. Саратов], советский учёный, специалист в области агролесомелиорации, заслуженный деятель науки РСФСР (1947), почётный член ВАСХНИЛ (с 1956). Окончил Лесной институт в Петербурге (1907), с 1920 профессор Саратовского университета, с 1924 — Саратовского с.-х. института; одновременно (1931—38) работал во Всесоюзном научно-исследовательском институте агролесомелиорации. Основные труды посвящены вопросам укрепления оврагов и облесения песков, полезащитного лесоразведения. Награжден орденом Ленина, 2 другими орденами, а также медалями.
Читать дальшеИнтервал:
Закладка:
