БСЭ БСЭ - Большая Советская Энциклопедия (ФО)
- Название:Большая Советская Энциклопедия (ФО)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (ФО) краткое содержание
Большая Советская Энциклопедия (ФО) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Ф. обусловлена деформацией электронных оболочек атомов и молекул и ориентацией оптически анизотропных молекул либо их частей, а в полимерах – раскручиванием и ориентацией полимерных цепей. Для малых одноосных растяжений или сжатий выполняется Брюстера закон. D n = kP, где D n – величина двойного лучепреломления (разность показателей преломления для обыкновенной и необыкновенной волн), Р – напряжение, k – упругооптическая постоянная (постоянная Брюстера). Для стекол k = 10 -13–10 -12 см 2/дин, для пластмасс (целлулоид) k = 10 -12–10 -11 см 2/дин.
Ф. используется при исследовании напряжений в механических конструкциях, расчёт которых слишком сложен. Исследование двойного лучепреломления под действием нагрузок в выполненной из прозрачного материала модели (обычно уменьшенной) изучаемой конструкции позволяет установить характер и распределение в ней напряжений (см. Поляризационно-оптический метод исследования ) . Ф. лежит в основе взаимодействия света и ультразвука в твёрдых телах.
Лит.: Ландсберг Г. С., Оптика, 5 изд., М., 1976; Дитчберн Р., Физическая оптика, пер. с англ., М., 1965; Фрохт М. М., Фотоупругость, пер. с англ., т. 1–2, М. – Л., 1948–50; Физическая акустика, пер. с англ., т. 7, М., 1974, гл. 5; Александров А. Я., Ахметзянов М. Х., Поляризационно-оптические методы механики деформируемого тела, М., 1973.
Э. М. Эпштейн.
Фотофильм
Фотофи'льм,фильм (обычно короткометражный), состоящий из неподвижных фотографий. Метод Ф., занимающий промежуточное положение между киноискусством и фотоискусством, получил некоторое распространение к середине 20 в. (например, «Взлётная полоса» французского режиссер К. Маркера, 1962).
Фотоформа
Фотофо'рма, негатив или диапозитив, используемый в процессе изготовления печатной формы (см. Глубокая печать, Офсетная печать ) .
Фотохимический реактор
Фотохими'ческий реа'ктор, устройство в виде стеклянного или кварцевого сосуда, предназначенное для проведения химических реакций, протекающих под действием света (искусственного или солнечного). Используется в промышленных установках по производству различных веществ и материалов (например, в установках для нитрозирования циклогексана в процессе производства капролактама ) . См. также Солнечная фотосинтетическая установка.
Фотохимия
Фотохи'мия,раздел химии, в котором изучаются реакции химические, происходящие под действием света. Ф. тесно связана с оптикой и оптическими излучениями. Первые фотохимические закономерности были установлены в 19 в. (см. Гротгуса закон, Бунзена – Роско закон ) . Как самостоятельная область науки Ф. оформилась в 1-й трети 20 в., после открытия Эйнштейна закона, ставшего основным в Ф. Молекула вещества при поглощении кванта света переходит из основного в возбуждённое состояние, в котором она и вступает в химическую реакцию. Продукты этой первичной реакции (собственно фотохимической) часто участвуют в различных вторичных реакциях (т. н. темновые реакции), приводящих к образованию конечных продуктов. С этой точки зрения Ф. можно определить как химию возбуждённых молекул, образовавшихся при поглощении квантов света. Часто более или менее значительная часть возбуждённых молекул не вступает в фотохимическую реакцию, а возвращается в основное состояние в результате различного рода фотофизических процессов дезактивации. В ряде случаев эти процессы могут сопровождаться испусканием кванта света (флуоресценция или фосфоресценция). Отношение числа молекул, вступивших в фотохимическую реакцию, к числу поглощённых квантов света называются квантовым выходом фотохимической реакции. Квантовый выход первичной реакции не может быть больше единицы; обычно эта величина значительно меньше единицы из-за эффективной дезактивации. Вследствие же темновых реакций общий квантовый выход может быть значительно больше единицы.
Наиболее типичная фотохимическая реакция в газовой фазе – диссоциация молекул с образованием атомов и радикалов. Так, при действии коротковолнового ультрафиолетового (УФ) излучения, которому подвергается, например, кислород, образующиеся возбуждённые молекулы O 2 * диссоциируют на атомы:
O 2 + h n 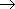
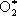 ,
, 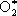 ® O + O.
® O + O.
Эти атомы вступают во вторичную реакцию с O 2, образуя озон: O + O 2® O 3.
Такие процессы происходят, например, в верхних слоях атмосферы под действием излучения Солнца (см. Озон в атмосфере ).
При освещении смеси хлора с насыщенными углеводородами (RH, где R – алкил) происходит хлорирование последних. Первичная реакция – диссоциация молекулы хлора на атомы, за ней следует цепная реакция образования хлор углеводородов:
Cl 2+ h n ® 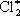 ® Cl + Cl
® Cl + Cl
Cl + RH ® HCl + R
R + Cl 2® RCl + Cl и т.д.
Общий квантовый выход этой цепной реакции значительно больше единицы.
При освещении ртутной лампой смеси паров ртути с водородом свет поглощается только атомами ртути. Последние, переходя в возбуждённое состояние, вызывают диссоциацию молекул водорода:
Hg* + H 2® Hg + H + H.
Это пример сенсибилизированной фотохимической реакции. Под действием кванта света, обладающего достаточно высокой энергией, молекулы превращаются в ионы. Этот процесс, называемый фотоионизацией, удобно наблюдать с помощью масс-спектрометра.
Простейший фотохимический процесс в жидкой фазе – перенос электрона, т. е. вызванная светом окислительно-восстановительная реакция. Например, при действии УФ света на водный раствор, содержащий ионы Fe 2 +, Cr 2 +, V 2 +и др., электрон переходит от возбуждённого иона к молекуле воды, например:
(Fe 2 +)* + H 2O ® Fe 3 ++ OH -+ Н +.
Вторичные реакции приводят к образованию молекулы водорода. Перенос электрона, который может происходить при поглощении видимого света, характерен для многих красителей. Фотоперенос электрона с участием молекулы хлорофилла представляет собой первичный акт фотосинтеза – сложного фотобиологического процесса, происходящего в зелёном листе под действием солнечного света.
В жидкой фазе молекулы органических соединений с кратными связями и ароматическими кольцами могут участвовать в разнообразных темновых реакциях. Кроме разрыва связей, приводящего к образованию радикалов и бирадикалов (например, карбенов ) , а также гетеролитических реакций замещения, известны многочисленные фотохимические процессы изомеризации, перегруппировок, образования циклов и др. Существуют органические соединения, которые под действием УФ света изомеризуются и приобретают окраску, а при освещении видимым светом снова превращаются в исходные бесцветные соединения. Это явление, получившее название фотохромии, – частный случай обратимых фотохимических превращений.
Читать дальшеИнтервал:
Закладка:
