БСЭ БСЭ - Большая Советская Энциклопедия (ЭЛ)
- Название:Большая Советская Энциклопедия (ЭЛ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (ЭЛ) краткое содержание
Большая Советская Энциклопедия (ЭЛ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Лит.: Милликен Р. Э., Электроны (+ и —), протоны, фотоны, нейтроны и космические лучи, пер. с англ., М. — Л., 1939.
Л. И. Пономарев.
Элементный анализ
Элеме'нтный ана'лизорганических соединений, элементарный анализ, совокупность методов количественного определения и качественного обнаружения элементов, входящих в состав органических соединений. Э. а. состоит из двух стадий: разложения органического вещества, например сжиганием в токе кислорода, сплавлением с некоторыми твёрдыми реагентами; количественного или качественного анализа образовавшихся неорганических соединений элементов (см. Количественный анализ, Качественный анализ ) .
Элементоорганические полимеры
Элементооргани'ческие полиме'ры,высокомолекулярные элементоорганические соединения. По составу главной и боковых цепей макромолекул Э. п. делят на 3 группы: 1) с неорганическими главными цепями, обрамленными органическими группами (например, полиорганосилоксаны, полиорганосилазаны — см. Кремнийорганические полимеры, полиорганофосфазены — см. Полифосфонитрилхлорид ) ; 2) с органонеорганическими главными цепями [например, карбосиланы (I), карбосилоксаны (II), борорганические полимеры с боразольными, фосфинбориновыми и карборановыми циклами в главной цепи, хелатные полимеры, содержащие в молекуле атомы металла, координационно связанные с органическими лигандами]; 3) с органическими главными цепями [например, полиалкенилтриалкилсиланы (III), фосфорсодержащие полимеры типа (IV); R — органический радикал].
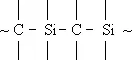 (I)
(I)
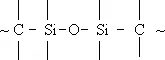 (II)
(II)
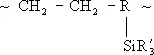 (III)
(III)
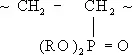 (IV)
(IV)
Наибольшее практическое применение из Э. п. получили кремнийорганические полимеры.
Лит.: Энциклопедия полимеров, т. 3, М., 1977.
Элементоорганические соединения
Элементооргани'ческие соедине'ния,содержат химическую связь элемент — углерод (к Э. с., как правило, не относят соединения, содержащие связь углерода с азотом, кислородом, серой и галогенами). Термин «Э. с.» предложен академиком А. Н. Несмеяновым. См. также Металлоорганические соединения, Кремнийорганические соединения, Фосфорорганические соединения, Борорганические соединения и др.
Элементы затрат
Элеме'нты затра'т,см. в ст. Себестоимость продукции.
Элементы орбиты
Элеме'нты орби'тыв астрономии, система величин (параметров), определяющих ориентацию орбиты небесного тела в пространстве, её размеры и форму, а также положение на орбите небесного тела в некоторый фиксированный момент. Невозмущённую орбиту, по которой движение тела происходит в соответствии с Кеплера законами, определяют 6 Э. о. 1) Наклон орбиты i к плоскости эклиптики или к плоскости земного экватора (в случае ИСЗ); может иметь значения от 0° до 180°. Наклон меньше 90°, если для наблюдателя, находящегося в северном полюсе эклиптики или в северном полюсе мира, тело представляется движущимся против часовой стрелки, и больше 90°, если тело движется в противоположном направлении. 2) Долгота (восходящего) узла 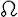 или прямое восхождение (восходящего) узла a W(для ИСЗ); может иметь значения от 0° до 360°. 3) Большая полуось орбиты а. Иногда вместо неё принимается среднее движение тела по орбите n, в случае невозмущённого движения однозначно зависящее от большой полуоси. 4) Эксцентриситет орбиты е. 5 ) Аргумент перигелия или перигея w (в случае Луны или ИСЗ); может иметь значения от 0° до 360°. 6) Эпоха (дата) Т, в которую тело находится в определённой точке орбиты, например в восходящем узле или в перигелии (перигее). Иногда в качестве эпохи выбирают начало суток, в этом случае положение орбиты задаётся средней аномалиейМ 0в эту эпоху.
или прямое восхождение (восходящего) узла a W(для ИСЗ); может иметь значения от 0° до 360°. 3) Большая полуось орбиты а. Иногда вместо неё принимается среднее движение тела по орбите n, в случае невозмущённого движения однозначно зависящее от большой полуоси. 4) Эксцентриситет орбиты е. 5 ) Аргумент перигелия или перигея w (в случае Луны или ИСЗ); может иметь значения от 0° до 360°. 6) Эпоха (дата) Т, в которую тело находится в определённой точке орбиты, например в восходящем узле или в перигелии (перигее). Иногда в качестве эпохи выбирают начало суток, в этом случае положение орбиты задаётся средней аномалиейМ 0в эту эпоху.
В случае возмущённой орбиты Э. о. рассматриваются как функции времени и обычно представляются в виде степенных рядов:
А = A 0 + A 1( t — T 0) + A 2( t — T 0) 2+...,
где A 0 — значение Э. о. А в эпоху T 0 . См. также Орбиты небесных тел, Орбиты искусственных космических объектов, Небесная механика.
Н. П. Ерпылёв.
Элементы химические
Элеме'нты хими'ческие.Каждый Э. х. — это совокупность атомов с одинаковым зарядом атомных ядер и одинаковым числом электронов в атомной оболочке. Ядро атомное состоит из протонов, число которых равно атомному номеру элемента, и нейтронов, число которых может быть различным. Разновидности атомов одного и того же Э. х., имеющие различные массовые числа (равные сумме масс протонов и нейтронов, образующих ядро), называются изотопами. В природе многие Э. х. представлены двумя или большим числом изотопов. Известно 276 стабильных изотопов, принадлежащих 81 природному Э. х., и около 1500 радиоактивных изотопов. Изотопный состав природных элементов на Земле, как правило, постоянен; поэтому каждый элемент имеет практически постоянную атомную массу, являющуюся одной из важнейших характеристик элемента. В настоящее время (1978) известно 107 Э. х., они, преимущественно нерадиоактивные, создают всё многообразие простых и сложных веществ. Простое вещество— форма существования элемента в свободном виде. Некоторые Э. х. существуют в двух или более аллотропных модификациях (например, углерод в виде графита и алмаза), различающихся по физическим и химическим свойствам; число простых веществ достигает 400 (см. Аллотропия ) . Иногда понятия «элемент» и «простое вещество» отождествляются, поскольку в подавляющем большинстве случаев нет различия в названиях Э. х. и образуемых ими простых веществ; «... тем не менее в понятиях такое различие должно всегда существовать», — писал в 1869 Д. И. Менделеев (Соч., т. 13, 1949, с. 490). Сложное вещество — соединение химическое— состоит из химически связанных атомов двух или нескольких различных элементов; известно более 100 тыс. неорганических и более 3 млн. органических соединений. Для обозначения Э. х. служат знаки химические, состоящие из первой или первой и одной из последующих букв латинского названия элемента. В формулах химических и уравнениях химических каждый такой знак (символ) выражает, кроме названия элемента, относительную массу Э. х., равную его атомной массе. Изучение Э. х. составляет предмет химии, в частности неорганической химии.
Читать дальшеИнтервал:
Закладка:
