Вилен Барабой - Ядерные излучения и жизнь
- Название:Ядерные излучения и жизнь
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1972
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Вилен Барабой - Ядерные излучения и жизнь краткое содержание
Ядерные излучения и жизнь - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Нужно учесть, что теоретические представления, которые легли в основу известных опытов Баррона и послужили толчком к испытанию противолучевых свойств сульфгидрильных соединений, в последующие годы претерпели серьезные изменения. Прежде всего оказалось, что те самые тиоловые ферменты, которые Баррон облучал в пробирках, совершенно иначе ведут себя в организме. Под влиянием даже смертельных доз радиации их активность не снижается. Наоборот, в ряде случаев в результате облучения наблюдалось увеличение их активности. Этот факт никак не вяжется с концепцией Баррона.
Однако защитное действие содержащих серу соединений было открыто. Пришлось срочно подводить под старую крышу новые стены, подыскивать новое объяснение фактам, обнаруженным на базе старой, ошибочной концепции. Теперь большинство ученых полагают, что механизм защитного действия соединений типа цистеина и цистеамина сводится к перехвату активных радикалов "на подходе" к белкам и другим биополимерным структурам. Благодаря сульфогидрильным группам эти вещества легко реагируют с любыми окислительными агентами. Окисляясь сами, они при этом обезвреживают, инактивируют свободные радикалы и перекиси, уменьшая их разрушительное действие на биополимерные структуры клетки.
Норвежские исследователи Элдьярн и Пиль предложили новую и оригинальную гипотезу защитного действия тиоловых соединений. Им удалось показать, что при введении в организм эти соединения вступают в связь с белками, а именно с их сульфогидрильными группами, образуя смешанные дисульфиды:
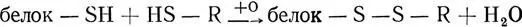
Сульфогидрильные группы белков, вступившие в такую временную связь, не боятся окисляющего действия свободных радикалов. Многие ученые в своих исследованиях подтвердили эту гипотезу. Так, советским радиобиологам В. Г. Яковлеву и Ф. Ю. Рачинскому с помощью меченого цистеамина (содержащего радиоактивную серу) удалось получить прямые доказательства образования смешанных дисульфидов белков и цистеамина.
Однако противолучевые вещества, содержащие - SH-группы, в опытах вне организма дают защиту полимеров, не содержащих серы, в том числе и нуклеиновых кислот; по-видимому, они защищают ДНК и в условиях организма. Это их действие нельзя объяснить с помощью теории образования смешанных дисульфидов.
В последние годы Бак и Александер выдвинули новые теоретические представления, позволяющие лучше понять механизм защитного действия тиоловых препаратов. Придавая особенно важное значение собственным биохимическим реакциям клеток организма на воздействие радиации, ученые пришли к выводу, что образование смешанных дисульфидов между введенным защитным препаратом и клеточными белками действительно имеет место, но это лишь первый шаг в механизме защиты. Вступив в соединение с белками клеток, защитные препараты оказывают сильное влияние на внутриклеточные процессы, вызывая набухание митохондрий, повышение проницаемости их мембран. Часть ферментов и более просто устроенных веществ выходит из митохондрий в протоплазму клетки и оказывает сильное влияние на все процессы ее жизнедеятельности.
Введение защитного вещества вызывает, таким образом, своего рода "биохимический шок" клетки, серьезную перестройку ее внутренней организации. Весь комплекс изменений или во всяком случае их часть таковы, что существенно повышают сопротивляемость клетки действию радиации, ее устойчивость в условиях облучения. Одно из проявлений "биохимического шока", имеющее, быть может, наиболее важное значение в механизме защиты, - увеличение в клетке количества свободных - SH-групп. Исследования советского радиобиолога Э. Я. Граевского и его сотрудников показали, что увеличение внутриклеточного уровня тиоловых групп происходит лишь частично (не более чем на 25 - 35%) за счет накопления . введенного извне радиозащитного вещества. Главное значение имеет мобилизация собственных ресурсов клетки. Освобождающиеся в клетке в процессе "биохимического шока" сульфогидрильные группы обладают высокой химической реактивностью, и именно они, очевидно, дают эффект защиты, перехватывая и обезвреживая водные радикалы на подходе к белкам и нуклеиновым кислотам.
Важную роль в механизме лучевого поражения играет растворенный в жидкостях организма кислопотт. Некоторые ученые высказали предположение, что тио-ловые защитные вещества связывают не только окислительные радикалы, но и кислород, уменьшая тем самым "кислородный эффект" облучения. Если цистеин связывает кислород и тем самым оказывает защитное действие, увеличение давления кислорода во вдыхаемом воздухе должно уменьшить его защитный эффект. И действительно, с помощью кислорода под давлением удалось снять противолучевое действие цистеина. Кислород под давлением, кстати говоря, совершенно самостоятельно вызывает повреждения, очень сходные с лучевыми.
Прямое определение кислорода в тканях живого организма осуществили в очень интересных и тщательно поставленных опытах советские ученые Э. Я. Граевский и М. М. Константинова. Они установили, что введение цистеамина и других сульфогидрильных соединений не оказывает достоверного влияния на уровень кислорода. Следовательно, в живом организме процессы происходят намного сложнее, чем это представляется некоторым ученым на основании модельных опытов в пробирке или даже экспериментов на мышах.
Однако мысль о возможности снижения глубины лучевых поражений путем уменьшения концентрации кислорода в клетках, вопреки первым неудачам, оказалась плодотворной. Снизить уровень кислорода в тканях - вызвать тканевую гипоксию - можно легче всего путем уменьшения количества кислорода во вдыхаемом воздухе. Такой опыт удобно осуществить на микроорганизмах, которые длительное время могут существовать в бескислородных условиях. Эти опыты, поставленные американским радиобиологом А. Холлендером и учеными других стран на бактериях (кишечной палочке и др.), водорослях, грибках, дали отличный результат. При одной и той же дозе облучения гибель микроорганизмов и задержка их деления были тем меньше, чем ниже концентрация кислорода в окружающей их среде.
В опытах на млекопитающих воспроизвести такие условия невозможно. Но все же снижение количества кислорода во вдыхаемом воздухе (до 5 - 7%) на 40 - 70% уменьшает гибель мышей, облученных летальными дозами радиации.
При понижении температуры тела животного (гипотермии) снижается интенсивность обменных процессов, в том числе окислительных процессов, связанных с поступлением кислорода в ткани и клетки. Установлено, что и гипотермия значительно уменьшает вредное действие радиации. Более того, оказалось, что животные (сурки, хомяки, суслики и др.), находящиеся в состоянии зимней спячки, без видимого вреда переносят такие дозы радиации, которые для них абсолютно смертельны в активном состоянии. Симптомы лучевой болезни у облученных животных проявлялись только после пробуждения от зимней спячки, когда с момента облучения прошло две-три недели. Эти исследования убедительно доказывают участие кислорода в механизме разрушительного действия радиации и перспективность методов защиты организма от облучения путем удаления кислорода из тканей или недопущения его в клетки.
Читать дальшеИнтервал:
Закладка: