Джеймс Уотсон - ДНК. История генетической революции
- Название:ДНК. История генетической революции
- Автор:
- Жанр:
- Издательство:Издательство Питер
- Год:2018
- Город:Санкт-Петербург
- ISBN:978-5-4461-0549-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Джеймс Уотсон - ДНК. История генетической революции краткое содержание
ДНК. История генетической революции - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Со времени эпохального отчета, составленного группой из Сент-Луиса, отсеквенировано уже множество раковых геномов, что помогло лучше определить спектр мутационных механизмов, стимулирующих рост опухолей. Вооружившись материалами программ Национального онкологического института, и в частности «Атласом ракового генома» (TCGA) – исчерпывающими каталогами генетических вариантов и генетической активности в десятках видов опухолей у тысяч пациентов, мы до сих пор обнаруживаем новых генетических персонажей в онкологической трагедии. Среди них множество генов, которые ранее никто и не думал подозревать в связи с раком. Красота систематических полногеномных исследований рака в том, что они дают непредвзятую картину всего спектра раковых мутаций. Мы больше не ограничены лишь тем набором генов, которые осознанно ищем. Уже известно, что при различных онкологических заболеваниях возникают мутации примерно в трех сотнях генов; ученые составили схемы тех процессов и биохимических путей, когда эти пути нарушаются. Гены могут быть связаны с метаболизмом, клеточным циклом, эпигенетикой, модификацией гистонов, генетической регуляцией и обеспечением целостности генома. Наконец-то за деревьями начал просматриваться лес. Пестрое множество мутантных генов постепенно упорядочивается в виде удобоваримого списка путей и процессов, которые нарушаются при раке.

Первооткрыватель лекарств Джей Бреднер (слева) знакомится с исследовательскими данными в компании Novartis
Недаром Джей Бреднер, онколог, ранее работавший в Институте онкологических исследований Даны Фарбер в Гарварде, а теперь возглавляющий отдел НИОКР в кембриджской компании Novartis , называл RAS, MYC и p53 «тремя неуязвимыми всадниками ракового апокалипсиса». Они стали такими знаменитыми мишенями не только потому, что так распространены, но и потому, что десятилетиями стимулировали разработку лекарств, упрямо не давая ни одной подходящей молекулярной канавки, которую мог бы заблокировать мелкомолекулярный препарат. Поэтому химики между собой называют их лекарственно недосягаемыми («undruggable»). В то время как большинство белков услужливо предлагают сколько угодно уголков и закоулков, где может разместиться маленький ген, RAS , например, является совершенно ровным, и там решительно негде закрепиться.
Для того чтобы найти препарат, который мог бы наконец справиться с RAS , Гарольд Вармус, еще будучи директором Национального института онкологии, в 2013 году запустил программу стоимостью 10 миллионов долларов под названием RAS Initiative. «Поиск лекарства для RAS – национальный приоритет», – считает Грег Вердайн, опытный химик из Гарвардского университета. RAS – первоочередная цель для его биотехнологической компании Warp Drive Bio . Возможно, определение приоритетов наконец начало приносить плоды. Кеван Шокат, исследователь из Медицинского института Говарда Хьюза при Калифорнийском университете в Сан-Франциско, недавно разработал новое соединение, которое может необратимо связываться со специфической формой RAS , вызывающей рак легких, но при этом не повреждает нормальную молекулу RAS . « RAS – словно переключатель, запускающий рак, а эта молекула позволяет надежно удерживать его в выключенном состоянии», – поясняет Кеван Шокат.
Наряду с RAS в списке приоритетных целей у разработчиков лекарств значится MYC . Этот белок активируется в семи из десяти случаев рака и вызывает рост и пролиферацию клеток. MYC – важнейшая шестеренка в процессе нормального клеточного деления, но в раковых клетках он напоминает сорванный вентиль. Срочность с разработкой лекарства от MYC объясняется тем, что он играет центральную роль во многих сигнальных путях и сетях. Как и RAS , он также удручающе гладкий. Поэтому многие исследователи пытались приглушить вредоносность MYC , нацеливаясь на другие шестеренки в онкогенной сети, в частности на небольшую группу белков, именуемых BET -активаторами. Первый эффективный ингибитор BET , который удалось разработать, называется JQ1 в честь Цзюнь-Ци, китайского сотрудника из лаборатории Бреднера. Цзюнь-Ци синтезировал соединение JQ1 , которое, связываясь с белком BRD4 из группы BET , не позволяет ему соединиться с промоторным участком ДНК, включающим MYC . Становится понятным: чтобы полностью блокировать MYC , потребуются гораздо более эффективные ингибиторы BET .
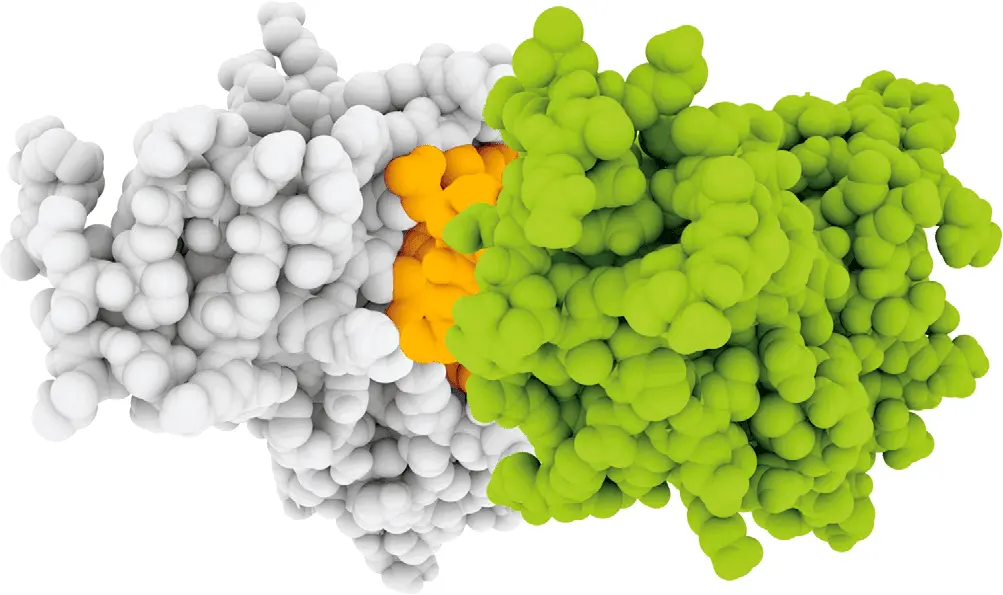
В поисках кооперации: лекарственное нацеливание – подход, широко применяемый в компании Warp Drive Bio, – обеспечивает связывание мелкомолекулярного препарата (оранжевый) с презентирующим белком (серым), который, в свою очередь, прикрепляется к мишени, например к RAS
Совершенно неудивительно, что среди первых пациентов, пытавшихся излечиться от рака при помощи секвенирования ДНК, были знаменитости первой величины с хорошими связями среди известных деятелей медицины. В 2004 году сооснователь Apple Стив Джобс по электронной почте сообщил коллегам, что ему диагностировали нейроэндокринный рак поджелудочной железы. Сделав ему биопсию опухоли, врачи секвенировали ДНК, но не получили четких результатов, необходимых для идентификации конкретных мутаций или лекарственных мишений, чтобы спасти Джобса. Когда в 2010 году британскому писателю, литературному критику и убежденному атеисту Кристоферу Хитченсу диагностировали рак пищевода – ту самую болезнь, от которой умер его отец, – к нему обратился его знакомый, директор Национальных институтов здравоохранения (и искренний христианин) Френсис Коллинз, иногда выступавший его оппонентом в ходе дебатов. Коллинз предложил Хитченсу провести секвенирование генома. ДНК из опухоли Хитченса (которую Коллинз сравнил со «слепым и бесчувственным монстром») секвенировала группа Мардис и Уилсона в Вашингтонском университете в Сент-Луисе.
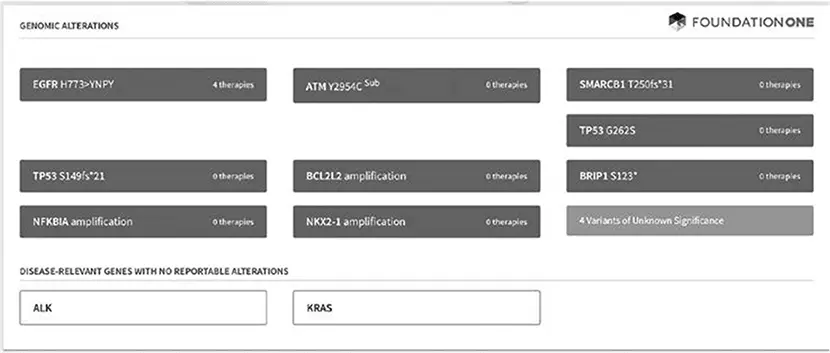
Отчет об анализе генома пациента с аденокарциномой легких. Перечислены гены, в которых кроются потенциально опасные мутации
Результаты оказались удивительными: обнаружилась специфическая мутация, связанная с одной из форм лейкемии, а не с раком пищевода. Поэтому врачи решили не прибегать к традиционной терапии, а прописали Хитченсу Gleevec , нацеленный на борьбу именно с этой мутацией. В таком режиме лечения Хитченс как никогда активно размышлял о проблеме рака – до самой смерти в конце 2011 года (он умер от пневмонии). Хотя ни Джобс, ни Хитченс не излечились от рака, их случаи иллюстрируют фундаментальную перемену в наших представлениях об онкологии, связанную с возможностью геномного анализа. Для принятия наиболее точного и эффективного решения требуется понимать генетику опухоли, а не ее локализацию в организме (как считалось ранее в течение целых десятилетий).
Читать дальшеИнтервал:
Закладка:










