Джеймс Уотсон - ДНК. История генетической революции
- Название:ДНК. История генетической революции
- Автор:
- Жанр:
- Издательство:Издательство Питер
- Год:2018
- Город:Санкт-Петербург
- ISBN:978-5-4461-0549-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Джеймс Уотсон - ДНК. История генетической революции краткое содержание
ДНК. История генетической революции - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Такое биохимическое сходство между разными организмами нагляднее всего демонстрируется в ходе так называемых спасительных экспериментов, цель которых – устранить тот или иной белок у одного вида, а затем задействовать соответствующий белок от другого вида, чтобы ликвидировать сложившиеся в ходе патологического процесса или уже имеющиеся дисфункции. Мы уже видели, как эта стратегия применяется в случае с белком инсулином. Поскольку человеческий и коровий инсулин схожи, диабетики выживают, принимая коровий инсулин в качестве заменителя человеческого.
В опыте, напоминающем эпизод из проходного научно-фантастического фильма, исследователи смогли вырастить глаза на лапках у дрозофил, манипулируя конкретным геном, определяющим расположение глаз у этой мушки. Этот ген инициирует работу множества других генов, участвующих в формировании глаза в заданном месте. Аналогичный мышиный ген настолько похож на ген дрозофилы, что будет работать точно так же, если поместить его – к слову, современный генетик делает это мановением руки – в геном дрозофилы, у которой этот ген ранее устранен. Сам факт, что такое возможно, мягко говоря, примечателен. Эволюция разделила предков дрозофил и мышей не менее полумиллиарда лет тому назад. Таким образом – следуя логике, которая применима к формированию эволюционных линий человека и дрожжей, развивавшихся одновременно и независимо друг от друга, – этот ген сохранился на протяжении более миллиарда лет эволюции. Ситуация станет еще более удивительной, если учесть, что мышиный глаз принципиально отличается от глаза дрозофилы как по структуре, так и по оптическим характеристикам. Предположительно, в каждой эволюционной линии глаз адаптировался к решению конкретных задач, но базовый механизм, определяющий местоположение глаза, в совершенствовании не нуждался и поэтому не изменился.
Наиболее отрезвляющим в рамках проекта «Геном человека» было осознание того, как удивительно мало мы знаем о функциях абсолютного большинства человеческих генов. Отсеквенированный геном – это подробный инвентарный список для сборки организма, но в нем не прописано, как именно собрать организм и как он затем будет работать. Чтобы воспользоваться этой добытой с таким трудом информацией, необходимо разработать методы для изучения функций генов в масштабах всего генома.
На заре разработки проекта «Геном человека» быстро сформировалось несколько новых научных дисциплин, получивших незапоминающиеся названия, которые заканчивались на «-омика», по образу «геномики». Две наиболее важные дисциплины именуются протеомика и транскриптомика, наряду с ними существуют еще и гликомика, липидомика, метаболомика и масса других дисциплин с еще более уморительными названиями. Протеомика – это наука о белках, кодируемых генами. Протеомика изучает, где и в каких ситуациях экспрессируются гены, то есть какие гены проявляют транскрипционную активность в конкретной клетке. Если требуется так или иначе понять работу генома в динамике, то есть рассмотреть, как разыгрывается сценарий жизни, то протеомика, транскриптомика и им подобные науки помогут взглянуть на это действо. Проблема состоит в том, что чем больше мы узнаем, тем лучше понимаем, что жизнь – это кинофильм с бесконечным числом кадров.
Ученые давно догадывались, что с биологической точки зрения белок гораздо сложнее, чем линейная последовательность аминокислот, из которых он состоит. Чтобы понять, как работает белок, необходимо разобраться, как именно эта последовательность сворачивается в уникальную трехмерную конфигурацию – такими вопросами и занимается протеомика. Структурный анализ белков по-прежнему выполняется при помощи рентгеновской дифракции: молекула бомбардируется рентгеновскими лучами, которые отражаются от атомов и при рассеянии образуют характерный узор, по которому можно определить трехмерную форму белка. В 1962 году Джон Кендрю и Макс Перуц, с которыми нам в свое время довелось вместе работать в Кавендишской лаборатории, совместно получили Нобелевскую премию по химии за уточнение структур двух белков: миоглобина (участвующего в создании в мышцах кислородного резерва, который расходуется по мере необходимости, восполняя временную нехватку кислорода) и гемоглобина (способного обратимо связываться с кислородом, обеспечивая его перенос в ткани). Это была фундаментальная работа. Рассматривая рентгеновские дифракционные снимки, которые они интерпретировали, я смог понять, насколько же просто (в сравнении с белками) устроена ДНК!
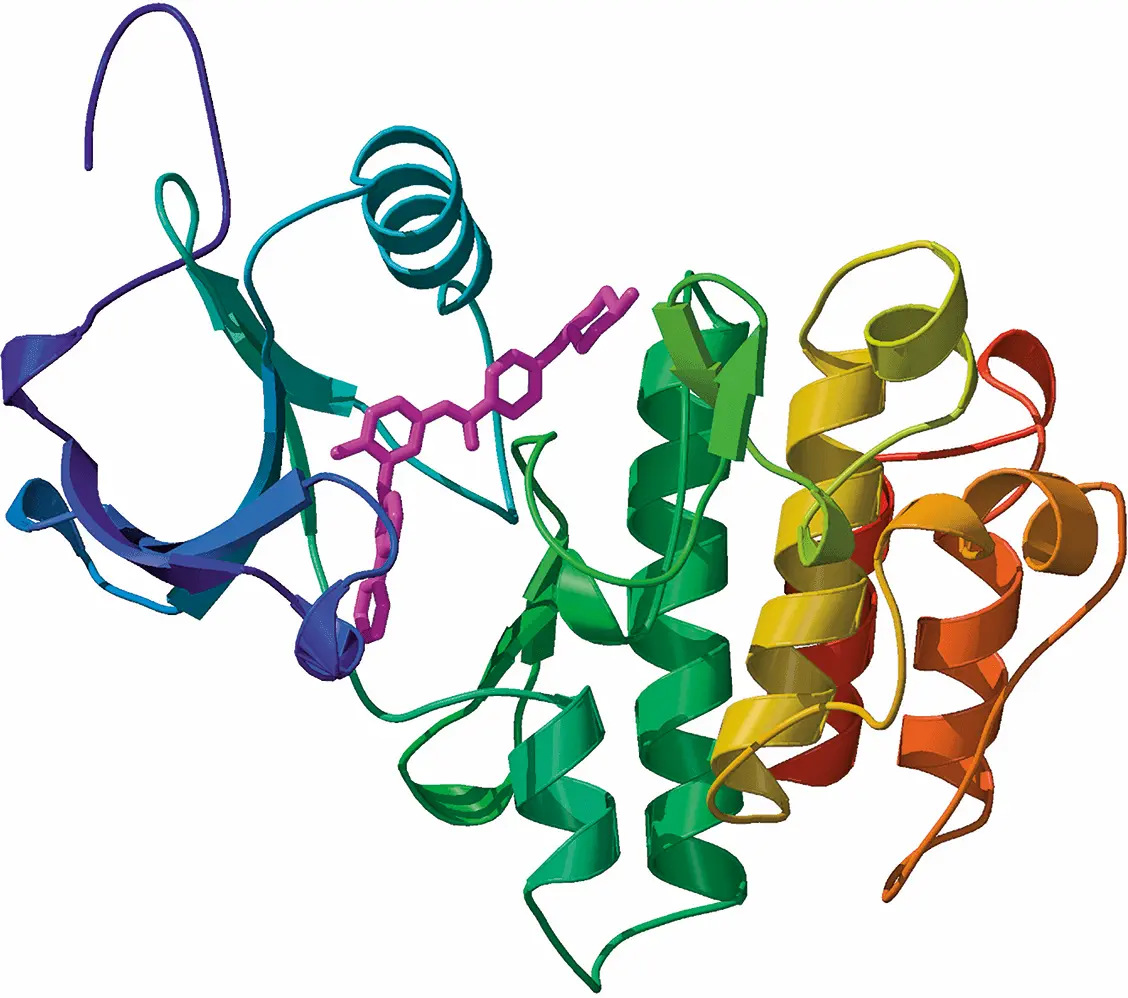
Протеомика: трехмерная структура белка BCR-ABL, вызывающего рак. Слияние двух генов, вызванное хромосомной аномалией, приводит к синтезу этого гибридного белка, вызывающего пролиферацию клеток и провоцирующего одну из форм лейкемии. Сиреневым показан препарат Gleevec, селективный ингибитор BCR-ABL (см. главу 14). Работа с такой трехмерной моделью помогает при разработке лекарств. (В структурной модели BCR-ABL не демонстрируются детали атомов или отдельных аминокислот, тем не менее компоновка белка передана точно.)
Представление об объемной структуре белка значительно облегчает работу химиков-фармацевтов, занятых поиском новых действенных лекарств (терапевтическая функция многих препаратов основана на ингибировании действия определенных белков). В нашем все более специализированном и автоматизированном мире фармацевтических исследований появились компании, предлагающие услуги по определению структуры белка, словно белок – штампованная конвейерная продукция. Теперь такая работа выполняется проще, чем во времена Перуца и Кендрю: появились более мощные рентгеновские облучатели, автоматизировалась запись данных, сами компьютеры стали гораздо быстрее, а их программы – интеллектуальнее. Поэтому расшифровка структуры белка теперь может занимать не годы, а считаные недели. В конце 2015 года в «базе данных белков» содержались атомные структуры более 26 тысяч человеческих белков.
Однако сплошь и рядом трехмерная структура как таковая ничего не говорит о функции белка. Напротив, важные подсказки можно получить, изучая, как именно неизвестный белок взаимодействует с белками-партнерами, ранее известными. Простой способ идентификации таких взаимодействий (BiFC) заключается в следующем: в условиях in vitro известный белок соединяем с неизвестным, обработанным флюорохромной меткой, флюорохром подбираем таким образом, чтобы испускаемое излучение было видимым в ультрафиолете. Остается обнаружить флуоресцентные сигналы заметной интенсивности взаимодействующих белковых комплексов. В таком случае можно предположить, что и внутри клетки два этих белка должны взаимодействовать. BiFC-подход существенно облегчил визуализацию сайтов белковых взаимодействий на субклеточном уровне.
Читать дальшеИнтервал:
Закладка:










