Александр Марков - Рождение сложности. Эволюционная биология сегодня: неожиданные открытия и новые вопросы
- Название:Рождение сложности. Эволюционная биология сегодня: неожиданные открытия и новые вопросы
- Автор:
- Жанр:
- Издательство:Астрель, Corpus
- Год:2010
- Город:Москва
- ISBN:978-5-271-24663-0
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Александр Марков - Рождение сложности. Эволюционная биология сегодня: неожиданные открытия и новые вопросы краткое содержание
Рождение сложности. Эволюционная биология сегодня: неожиданные открытия и новые вопросы - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Для управления собственными генами зародыш использует множество разных механизмов: это и регуляция транскрипции (считывания генов) при помощи малых РНК и специальных регуляторных белков — транскрипционных факторов ( Hox -гены, как мы помним, тоже кодируют транскрипционные факторы), и особые «эпигенетические» механизмы, о которых мы подробнее поговорим в главе 8.
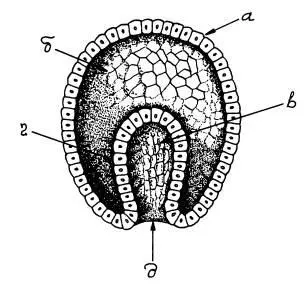
Типичная гаструла многоклеточного животного. а — эктодерма (наружный зародышевый листок), б — бластоцель (первичная полость тела), в — первичная кишка, г — энтодерма (внутренний зародышевый листок), д — бластопор (первичный рот).
Еще одно обстоятельство, которое делает сомнительным тезис о полной и однозначной обусловленности онтогенеза геномом зиготы, состоит в том, что, как уже было сказано выше, у подавляющего большинства животных на ранних стадиях развития геном вообще не функционирует. Он просто-напросто отключен, все гены молчат и матричные РНК («считываемые» с генов матрицы для синтеза белка) не производятся.
Зародыш между тем претерпевает сложные превращения. Яйцеклетка начинает дробиться, число клеток эмбриона растет в геометрической прогрессии: 2, 4, 8, 16, 32… Наконец формируется однослойный шар из клеток (бластула). Клетки, находящиеся на одном из полюсов бластулы, мигрируют внутрь, давая начало второму зародышевому листку (энтодерме), из которой позже разовьется кишечник. На этой стадии двуслойный зародыш называется гаструлой. Только на этом этапе у многих животных начинают наконец включаться гены, унаследованные от папы с мамой. У других это происходит чуть раньше — на стадии бластулы. И только млекопитающие — группа, уникальная во многих отношениях, — включают свои гены еще раньше (например, мышь делает это на стадии двух клеток) [64] Другая уникальная особенность млекопитающих — мощное развитие «геномного импринтинга», механизма, при помощи которого родители целенаправленно влияют на наследственные свойства эмбриона, отчасти — в своих собственных корыстных интересах (см. главу 8). Вполне возможно, что между этими двумя особенностями существует связь. Родители могут быть заинтересованы в том, чтобы «отредактированные» ими гены зародыша включились пораньше.
.
Как удается эмбриону развиваться без всякого «генетического контроля» вплоть до стадии гаструлы? Почему гены зародыша так долго остаются выключенными? Какие механизмы обеспечивают отключение генов в зиготе, а затем их своевременное включение [65] Последующий текст данного раздела основан на статье: Alexander F. Schier. The Maternal-Zigotic Transition: Death and Birth of RNAs // Science. 2007. V. 316. P. 406–407.
?
Ответ на первый вопрос более или менее ясен. Яйцеклетка содержит большое количество матричных РНК, унаследованных от материнского организма. Эти мРНК считываются с материнских генов заблаговременно, в процессе созревания яйцеклетки. Именно они обеспечивают синтез белков, необходимых для ранних стадий онтогенеза. В определенный момент материнские мРНК начинают уничтожаться. Это происходит как раз тогда, когда зародыш начинает сам производить мРНК, то есть включает свои гены. Этот довольно быстрый процесс замены зародышем материнских мРНК на свои собственные называется maternal-zygotic transition (MZT).
Менее ясен вопрос о том, что движет процессом MZT. Предполагается три возможных механизма.
1. По мере роста числа клеток, из которых состоит зародыш, начинает сказываться нехватка тех веществ (что бы они из себя ни представляли), которые не позволяют генам зародыша включиться. Ранние стадии эмбриогенеза животных не случайно называют «дроблением»: зигота именно дробится, клетки эмбриона после каждого деления становятся все мельче, поскольку между клеточными делениями отсутствует стадия роста клеток. Общее количество цитоплазмы не растет, тогда как количество клеточных ядер, а следовательно и ДНК, увеличивается в геометрической прогрессии. Если предположить, что яйцеклетка заранее запаслась какими-то ингибиторами транскрипции, то количество этих гипотетических ингибиторов, приходящихся на каждую клетку, должно быстро убывать, и в конце концов их остается так мало, что они уже не могут сдерживать транскрипцию.
2. Не исключено, что в зиготе изначально имеет место целенаправленное блокирование некоторых ключевых генов, работа которых инициирует транскрипцию. Так, показано, что искусственное введение в эмбрион мощных активаторов транскрипции (транскрипционных факторов «широкого спектра действия») может вызвать преждевременное частичное включение эмбрионального генома.
3. Наконец, сама по себе быстрая череда клеточных делений может мешать транскрипции. Ведь каждому делению должно предшествовать удвоение ДНК (репликация). В ходе дробления репликация должна происходить по сути дела непрерывно. Между тем известно, что репликация может мешать транскрипции, а во время клеточного деления (митоза) могут происходить обрыв и уничтожение тех мРНК, синтез которых еще не закончился. Может быть, клетки эмбриона просто физически не успевают транскрибировать свои гены? Искусственное замедление процесса дробления действительно может вызвать преждевременное включение эмбрионального генома. Кстати, у млекопитающих дробление протекает сравнительно медленно, не этим ли объясняется раннее включение генов зародыша?
Впрочем, ни одна из этих теорий не объясняет всей совокупности имеющихся фактов. Например, они не могут объяснить, почему эмбриональные гены включаются не все сразу, а постепенно, в строго определенном порядке.
Вторым существенным аспектом MZT является уничтожение материнских мРНК. Тут, как выяснилось, все предусмотрено заранее: материнские мРНК помечены особой последовательностью нуклеотидов, расположенной на нетранслируемом (то есть не кодирующем белок) «хвостике» этих молекул. Среди первых генов, которые эмбрион включает в процессе MZT, находятся гены особых белков и маленьких РНК, которые распознают эту последовательность, прикрепляются к ней и тем самым инициируют уничтожение материнских мРНК.
До полного понимания всех этих процессов науке еще очень далеко, но дело движется. Когда основные механизмы генной регуляции в ходе раннего онтогенеза будут расшифрованы, биологи смогут вплотную заняться следующим принципиальным вопросом, а именно — зачем все это надо? Почему животные не доверяют своему геному контроль над ранними стадиями развития, а потом в какой-то момент вдруг «переключаются» с материнских мРНК на свои собственные?
Между прочим, эта проблема имеет не только теоретическое, но и практическое значение. Трудности, с которыми сталкиваются работы по клонированию животных, во многом определяются тем, что мы еще слишком мало знаем о работе генов в ходе раннего развития. Клонирование животных осуществляется путем пересадки ядра из соматической (неполовой) клетки одного животного в яйцеклетку другого. Однако для нормального развития необходимо, чтобы гены зародыша поначалу помалкивали, а они в донорском ядре вполне активны. Цитоплазма яйцеклетки должна каким-то образом «перепрограммировать» ядро, выключить геном, а потом в нужный момент снова включить его. Пока мы не знаем, как ей в этом помочь, больших успехов в клонировании ожидать трудно.
Читать дальшеИнтервал:
Закладка:







