Вильгельм Штрубе - Пути развития химии. Том 2. От начала промышленной революции до первой четверти XX века
- Название:Пути развития химии. Том 2. От начала промышленной революции до первой четверти XX века
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1984
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Вильгельм Штрубе - Пути развития химии. Том 2. От начала промышленной революции до первой четверти XX века краткое содержание
Пути развития химии. Том 2. От начала промышленной революции до первой четверти XX века - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
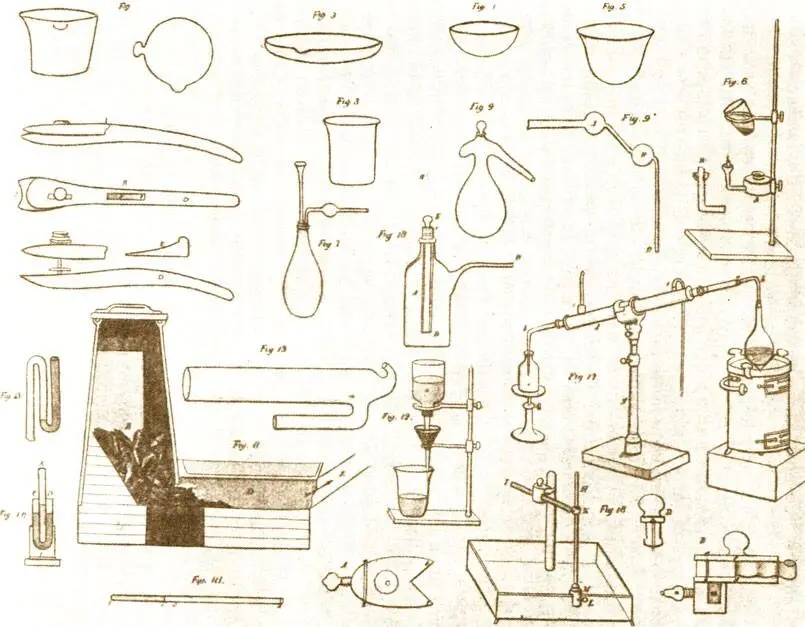
Лабораторное оборудование Й. Берцелиуса (1820 г.)
Изобретение "вольтова столба" открыло перед химическим анализом новые возможности. С этого времени использование электрического тока, а также различных измерительных приборов и систем, позволяющих работать при разных давлениях, постепенно вошло в обычную практику.
Й. Я. Берцелиус сконструировал и изготовил многочисленные приборы из стекла. Он сам был великолепным стеклодувом и считал, что химик должен уметь обращаться со стеклом и паяльной трубкой [196]. Даже во второй половине XIX в. химик должен был большей частью сам изготовлять некоторые из необходимых ему деталей лабораторных приборов из стекла. Создание большого числа лабораторий послужило стимулом к возникновению промышленного производства химикатов и реактивов. Это позволило заказывать реактивы и запасаться ими заранее. Во второй половине XIX в. цена на реактивы была очень высока, и для студентов покупка реактивов обходилась весьма дорого. В целом, включая все другие расходы, стоимость обучения химии одного студента в Германии в 1913 г. составляла 10 000 марок. Для сравнения достаточно, например, сказать, что штатив с двумя кольцами, одним зажимом и одной муфтой стоил в то время 6 марок 45 пфеннигов, а одно куриное яйцо — лишь 8 пфеннигов [91, с. 287].
Каждый пытливый химик так или иначе внес свой вклад в совершенствование лабораторной техники. Приведем некоторые примеры. Уже со времен Либиха и Вёлера для проведения химических реакций под давлением использовались запаянные трубки. После усовершенствования калориметра П. Фавром и Ж. Зильберманом (в 1848 г.) стало возможным определять теплоты сгорания органических веществ. Важную роль в лабораторной практике играл микроскоп, который впервые для исследования природных явлений использовал А. ван Левенгук [197]. В конце XVIII в. А. Маргграф с помощью микроскопа установил идентичность кристаллов свекловичного и тростникового сахара. В конце XVIII в. Товий Егорович (Иоганн Тобиас) Ловиц использовал микроскоп для определения кристаллических форм веществ, а минералоги — для определения состава продуктов, получающихся при прокаливании образцов с использованием паяльной трубки.
В середине XIX в., после того как стало известно, что существует определенная зависимость между интенсивностью окраски раствора и количеством вещества, вызывающим эту окраску, были созданы первые колориметры. В 1853 г. Александр Мюллер представил в "Журнал прикладной химии" статью "Усложненный колориметр" [65]. Дальнейшее развитие колориметрии связано с именем Ж. Дюбоска (1863 г.). В журнале "Новости химии" он описал двухлучевой колориметр [66].
Говоря об оптических методах, следует упомянуть и фотометрию. И. Бар и Р. Бунзен использовали для количественного анализа абсорбционную спектроскопию (спектры поглощения). В 1870 г. К. Фирордт опубликовал работу о применении созданного им спектрофотометра для измерения спектров поглощения и количественного анализа [67]. В 1877г. П.Глен и К. Г. Хюфнер сконструировали фотометр, в котором интенсивность света регулировалась с помощью поляризатора.
Учитывая значения критических температур газов, Рауль Пикте (Женева) и Луи Кайете (Париж) независимо друг от друга разработали установки для работы при высоких давлениях с такими газами, как кислород, азот и оксид азота. Карл Линде и другие ученые усовершенствовали эти установки: в них за счет расширения сильно охлажденных газов создавались еще более низкие температуры, которые использовались для проведения химических экспериментов, при этом были получены водород и кислород в твердом состоянии, а также жидкий гелий. Были достигнуты температуры, близкие к абсолютному нулю. В лабораториях ученые стали получать жидкие воздух и диоксид серы, твердый диоксид углерода.
Для измерения электропроводности растворов Ф. Р. Кольрауш в 1879 г. разработал метод, который позволял наряду с определением молекулярного веса (массы) устанавливать и степень диссоциации электролита.
В 1892 г. французский ученый А. Муассан впервые использовал электрическую печь. Нагревая в ней вещества до очень высоких температур, он смог получить карбиды и нитриды металлов.
Пятью годами позднее немецкий физико-химик Г. Гольд -шмидт разработал метод, названный алюмотермией, пользуясь которым можно было получать температуры до 3000 °С. При этом смесь порошкообразного алюминия и оксида железа доводилась до накаливания в присутствии смеси ВаО 2+ Mg, которая играла роль "запала". Благодаря высокой температуре, возникающей при взаимодействии Fe 3O 4и алюминия, железо выделялось в раскаленном добела (расплавленном) состоянии. Этот метод использовался при сварке железных изделий, а также (в случае других исходных оксидов) для получения трудно восстанавливаемых металлов.

Прибор Э. Резерфорда для расщепления атомных ядер (1919 г.)
Рентгеновские лучи, проходящие сквозь светонепроницаемые вещества, вызывающие флуоресценцию веществ и почернение фотопластинок, стали важным инструментом исследований. Природа рентгеновских лучей была установлена в 1912 г. Максом Лауэ, который обнаружил дифракцию этих лучей кристаллами. Рентгеновские лучи подобны световым, но с длиной волны, примерно в 5000 раз меньшей, чем у лучей видимой части спектра. По дифракции рентгеновских лучей были определены длины волн рентгеновского спектра для различных элементов и установлено расположение атомов в кристаллах. Тем самым были заложены основы структурной химии. Используя этот метод, английские физики Уильям Брэгг и его сын Лоуренс определили структуры примерно 20 кристаллических соединений. Кроме того, они определили длины волн рентгеновского излучения.
В конце XIX в. открытие радиоактивности тоже дало в руки химиков новый метод исследования [100]. Несложное устройство (сильный магнит и свинцовая камера с отверстиями, в которой находился радий) позволило П. Виллару и Э. Резерфорду доказать, что радий испускает лучи трех различных видов: α, β и γ. Облучая потоком α-частиц тонкую металлическую фольгу, Резерфорд установил, что α-частицы представляют собой ядра атомов гелия [101].
В 1897 г. Дж.Дж. Томсон сконструировал прибор, с помощью которого он, исследуя отклонения катодных лучей в магнитном и электрическом полях, показал, что они представляют собой поток отрицательно заряженных частиц, измерил удельный заряд этих частиц и нашел, что их масса приблизительно в 1837 раз меньше массы атома водорода.
Читать дальшеИнтервал:
Закладка:


![Жорж Вигарелло - История тела Том 2 [От Великой французской революции до Первой мировой войны]](/books/1081096/zhorzh-vigarello-istoriya-tela-tom-2-ot-velikoj-fran.webp)







