Михаил Супотницкий - Микроорганизмы, токсины и эпидемии
- Название:Микроорганизмы, токсины и эпидемии
- Автор:
- Жанр:
- Издательство:Вузовская книга
- Год:2006
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Супотницкий - Микроорганизмы, токсины и эпидемии краткое содержание
Кроме того, в монографии, впервые для отечественной литературы, обстоятельно освещены эпидемиология биологического террористического акта и методология выявления такого преступления. Книга хорошо иллюстрирована, содержит приложения и рассчитана на широкий круг специалистов.
Микроорганизмы, токсины и эпидемии - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Обычно обе цепи РНК в ретровирусной частице являются производными от одного родительского провируса. Однако если инфицированная клетка одновременно содержит два различных провируса, то их РНК-транскрипты могут сформировать отдельный гетерозиготный вирион. После проникновения в новую клетку, под действием обратной транскриптазы, заново синтезированная ретровирусная последовательность будет рекомбинантом двух родительских. Сходство с половым процессом здесь в том, что:
1) обе цепи РНК как две родительские гаметы сливаются в одну;
2) генетическая информация потомков будет рекомбинантной
3) последующие «поколения» будут нести информацию обоих родителей [Temin Н., 1991].
«Половой процесс» дает ВИЧ ряд существенных преимуществ перед другими РНК-вирусами. Легко возникающие мутации, способствуют отбору и закреплению вариантов РНК-вируса, наиболее «удачно» использующих данного хозяина. Но для любого микроорганизма, который достиг пика на «ландшафте приспособленности», новая мутация не создает однозначных преимуществ. Более того, для него это ступенька на нижний уровень приспособленности. Генетическая рекомбинация может создать условия для регенерации геномов более «удачливых» ретровирусов из предковых геномов вирусов, менее адаптированных из-за мутаций. Однако, при смене условий существования такая консервация на высоте адаптивного пика превращается для вируса в ловушку. Рекомбинация между РНК-геномами двух высокоадаптированных ВИЧ, дает возможность рекомбинанту «сесть» на другой адаптивный пик, более соответствующий изменившимся условиям. Т. е., как заметил S. Kaufman (1993), помочь ему совершить «эволюционно широкий прыжок».
Сравнение патогенезов. Патогенез ВНО определяется необходимостью его быстрого размножения до количеств, позволяющих смену хозяина в течение короткого промежутка времени — от момента его инфицирования до его гибели или выздоровления. Выздоровление — это процесс разрешения от инфекции, осуществляемый иммунной системой хозяина.
ВНО variola maior обуславливает генерализованную инфекцию, которая в высоком проценте случаев завершается летальным исходом. Для этого вирус располагает беспрецедентным, по сравнению с вирусами других семейств, набором генов, белковые продукты которых эффективно изменяют многочисленные защитные реакции организма (рис. 29).
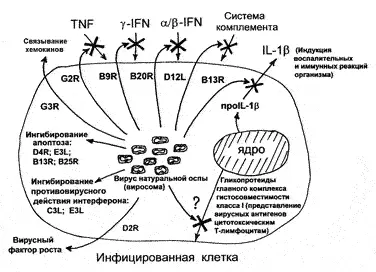
Рис. 29. Общая схема синтеза ВНО молекулярных факторов, обеспечивающих вирусу преодоление защитных барьеров человека. Вирус располагает беспрецедентным, по сравнению с вирусами других семейств, набором генов, белковые продукты которых эффективно изменяют многочисленные защитные реакции организма [Маренникова С.С., Щелкунов С.Н., 1998]
Первым неспецифическим и, возможно, самым древним барьером, который вынужден преодолевать ВНО, является программированная гибель клеток (апоптоз). Инфицирование клетки запускает механизм ее самоубийства, благодаря чему предотвращается размножение вируса и его распространение среди соседних клеток. ВНО располагает, по крайней мере, четырьмя генами, белковые продукты которых ингибируют апоптоз по альтернативным и дублирующим механизмам [Маренникова С.С., Щелкунов С.Н., 1998].
Вторым неспецифическим барьером являются местные воспалительные процессы. Они быстро индуцируются для ограничения распространения вируса в первые часы и дни после инфицирования, пока формируется полноценный иммунный ответ. ВНО несет гены не менее чем пяти белков, блокирующих различные этапы развития воспаления в участках размножения вируса (SPI-2, G3R, растворимых аналогов рецепторов фактора некроза опухолей — TNF и гамма-интерферона — гаммаlFN) и предотвращающих развитие системных реакций (растворимый рецептор интерлейкина-1бета — IL-1 бета). Как правило, все эти белки обладают одновременно несколькими активностями. Например, TNF-связывающий белок необходим еще и для развития генерализованной инфекции, столь характерной для ВНО. Поэтому эти белки считаются факторами вирулентности ВНО [Маренникова С.С., Щелкунов С.Н., 1998].
Система блокирования интерферона у ВНО также мультигенна (не менее 5 белков), поэтому он очень устойчив к его действию. Синтезируемые вирусом аналоги растворимых рецепторов IFN обоих типов, интерферируют с IFN, связывая его клеточные рецепторы. Это приводит к блокированию антивирусного состояния клетки и предотвращает лейкоцитарную инфильтрацию в участки вирусной репликации [Alcami A., Smith G., 1996].
Для облегчения распространения ВНО по тканям организма хозяина, в его геноме содержится ген C11R VAC–COP, кодирующий белок VGF, отнесенный к семейству эпидермального фактора роста. Он стимулирует рост и/или метаболическую активность неинфицированных клеток, обеспечивая тем самым распространение ВНО по организму. На эффективность диссеминации ВНО в организме человека также влияют белки оболочки внеклеточных вирионов (прежде всего, гемагглютинин) и анкиринподобные белки (определяют круг хозяев вируса). Пока не идентифицированы вирусные белки, подавляющие созревание гликопротеидов главного комплекса гастосовместимости класса I и тем самым снижающих эффективность представления на поверхности инфицированной клетки вирусных антигенов специфическим цитотоксическим Т-лимфоцитам [Маренникова С.С., Щелкунов С.Н., 1998].
Однако большое количество синтезируемых ВНО белковых структур неизбежно обнаруживаются иммунной системой хозяина, Поэтому патогенез ВНО построен на компромиссе между скоростью развития иммунного ответа хозяина (индуцируется полный спектр клеточно-опосредованных и гуморальных иммунных ответных реакций) и скоростью размножения вируса до количеств, достаточных для его передачи другому реципиенту. Например, ранее всех появляющиеся антигемагглютинины (2–3 день болезни), достигают своего максимума между 12 и 15 днями, а максимальные титры вируса в зеве определяются на 3-й и 4-й дни и держатся до 8-го дня у 95–100 % больных. Затем они начинают снижаться [Маренникова С.С., Щелкунов С.Н., 1998]. У переболевших оспа оставляет длительный, стойкий и стерильный иммунитет, что исключает возможность повторного использования вирусом для своего размножения того же хозяина. Эта та цена, которую вирус платит за сложность своего генома иммунной системе человека. Однако заболевший успевает инфицировать от 5 (в среднем) до 38 человек, из них не менее трети погибнет — это уже цена, которую платим мы за тоже самое (рис. 30).
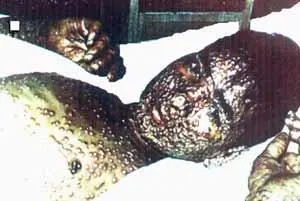
Рис. 30. Внешний вид больного натуральной оспой. Оспенные папулы. Возбудитель максимально накапливается на ранней стадии инфекции, стремясь успеть сменить хозяина до развития у него иммунитета. Используемый ВНО воздушно-капельный механизм передачи позволяет одному больному инфицировать десятки людей. Но эта цепочка рано или поздно прервется либо из-за гибели инфицированных либо из-за приобретения иммунитета чувствительной популяцией. Рисунок из книги Е.П. Шуваловой (1974)
Читать дальшеИнтервал:
Закладка:






![Михаил Супотницкий - Очерки истории чумы. Книга II. Чума бактериологического периода [без иллюстраций]](/books/1084186/mihail-supotnickij-ocherki-istorii-chumy-kniga-ii.webp)
![Михаил Супотницкий - Очерки истории чумы. Книга I. Чума добактериологического периода [без иллюстраций]](/books/1084187/mihail-supotnickij-ocherki-istorii-chumy-kniga-i-ch.webp)


