Нурбей Гулиа - Удивительная механика
- Название:Удивительная механика
- Автор:
- Жанр:
- Издательство:НЦ ЭНАС
- Год:2006
- Город:Москва
- ISBN:5-93196-591-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Нурбей Гулиа - Удивительная механика краткое содержание
Нурбей Владимирович Гулиа – профессор, доктор технических наук, рассказывает в своей книге о работе над созданием эффективного накопителя энергии – «энергетической капсулы», которая позволила бы действительно по-хозяйски, бережно использовать энергию, даваемую нам природой. Книга должна помочь молодому читателю найти свой путь самореализации в изобретательском творчестве, без которого невозможно решение ни одной научно-технической задачи, тем более в таких важных областях экономики, как энергетика и транспорт.
Удивительная механика - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Так или иначе, огромная заслуга Вольты состоит в том, что он не только построил гальванический элемент, но и объяснил его действие, чего по вполне понятным причинам не могли сделать древние.
Элемент Вольты давал очень маленькое напряжение. Чтобы повысить его, стали изготавливать батареи из медных и цинковых пластин, переложенных прокладками, смоченными серной кислотой. Батареи эти, названные вольтовыми столбами, обеспечивали уже достаточно большое напряжение. После Вольты немало ученых – Жорж Лекланше, Якоб Даниэль, Вильям Грове и
Угольный электрод

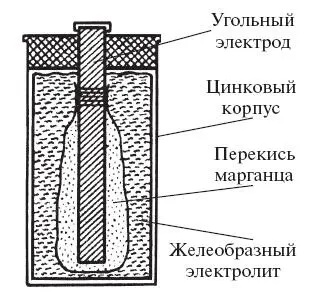
Лекланше, твердые – цинковый стаканчик и графитовый стержень. А вот электролит уже не жидкий. Ведь жидкость может в любой момент пролиться, а делать элемент герметичным дорого и сложно. Вот и заменили жидкость желеобразным электролитом. Получился удобный и практичный источник электричества.
Если через разряженную сухую батарею особыми импульсами пропустить ток, ее можно вновь «оживить». Эту операцию порой проделывают по несколько раз. Однако она ненадолго восстанавливает элемент.
Постойте-постойте… Как бы там ни было, получается, что гальванический элемент – тот же аккумулятор! Заряжая его электрическим током, восстанавливая, мы накапливаем в нем электроэнергию, которую затем расходуем. Так ли это?
Оказывается, и так и не так. Прежде всего, не каждый гальванический элемент можно подзарядить. Нельзя это сделать, например с элементом, который состоит из двух электролитов. Таков элемент Даниэля, где две разные жидкости разделены пористым стаканчиком. Постепенно просачиваясь через стаканчик, электролиты смешиваются, реагируют друг с другом и выделяют ток. Этот элемент, если он уже отработал свой срок, не восстановишь.
Другие элементы с твердыми электродами в принципе подзаряжаются, накапливают энергию. Но процесс накопления столь неэкономичен и неэффективен, что многие считают подзарядку таких элементов неоправданной. Накапливается только ничтожная часть поданной на элемент электроэнергии, а сам элемент после нескольких таких зарядок разрушается. Чтобы стать хорошим накопителем, гальванический элемент должен достаточно хорошо «переносить» процесс зарядки. И этого наконец удалось добиться в середине XIX века.
В 1859 году французский ученый и инженер Гастон Планте провел любопытный опыт, внешне очень похожий на опыт Вольты. Как и Вольта, Планте построил гальванический элемент, однако в качестве электродов он взял две свинцовые пластины, в обычных условиях покрытые пленкой окиси свинца. Электролит был все тот же – разбавленная серная кислота. Планте подключил к электродам источник постоянного тока и некоторое время пропускал ток через свой элемент, совсем как при подзарядке сухих элементов. Потом он отключил ток и подключил к электродам гальванометр. Прибор показал, что гальванический элемент сам стал вырабатывать электроток и при этом выделять почти всю энергию, затраченную на его зарядку. Зарядку можно было повторять много раз: элемент неизменно работал исправно и не разрушался, подобно сухим батареям.
Этот гальванический элемент назвали элементом второго рода, или аккумулятором.
Как же происходит накопление энергии в аккумуляторе Планте? При пропускании тока через электролит из серной кислоты на свинцовой пластине, соединенной с отрицательным полюсом источника тока – катодом, – выделяется водород, который восстанавливает окись свинца в чистый свинец. На электроде, соединенном с положительным полюсом – анодом, – выделяется кислород, который окисляет окись свинца до перекиси. Аккумулятор зарядится в тот момент, когда катод целиком станет чистым свинцом, а анод – перекисью свинца. Тогда между электродами окажется наибольшее напряжение.
Соединяя пластины-электроды проводником с потребителем, расходуя энергию, мы разряжаем аккумулятор. Направление тока при разрядке противоположно тому, что было при зарядке. Положительно заряженная пластина будет восстанавливаться водородом, а отрицательная – окисляться кислородом. Как только пластины станут одинаковыми, аккумулятор прекратит давать ток. Надо повторить зарядку.
Ясно, что энергия в таком аккумуляторе накапливается не в виде электрического или магнитного поля, как в предыдущих накопителях электрической энергии, а в виде вполне осязаемого вещества – свинца, переходящего с выделением энергии в перекись свинца. Сам процесс накопления и выделения энергии здесь происходит иначе, нежели в чисто электрических аккумуляторах – конденсаторах и электромагнитах. Поэтому такой аккумулятор принято называть электрохимическим.
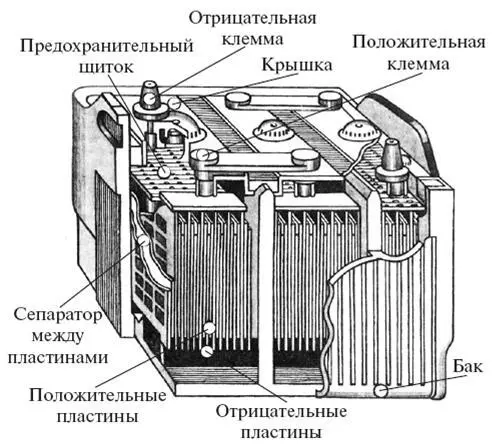
В конструкциях автомобильных свинцово-кислотных аккумуляторов ученые постарались как можно больше увеличить поверхность электродов, не нарушая при этом их прочности. Ведь именно от величины поверхности зависит энергоемкость аккумулятора. Сейчас пластины аккумулятора изготовляют в форме свинцовых решеток, покрытых перекисью свинца (положительный электрод) и губчатым свинцом (отрицательный электрод). Электролитом служит 25—35%-ный водный раствор серной кислоты. Заряженный автомобильный аккумулятор имеет напряжение (точнее, электродвижущую силу) на клеммах 2-2,2 В. При разрядке это напряжение падает, и когда оно достигает 1,8 В, разрядку обычно прекращают, иначе решетка из свинца может слишком истончиться в ходе реакции, и пластины, потеряв прочность, рассыплются.
Мне очень хотелось узнать, что будет с аккумулятором, если попробовать хотя бы кратковременно получить от него ток большой мощности. Однажды я упросил одного знакомого водителя включить стартер, питаемый, как известно, от аккумулятора, при не включенном двигателе. Двигатель, естественно, не завелся, а секунд через 15—20 стартер начал сбавлять обороты. Еще через некоторое время он вообще остановился. Было полное впечатление, что аккумулятор разрядился и больше из него «выжать» ничего нельзя. Я думал, водитель рассердится, скажет, мол, видишь, к чему привели твои опыты. Но он неторопливо выключил стартер, а потом, спустя пару минут, снова включил его. Стартер заработал! Откуда взялись «силы» у аккумулятора? Не мог же он, как живое существо, «отдохнуть»!
Читать дальшеИнтервал:
Закладка:






