Елена Хохрякова - Современные методы обеззараживания воды
- Название:Современные методы обеззараживания воды
- Автор:
- Жанр:
- Издательство:Литагент «Аква-Терм»9c582a94-26cf-11e4-a844-0025905a069a
- Год:2014
- Город:Москва
- ISBN:978-5-905024-22-1
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Елена Хохрякова - Современные методы обеззараживания воды краткое содержание
Микробиологические загрязнения воды занимают первое место по степени риска для здоровья человека. Поэтому обеззараживание воды является обязательным условием достижения ее питьевого качества по установленным гигиеническим нормативам. В издании даны основные сведения о современных методах обеззараживания питьевой воды; краткая характеристика каждого метода, его аппаратурного оформления и возможности применения в практике централизованного и индивидуального водоснабжения. В брошюре также изложены начальные сведения по основным источникам водопользования и пригодности их для питьевых целей. Приведены нормативные документы, регламентирующие водно-санитарное законодательство, сравнительный обзор нормативных документов, регламентирующих качество питьевой воды в части обеззараживания, принятых в России и за рубежом.
Современные методы обеззараживания воды - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Cl 2+ 2NaOH = NaClO + NaCl + H 2O
или электрохимическим методом по реакции:
NaCl + H 2O = NaClO + H 2.
Вещество гипохлорит натрия (NaClO) в чистом химическом виде (т. е. без воды) представляет собой бесцветное кристаллическое вещество, легко разлагающееся на хлорид натрия (поваренная соль) и кислород:
2NaClO = 2NaCl + O 2.
При растворении в воде, гипохлорит натрия диссоциирует на ионы:
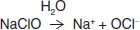
Гипохлорит-ион OCl -в воде подвергается гидролизу, образуя хлорноватистую кислоту HOCl:
ОCl -+ H 2O = HOCl + OH -.
Именно наличие хлорноватистой кислоты в водных растворах гипохлорита натрия объясняет его сильные дезинфицирующие и отбеливающие свойства. Наивысшая бактерицидная способность гипохлорита проявляется в нейтральной среде, когда концентрации HClO и гипохлорит-анионов ClO -приблизительно равны.
Разложение гипохлорита сопровождается образованием ряда активных частиц, в частности, атомарного кислорода, обладающего высоким биоцидным действием. Образующиеся частицы принимают участие в уничтожении микроорганизмов, взаимодействуя с биополимерами в их структуре, способными к окислению. Исследованиями установлено, этот процесс аналогичен тому, который происходит естественным образом во всех высших организмах. Некоторые клетки человека (нейтрофилы, гепатоциты и др.) синтезируют хлорноватистую кислоту и сопутствующие высокоактивные радикалы для борьбы с микроорганизмами и чужеродными субстанциям.

Обеззараживание воды и окисление примесей с использованием гипохлорита натрия, производимого электрохимически, впервые было применено в США в конце 30-х гг. XX в… Гипохлорит натрия обладает рядом ценных свойств. Его водные растворы не имеют взвесей и поэтому не нуждаются в отстаивании в противоположность хлорной извести. Применение гипохлорита натрия для обработки воды не вызывает увеличения ее жесткости, поскольку не содержит солей кальция и магния как хлорная известь или гипохлорит кальция.
Бактерицидный эффект раствора NaClO, полученного электролизом, выше, чем у других дезинфектантов, действующее начало которых – активный хлор. Кроме того, раствор обладает еще большим окислительным действием, чем растворы, приготовленные химическим методом, поскольку содержит больше хлорноватистой кислоты (HClO).
Недостатком данного метода является то, что водные растворы гипохлорита натрия неустойчивы и со временем разлагаются даже при комнатной температуре.
Промышленностью нашей страны гипохлорит натрия выпускается в виде водных растворов различной концентрации.
В соответствии с ГОСТ 11086-76 раствор гипохлорита натрия, получаемый по химическому методу, выпускается в виде трех марок. Ниже приведены показатели по составу продуктов.

Гипохлорит натрия в виде раствора (марки А, Б или «Белизна») – это раствор гипохлорита (16–19 % NaOCl) с примесью хлорида и гидроксида натрия (рН 12–14). Оба раствора со временем разлагаются. Скорость разложения зависит от условий их хранения.
Раствор гипохлорита натрия реагент легко дозируется, что позволяет автоматизировать процесс обеззараживания воды.

4.2.4. Хлорсодержащие реагенты
Использование для обеззараживания воды хлорсодержащих реагентов (хлорной извести, гипохлоритов натрия и кальция) менее опасно в обслуживании, чем применение хлора и не требует сложных технологических решений. Правда, применяемое при этом реагентное хозяйство более громоздко, что связано с необходимостью хранения больших количеств препаратов (в 3–5 раз больше, чем при использовании хлора). Во столько же раз увеличивается объем перевозок.
При хранении происходит частичное разложение реагентов с уменьшением содержания хлора. В связи с этим необходимо обустраивать систему притяжно-вытяжной вентиляции и соблюдать меры безопасности для обслуживающего персонала. Растворы хлорсодержаших реагентов коррозионно-активны и требуют оборудования и трубопроводов из нержавеющих материалов или с антикоррозийным покрытием, при индивидуальном водоснабжении обычно не используются.

4.2.5. Хлорирование для индивидуального водоснабжения
Все большее распространение, особенно на небольших станциях водоподготовки, получают установки по производству активных хлорсодержаших реагентов электрохимическими методами.
В России несколько предприятий предлагают установки типа «Санер», «Санатор», «Хлорэл-200» для производства гипохлорита натрия методом диафрагменного электролиза поваренной соли.

Наиболее просто и часто вопросы хлорирования воды для индивидуального водоснабжения решаются применением гипохлорита натрия, в качестве реагента возможно применение раствора «Белизна».
Многим потребителям не нравится то, что льющаяся из крана вода может иметь запах хлора, однако эта проблема легко решается посредством установки угольного фильтра.
Методы подготовки воды хлорированием требуют точного дозирования реагентов в обрабатываемую воду, поскольку реагенты отличаются высокой химической активностью. Для решения задач хлорирования нужно применять современную цифровую технику, обеспечивающую точное дозирование реагента пропорционально расходу или объему обрабатываемой воды.
На рынке представлено большое разнообразие дозирующих насосов, различающихся производительностью.

4.3. Другие галогены для обеззараживания воды
4.3.1. Йодирование
Йод – химический элемент из группы галогенов, «родственниками» которого являются фтор, хлор и бром, обозначается символом I (от греч. iodes – фиолетовый; лат Iodum), имеет порядковый номер 53, атомный – 126,90, плотность твердого – 4,94 г/см 3, температура плавления – 113,5 °С, кипения – 184,35 °С. В природе йод в основном сосредоточен в морской воде (в среднем около 0,05 мг/л). Кроме того, он есть и в морских отложениях. Это позволяет ему переходить в подземные воды, в которых его содержание может достигать более 100 мг/л. Столь высокое содержание йода характерно также для районов нефтяных месторождений. В то же время в поверхностных водах его содержание невелико (концентрация колеблется от 1 до 0,01 мкг/л).
Читать дальшеИнтервал:
Закладка:










