Михаил Никитин - Происхождение жизни. От туманности до клетки
- Название:Происхождение жизни. От туманности до клетки
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2016
- Город:Москва
- ISBN:978-5-9614-4350-9
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Никитин - Происхождение жизни. От туманности до клетки краткое содержание
Происхождение жизни. От туманности до клетки - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
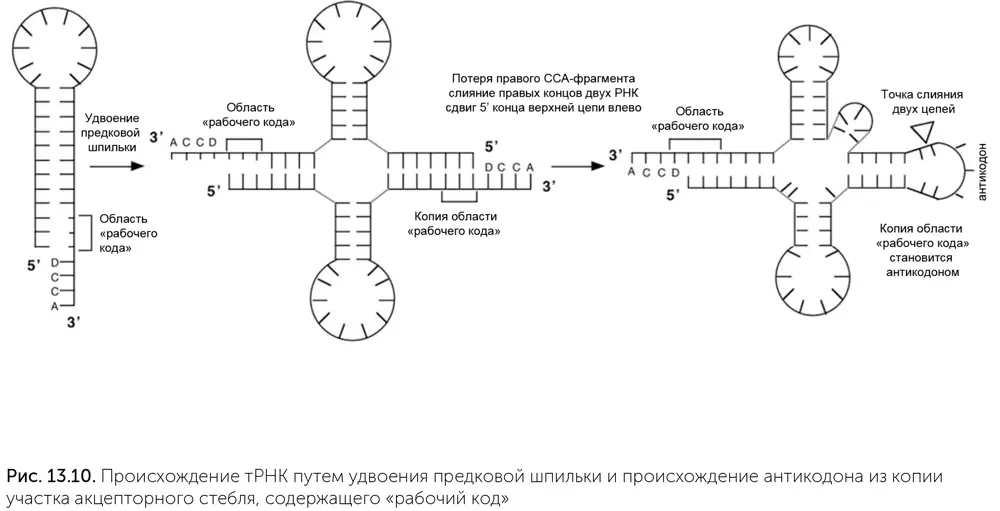
Порядок развития белкового синтеза и генетическом кода
Мы рассмотрели ключевые факты, проливающие свет на историю рибосом и генетического кода. Попробуем теперь собрать из фрагментов последовательную историю.
1. Основа большой субъединицы рибосомы, пептидил-трансферазный центр, вначале строил пептиды из небольшого набора аминокислот без участия матричной РНК. Возможны три варианта последовательности таких пептидов: чистые полимеры одной аминокислоты, случайное чередование нескольких аминокислот и закономерное чередование, в простейшем случае повтор двух аминокислот. Наличие двух классов аминоацил-тРНК-синтетаз, узнавание ими тРНК с разных сторон и неслучайная принадлежность аминокислот двум классам синтетаз в древних белках могут быть следами двухаминокислотных повторов на этом этапе развития рибосомы. Аминокислоты доставлялись к проторибосоме на молекулах транспортных РНК. Но эти тРНК были меньше и проще современных и имели один длинный двуспиральный участок (современные – четыре коротких). «Рабочий код» (последовательность трех первых нуклеотидов акцепторного стебля) мог использоваться дважды. Сначала вне рибосомы он опознавался рибозимными аминоацил-тРНК-синтетазами для прикрепления каждой аминокислоты к своей тРНК. Затем уже в проторибосоме он мог использоваться для правильного чередования аминокислот в периодических пептидах.
2. В какой-то момент происходит внутренняя дупликация в молекулах транспортных РНК, и они превращаются из древних одиночных шпилек в современные «трилистники». Образуется антикодоновая петля как копия участка акцепторного стебля с «рабочим кодом», и взаимодействие этой петли с другими молекулами РНК позволяет упорядочить последовательность пептидов, производимых на древней рибосоме. Вероятно, сначала антикодоновые петли взаимодействовали со специальным участком рибосомной РНК, а потом ему на смену пришли сменные матричные РНК, позволив одной рибосоме производить множество разных белков. К большой субъединице рибосомы присоединилась малая и стала контролировать взаимодействие транспортной и матричной РНК.
3. Мы можем восстановить набор аминокислот, используемых проторибосомой на этих двух этапах, по двум источникам: совпадение «рабочего кода» в акцепторном стебле транспортной РНК со стандартным кодом в антикодоновой петле той же тРНК и присутствие аминокислоты в составе древнейших белков (внутренние домены рибосомных белков L2, L3, L4, L22). «Рабочий код» дает нам пять аминокислот (глицин, аланин, пролин, аспарагиновая кислота, валин), рибосомные белки – тоже пять, но других (глицин, аланин, пролин и вместо аспарагиновой кислоты и валина – аргинин и лизин). Выше мы упоминали, что в древнейшем генетическом коде вместо аргинина и лизина, скорее всего, были их более простые аналоги, такие как орнитин, диаминопропионовая и диаминобутановая кислоты. Далее для краткости мы будем называть только орнитин, но на самом деле это могла быть любая из этих трех аминокислот или даже могли быть задействованы все три одновременно. Совпадение «рабочего кода» с обычным антикодоном для них могло быть стерто позже, когда эти аминокислоты были заменены на лизин и аргинин. Иными словами, в минимальный набор аминокислот, с которого начался кодируемый синтез белка, входят шесть: глицин, аланин, пролин, аспарагиновая кислота, валин, орнитин. Скорее всего, эти же шесть аминокислот использовались и на первом этапе развития рибосомы, до внутренней дупликации тРНК и появления кода. На этом первом этапе из шести древнейших аминокислот могли строиться вспомогательные пептиды для разных рибозимов. Это могли быть пептиды с положительным зарядом, стабилизирующие укладку рибозимов, на основе чередования орнитина с аланином, глицином или пролином. Кроме того, могли производиться и пептиды с отрицательным зарядом для работы в составе рибозимов-полимераз на основе чередования аспарагиновой кислоты, валина и глицина.
4. Переход к кодированию последовательностей пептидов при помощи матричной РНК дал возможность строить более длинные и воспроизводимые вспомогательные пептиды для разных рибозимов, а затем и полноценные белки, способные компактно свернуться без участия РНК. На этом этапе возникают первые рибосомные белки и первые ферменты, состоящие из бета-слоев, в том числе аминоацил-тРНК-синтетазы.
5. Добавление к аминокислотному набору цистеина, серина и гистидина резко расширяет каталитические возможности белков. Появляются многие основные классы ферментов. Разнообразие белков растет, и все сильнее проявляется врожденный недостаток белков с бета-слоевой укладкой: они склонны соединяться в кристаллоподобные структуры. Известный пример такой кристаллизации бета-слоевого белка – образование амилоидных фибрилл в нервных клетках при болезни Альцгеймера. Толчком к появлению таких кристаллов может стать как неожиданное изменение температуры и солевого состава среды, так и мутация в гене, кодирующем этот белок. По этой причине естественный отбор поддерживает появление белковых структур, состоящих из альфа-спиралей.
6. Для появления белков со стабильной альфа-спиральной укладкой необходимо найти замену орнитину, валину и аспарагиновой кислоте, так как они нарушают устойчивость альфа-спиралей. Добавление в код лейцина, изолейцина, лизина либо аргинина, а также глутаминовой кислоты решает эту проблему. На этом этапе могла возникнуть большая часть универсальных белковых укладок.
7. Завершение стандартного генетического кода. Добавляются ароматические аминокислоты, аспарагин, глутамин. Ароматические аминокислоты могут вступать во взаимодействие с азотистыми основаниями в РНК и коферментах и дают новый способ связывания белков с РНК – это так называемое стэкинг-взаимодействие, основанное на параллельном расположении ароматических колец пуриновых и пиримидиновых оснований. Фенилаланин, кроме того, является самой крупной из гидрофобных аминокислот и повышает стабильность укладки больших белков. Позднее добавление аспарагина и глутамина связано с их плохой устойчивостью к высоким температурам. В белках гипертермофильных микробов, живущих при температуре 90–110 °C, содержание аспарагина и глутамина очень мало. Видимо, они вошли в генетический код после выхода протоклеток из горячих геотермальных водоемов в моря.
Как мы видим, сложнейшая система производства белков вполне могла развиваться постепенно. Многие ее компоненты, такие как транспортные РНК и рибосомная РНК малой субъединицы, исходно имели другие функции, не связанные с белками. Проторибосома, собирающая короткие пептиды без кода, тоже могла быть полезна для организмов РНК-мира. Появление генетического кода и матричных РНК повысило точность и воспроизводимость этих коротких пептидов. После этого дальнейшее совершенствование рибосомы и расширение набора аминокислот поддерживались естественным отбором в первую очередь потому, что позволяли получать новые, более эффективные белковые ферменты.
Читать дальшеИнтервал:
Закладка:







