Сергей Титов - Естествознание. Базовый уровень. 10 класс
- Название:Естествознание. Базовый уровень. 10 класс
- Автор:
- Жанр:
- Издательство:Array Литагент «Дрофа»
- Год:2013
- Город:Москва
- ISBN:978-5-358-13589-5
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Сергей Титов - Естествознание. Базовый уровень. 10 класс краткое содержание
Учебник объединяет сведения об основных законах и закономерностях, наиболее важных открытиях и достижениях в области химии, физики, астрономии, что формирует у учащихся представление о природе как целостной системе, а также о взаимосвязи человека, природы и общества.
Современное оформление, многоуровневые вопросы и задания, дополнительная информация и возможность параллельной работы с электронным приложением способствуют эффективному усвоению учебного материала.
Учебник адресован учащимся 10 класса.
Естествознание. Базовый уровень. 10 класс - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Масса атома определяется главным образом массой его ядра, которое состоит из двух видов частиц, называемых нуклонами (от лат. nucleus – ядро), имеющих почти одинаковую массу. Нуклоны бывают двух видов: положительно заряженные протоны и нейтральные нейтроны.
Вид атома с определённым зарядом ядра называют химическим элементом. Атом каждого элемента отличается от других числом протонов в атомном ядре, которое соответствует его порядковому номеру в Периодической системе элементов Д. И. Менделеева и числу электронов в электронной оболочке. Кроме того, число протонов определяет электрический заряд ядра, так как электрически нейтральные нейтроны не вносят в него вклада. Поэтому число протонов в ядре какого-либо атома называют его зарядовым числом. Самое простое строение имеет атом водорода. Он состоит всего из одного протона и одного электрона. Другие элементы обязательно имеют в составе своего ядра нейтроны. Так, ядро атома гелия состоит из двух протонов и двух нейтронов.
Масса ядра определяется суммой масс составляющих его протонов и нейтронов и называется атомной массой. Поскольку масса атомов очень мала, её неудобно измерять непосредственно в граммах. Поэтому в практических целях используют величину, называемую массовым числом, которая равна числу всех входящих в ядро нуклонов. Масса одного протона или нейтрона, таким образом, принимается за единицу.
Может показаться, что каждый химический элемент должен всегда иметь определённое зарядовое число и определённую атомную массу. Однако это утверждение верно только в отношении зарядового числа. Ещё в начале XX в. было обнаружено, что некоторые элементы, проявляющие одинаковые свойства в химических реакциях, состоят из атомов, имеющих различную атомную массу. Атомы одного и того же элемента, имеющие различную массу, были названы изотопами. Встречающиеся в природе элементы чаще всего являются смесью нескольких изотопов, один из которых является преобладающим. Атомы всех изотопов одного элемента имеют одинаковый заряд ядра и, соответственно, занимают одно и то же место в периодической системе химических элементов. Различие между ними заключается в числе содержащихся в ядре нейтронов.
Ядро атома гелия чаще всего содержит два нейтрона, но встречаются изотопы, число нейтронов в ядре которых равно одному или трём. Кислород в природе может существовать в виде трёх изотопов с восемью, девятью или десятью нейтронами. При этом число протонов в ядре атома кислорода и, следовательно, его зарядовое число и атомный номер всегда равны восьми. Водород является первым элементом периодической системы элементов. Ядро его атома содержит всего один протон и чаще всего вообще не содержит нейтронов. Такой изотоп водорода называют протий. Однако в природном водороде содержится почти 0,02 % изотопа, называемого дейтерием и содержащего один нейтрон (рис. 115, А). Соответственно, атомная масса дейтерия равна двум.
Рассмотренные изотопы гелия, кислорода и водорода называют стабильными, так как они устойчивы и не подвергаются самопроизвольному распаду. К настоящему времени в природе обнаружено 270 стабильных изотопов. Кроме них существуют и нестабильные изотопы, ядро которых неустойчиво и подвержено постоянному распаду. Эти изотопы чаще всего встречаются у тяжёлых элементов, т. е. элементов с большой атомной массой. Нестабильные изотопы часто получают искусственно при помощи ядерных реакций. Таким способом можно получить, например, нестабильный изотоп водорода, в ядре которого находятся два нейтрона. Этот изотоп водорода называется тритием из-за того, что его атомная масса равна трём (один протон плюс два нейтрона) (см. рис. 115, А).
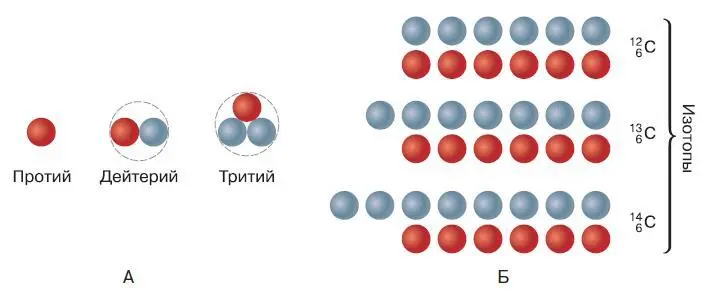
Рис. 115. Состав атомных ядер: А – водорода; Б – углерода (красные шарики – протоны, голубые – нейтроны)
Большинство природных химических элементов существуют в виде нескольких устойчивых изотопов (рис. 115, Б). Например, железо имеет четыре стабильных изотопа, ртуть – семь, а олово – десять. Поэтому атомная масса элементов выражается дробным числом. Так, хлор, встречающийся в природе, на 76,5 % состоит из изотопа с атомной массой, равной 35, и на 24,5 % – из изотопа с массой 37. Поэтому средняя атомная масса хлора равна приблизительно 35,5.
Как следует из самого названия, нестабильные изотопы не могут существовать в течение неограниченного периода времени и постоянно распадаются. Скорость распада ядер этих изотопов измеряется их периодом полураспада – временем, за которое первоначальное количество частиц уменьшается вдвое. У большинства нестабильных изотопов этот период составляет не более нескольких секунд, хотя известны изотопы с периодом полураспада в миллионы лет. Во время распада ядра таких атомов испускают радиоактивное излучение. Таким образом, можно сказать, что все неустойчивые изотопы обладают радиоактивностью (рис. 116).
Химические свойства элементов, т. е. их способность вступать в химические реакции, не зависят от числа нейтронов в ядре атома, а связаны со строением его электронной оболочки. Поэтому в химическом отношении все изотопы одного элемента являются абсолютно одинаковыми. Эту особенность используют во многих областях науки, техники и медицины. Таким образом можно, например, судить о превращениях какого-либо химического вещества в организме и о местах его включения в клетки и ткани. Можно синтезировать биологически активное вещество, включив в него неустойчивый радиоактивный изотоп какого-либо атома, например углерода или азота. В химическом и биологическом отношении это вещество ничем не будет отличаться от такого же вещества, не содержащего радиоактивного изотопа. В какие бы другие соединения это вещество ни превращалось, как бы ни изменялось строение его молекулы, радиоактивное излучение нестабильного атома всегда будет сохраняться. Если затем ввести это вещество в кровь, то, измеряя испускаемое этим изотопом слабое, безопасное для организма, радиоактивное излучение в различных участках человеческого тела, можно судить о том, где и в каких количествах накапливается в организме это вещество или продукты его обмена. Постепенно эти продукты или само вещество будут выводиться из организма, и по уменьшению радиоактивности можно определить скорость их выведения. Такой метод получил название исследования с применением «меченых атомов».

Рис. 116. Радиоактивный металл кюрий светится в темноте, испуская большое количество ядер гелия
Читать дальшеИнтервал:
Закладка:










