Фрадкин Захарович - Белые пятна безбрежного океана
- Название:Белые пятна безбрежного океана
- Автор:
- Жанр:
- Издательство:Недра
- Год:1983
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Фрадкин Захарович - Белые пятна безбрежного океана краткое содержание
В книге рассказывается о воде - самом распространенном и в то же время самом загадочном веществе на Земле. Приведены гипотезы, объясняющие происхождение воды на планете, раскрывается роль воды в формировании атмосферы, океанов, климата и как движителя научно-технического прогресса на протяжении всей истории человечества.
Белые пятна безбрежного океана - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
У каждой молекулы Н 2О два "голых" водородных протона, поэтому она захватывает сразу двух оказавшихся поблизости "соседок". Но одновременно на ее собственный атом кислорода будут переброшены два "багра" с других не менее расторопных протонов.
Так, быть может несколько упрощенно, мы с возможной наглядностью нарисовали картину возникновения кристаллической структуры льда - возникновение тетраэдров, которые начнут выстраиваться один за другим, как солдаты на плацу.
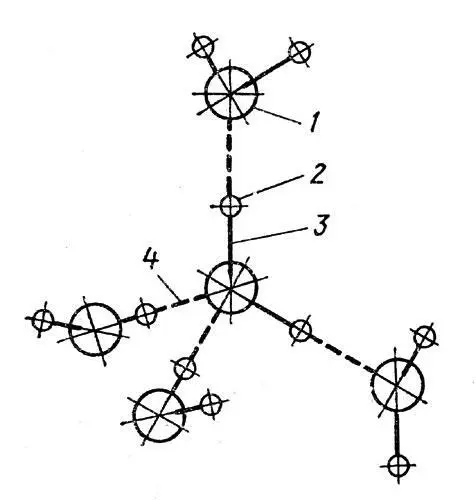
Рис. 11. Образование водородных связей между молекулами воды. 1 - кислород; 2 - водород; 3 - ковалентные связи; 4 - водородные связи. Каждая молекула перекидывает два мостика и одновременно на нее перекидываются два мостика. В результате возникает геометрическая фигура - тетраэдр
Так как для построения тетраэдра молекулы должны вначале отодвинуться одна от другой на определенные расстояния, объем, занимаемый замерзающей водой, естественно, увеличивается. И он будет расти до тех пор, пока вся вода не обратится в лед (рис. 11).
- Но, позвольте! - вправе удивится читатель. - Раз уж в кристаллах льда водородные связи проявили себя в полную силу, где же предсказанная вами "сверхпрочность"? Почему лед не стал прочнее стального сплава?
А потому, дорогой читатель, что в лед перешли все "пороки" воды: растворенные в ней газы и механические примеси. Кристаллическая структура льда полна всевозможных дефектов: трещин, уродливых нагромождений, втиснувшихся в парадный строй кристаллов атомов примесей. И от возможной сверхпрочности не осталось и следа.
Нет, обычным превращением воды в лед сверхпрочности не достичь. Кстати, аналогичную картину мы наблюдаем и в металлургии. Твердеющий расплав - тот же лед. Теория показала, что сталь и даже чистое железо могли бы стать по крайней мере в 1000 раз прочнее, если бы удалось получить идеальную кристаллическую структуру без искажения геометрии кристаллической решетки. Но, увы, здесь, как и в воде, делают свое "грязное" дело газовые включения и посторонние механические примеси.
Раз уж речь зашла о льдах... Чтобы превратить лед в воду, его нужно нагреть. При этом каждый килограмм льда потребует довольно приличного количества тепла - 340 кДж. Однако с оговоркой: 340 кДж, если лед взят при 0°С и при нормальном атмосферном давлении. Для расплавления 1 кг льда, взятого при минус 7°С, достаточно уже 323,24 кДж, а при минус 13°С понадобится еще меньше - 310,7 кДж. Получается, что с каждым градусом вниз по шкале термометра теплота плавления льда убывает на 2,1 кДж.
Не удивительно ли? Чем холоднее лед, тем легче его превратить в воду! Вот вам и еще одно "чудачество" воды, которое может быть объяснено только специфичностью водородных связей.
Как странно иногда совершаются научные открытия! Сколько мудрецов до Архимеда пользовались ванной, но ни одному из них в голову не приходило усмотреть в льющейся через края воде явление необычайной важности.
А вот пример сегодняшнего дня. Уже не одно столетие клянет человечество воду за ее коварное свойство: замерзая в трубах, рвать их стенки. А сколько нерадивых шоферов и по сей день "размораживает" автомобильные двигатели, оставляя в них зимой воду?
Но почему-то никто, в том числе и мы с вами, не задумывались над тем, какая огромная, не используемая человеком, сила действует на наших глазах.
27 февраля 1974 г. газета "Советская индустрия" сообщила о замечательном изобретении московского инженера П. А. Радченко. Суть изобретения сводится к сварке, с помощью льда! Точнее, с помощью того давления, которое возникает в момент превращения воды в лед. Количество потребляемой воды - объем куриного яйца. Источник холода - в зимнее время воздух с улицы: ведь очень-то низких температур и не требуется - нуля вполне достаточно.
Не даром говорят: "Все великое - просто!"
Водородная связь водородной связи рознь
В наши дни выявилась еще одна (наверняка не последняя!) странность в поведении воды. Оказалось, что в зависимости от способа получения Н 2О может обладать различной силой водородных связей.
Например, талая вода, т. е. вода, образующаяся в момент таяния льда, и она же, взятая спустя некоторое время, - не одна и та же вода. Вообще, по многим общеизвестным физико-химическим свойствам она осталась нашей старой знакомой (по чистоте, плотности, химическому составу и пр.), но претерпела изменение с самом главном - в величине водородных связей между молекулами.
Последнее обстоятельство подтверждается так: чтобы превратить 1 кг обычной (например, водопроводной) воды в пар необходимо 2260 кДж тепла. А для талой воды потребуется уже 2268,38 кДж. Разность в 8,38 кДж при современной измерительной технике - величина весьма заметная.
За счет чего появилась эта разница? Известно, что водородные протоны в молекуле Н 2О ведут себя, подобно двум раскрученным волчкам,- они вращаются вокруг собственных осей и, значит, обладают моментом количества движения или, как принято говорить в молекулярной физике, имеют спин.
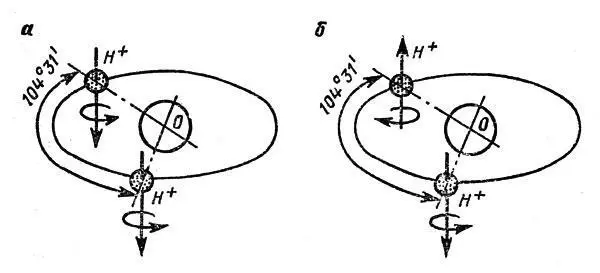
Рис. 12. Два энергетических состояния молекулы Н2О: а - паравода; б - ортовода
Когда протоны вращаются в одну сторону, их моменты складываются, и получается молекула параводы. Если же они вращаются в разные стороны, возникает разность моментов, и получается молекула ортоводы. Схематично обе разновидности молекул показаны на рис. 12. Естественно, молекулы параводы и ортоводы должны находиться на разных энергетических уровнях. Величина того и другого уровней установлена физиками достаточно точно, и ничего неопределенного здесь не осталось.
До сих пор существовало твердое убеждение, что количественное соотношение между пара- и ортомолекулами в природной воде -сохраняется при любых условиях (и зимой и летом) строго постоянным. Действительно, каждый раз эксперименты подтверждали: вода состоит на 3/4 из ортоводы и на 1/4 из параводы. Однако из поля зрения экспериментаторов до сих пор выпадал сущий "пустяк" - момент перехода изо льда в воду. Именно сам момент! Тут-то и обнаружили себя 8,38 кДж. Желание установить свойства воды в момент перехода привело сотрудников лаборатории бионики Казанского университета У. Ахмерова и А. Бильдюковича к смелой догадке: а не происходит ли в талой воде изменение направления вращения одного из водородных протонов молекулы ортоводы и превращения ее в параводу.
Расчеты блестяще подтвердили догадку. Соотношение в талой воде изменилось в пользу параводы и ровно настолько, что энергетический уровень "смеси" повысился как раз на 8,38 кДж. Правда, спустя сутки теплота парообразования талой воды составляла уже 2264,19 кДж, т.е. разница по сравнению с обычной водой снизилась до 4,19 кДж. Еще сутки она едва достигала 2,10 кДж. И так далее, пока соотношение между ортоводой и параводой не пришло в норму (3/4:1/4).
Читать дальшеИнтервал:
Закладка:










