Пекка Теерикор - Эволюция Вселенной и происхождение жизни
- Название:Эволюция Вселенной и происхождение жизни
- Автор:
- Жанр:
- Издательство:Эксмо
- Год:2010
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Пекка Теерикор - Эволюция Вселенной и происхождение жизни краткое содержание
Сэр Исаак Ньютон сказал по поводу открытий знаменитую фразу: «Если я видел дальше других, то потому, что стоял на плечах гигантов».
«Эволюция Вселенной и происхождение жизни — описывает восхождение на эти метафорические плечи, проделанное величайшими учеными, а также увлекательные детали биографии этих мыслителей. Впервые с помощью одной книги читатель может совершить путешествие по истории Вселенной, какой она представлялась на всем пути познания ее природы человеком. Эта книга охватывает всю науку о нашем происхождении — от субатомных частиц к белковым цепочкам, формирующим жизнь, и далее, расширяя масштаб до Вселенной в целом.
«Эволюция Вселенной и происхождение жизни» включает в себя широкий диапазон знаний — от астрономии и физики до химии и биологии. Богатый иллюстративный материал облегчает понимание как фундаментальных, так и современных научных концепций. Текст не перегружен терминами и формулами и прекрасно подходит для всех интересующихся наукой и се историей.
Эволюция Вселенной и происхождение жизни - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Похоже, что требовалось много, а точнее — огромное количество нитей РНК достаточной длины и разнообразия, чтобы создать хотя бы один полимер, способный к самокопированию, а затем и копированию других РНК. Таким образом, требовалось высокоэффективное спонтанное формирование РНК-полимеров, чтобы запустить функционирующий РНК-мир. Предбиологическую полимеризацию нуклеотидов трудно объяснить известной химией РНК, так как для этого нужна энергия, и легко это не происходит. При оптимальных лабораторных условиях удается производить полимеры длиной 4050 нуклеотидов. В этих экспериментах нуклеотиды полимеризуют-ся в водном растворе в присутствии глинистых минералов. Тонкослойные глины из положительно заряженных минеральных частиц связывают отрицательно заряженные нуклеотиды и помещают их в нужное место, способствуя их реакциям между собой. В дальнейшем присутствие глины значительно стабилизирует готовые РНК-полимеры, которые в ином случае могли бы легко разложиться из-за гидролиза. Эти условия «вода-глина» детально исследовал, например, Джеймс Феррис (J. Ferris) из Нью-Йоркского центра изучения происхождения жизни (Политехнический институт Ренсселе).
Группа Дэвида Димера (D. Deamer) из Калифорнийского университета обнаружила иные условия, способствующие полимеризации РНК, хотя и менее успешно, чем глины. В холодных (-18 °C) ледяных растворах исходные вещества концентрируются в воде, остающейся между кристаллами льда. Низкая температура снижает скорость реакций между компонентами и позволяет возникнуть связям между нуклеотидами. В таких условиях за несколько дней появлялись полимеры, содержащие вплоть до 16 нуклеотидов.
Теперь расскажем о проблемах полимеризации. На рис. 30.5 показаны формы субъединиц нуклеозидов и их фосфодиэфирные связи в РНК-полимерах. На этом рисунке изображены и альтернативные строительные блоки, которые не могут быть использованы в РНК-полимерах. Как уже говорилось, РНК-нуклеотиды формируются из оснований — аденина, гуанина, цитозина и урацила, соединенных с сахаром рибозой (см. рис. 28.4 и 28.5). Соседние сахара рибозы должны связываться друг с другом через фосфоризирующие связи между 5'-углеродом одной рибозы с 3'-углеродом предыдущей. Фосфоризирующая связь формируется через фосфатную часть, содержащую фосфор (Р) и кислород (О). Для этого нуклеозиды должны сначала связать фосфатную группу (см. рис. 28.4) или фосфоризироваться своим 5'-углеродом, чтобы затем превратиться в нуклеотиды. На молодой Земле это было затруднительно, так как растворимых фосфатов почти не имелось. Возможно, небольшая часть фосфатов образовалась из неорганических минералов фосфата кальция (гидроксилапатит), хотя они очень плохо растворяются в воде. Возможно также, что фосфаты появились из линейных полифосфатов вулканического происхождения или продуктов их распада. Даже если эти источники обеспечивали нужное количество растворимых фосфатов, то фосфоризация нуклеозидов должна была быть очень затруднена, ведь в лабораторных условиях она может быть завершена только при наличии мочевины, хлористого аммония и тепла. Далее, для полимеризации нуклеотидов нужно еще, чтобы они были активированы какой-нибудь высокоэнергичной связью (например, связью с аналогом основания или аминокислотой) в положении 5', чтобы обеспечить энергией реакции связи между нуклеотидами.
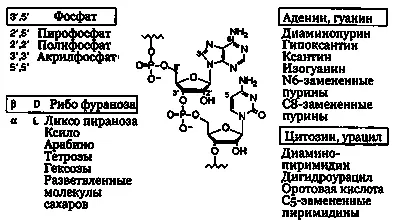
Рис. 30.5. Полимеры, сформированные фосфодиэфирными связями (содержащими фосфор и кислород) между 5'- и 3'-углеродами β-D-нуклеотидов. Нуклеозиды образованы из оснований аденина, гуанина цитозина, урацила и четырехуглеродной циклической формы рибозы в D-ориентации. Перепечатано с разрешения Macmillan Publishers Ltd; G. F. Joyce: The Antiquity ofRNAbased evolution. Nature 418:214, copyright (2002).
Еще одна трудность полимеризации рибонуклеотидов состоит в том, что в смеси мономеров могут происходить различные реакции. Чтобы сформировать функциональный полимер, фосфоризирующие соединения должны образовываться между 5'- и 3'-углеродами соседних нуклеотидов. Но кольцо рибозы имеет реакционноспособные группы ОН у углеродов в положениях 5', 3' и 2. В добиологических условиях между всеми этими группами могли протекать реакции, и в результате внутримолекулярных реакций между ОН-группами в положениях 2' и 3' могли формироваться циклические соединения. Более того, молекулы фосфатов могли создать разные полифосфатные связи между разными углеродами. Все эти разнообразные связи могли привести в тупик дальнейшую полимеризацию.
По мнению Джеральда Джойса (Исследовательский институт Скрипса, Ла-Хойя, Калифорния), ведущего специалиста по добиологической химии РНК, отсутствие специфичности является основной проблемой добиологических реакций. Спонтанные реакции, начавшиеся с синильной кислоты или с цианистого ацетилена, цианита и мочевины, могут дать разные аналоги оснований. Но из всех них только пурины аденин и гуанин, а также пиримидины цитозин и урацил природа использовала для формирования функциональных нуклеозидов. В составе нуклеозидов в добиологических условиях существующие основания могли быть связаны с составляющими рибозы, причем с одинаковым успехом как в а-, так и в р-конфигурациях, а фураноза (четырехуглеродное кольцо) рибозы могла сформироваться как в L-, так и в D-изоформах (лево- и правовращающих плоскость поляризации света, как описано в главе 28). Сахар рибоза также мог сформироваться в виде пятиуглеродного кольца (пираноза) путем соединения 5'- и 1'-углеродов. Добиологические реакции полимеризации между всеми различными аналогами и изоформами нуклеотидов могли привести к большому разнообразию фосфатных соединений разных атомов углерода рибозы. В целом эти реакции могли легко использовать разные варианты пуринов и пиримидинов, связываясь с которыми разные производные разных циклических сахаров формируют L- и D-конфигурации. Эти совершенно случайные аналоги нуклеозидов могут затем фосфорилироваться на разных позициях углерода, и потом опять случайно фосфорилированные аналоги нуклеотидов могли связаться друг с другом разными способами, что показано на рис. 30.5. Ни один из этих альтернативных вариантов не производит функциональноактивные РНК-полимеры.
Только правильно сформированные и полимеризированные нуклеотиды могут быть функциональными шаблонами для репликации через комплементарное спаривание оснований. Мы не понимаем, как жизнь при отсутствии каких-либо ферментных реакций отбора выбирала как раз нужные нуклеотидные компоненты и их специфические изоформы и как она контролировала формирование фосфоризующих связей только между 5'- и 3'-углеродами нуклеотидов.
Читать дальшеИнтервал:
Закладка:








