Ларс Орстрём - Химия навсегда. О гороховом супе, опасности утреннего кофе и пробе мистера Марша
- Название:Химия навсегда. О гороховом супе, опасности утреннего кофе и пробе мистера Марша
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:2021
- ISBN:978-5-389-19541-7
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ларс Орстрём - Химия навсегда. О гороховом супе, опасности утреннего кофе и пробе мистера Марша краткое содержание
Химия навсегда. О гороховом супе, опасности утреннего кофе и пробе мистера Марша - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Если мы направим узкий рентгеновский луч на кристалл, фотоны луча станут отталкиваться от атомов, с которыми будут сталкиваться, – или, вернее, от их электронов. Некоторые на поверхности, некоторые в первом слое, некоторые в следующем и так далее. Если поместить позади кристалла фотографическую пластину (или еще какой-нибудь чувствительный элемент), в его центре мы увидим большое пятно от луча, который проходит через кристалл, а также более бледные пятна вокруг него. Эти смещенные от центра пятна возникают от фотонов, которые по пути столкнулись с атомом. Из-за того, что световые волны прошли разные расстояния, максимумы и минимумы волны (своеобразные «пики» и «ущелья») теперь находятся не там же, где у лучей, которые отражались от верхнего слоя и слоя, следующего за ним, и которые преодолели чуть большее расстояние.
Для обычного света это расхождение настолько мало, что оно не имеет значения, но поскольку длина волны рентгеновских лучей близка к внутримолекулярным и межмолекулярным расстояниям между атомами, то разница в преодоленном пути может достигать половины длины волны. Когда такие комбинации лучей выходят из кристалла и снова соединяются, образуя отраженный луч, максимум волны в одном отражении теперь совпадает с минимумом волны в другом отражении – две волны гасят друг друга, и пятно на пленке не появится. Это явление известно как деструктивная интерференция.
С другой стороны, если разница в пройденном расстоянии составляет одну, две, три или любое другое целочисленное значение длины волны, для фотонов максимумы совпадут, и они окажутся «в фазе». Это конструктивная интерференция, а кристаллографы просто скажут, что в таких случаях вы видите дифракционный пик . Измерив интенсивность и расположение таких пиков (дифракционную картину) на фотопленке, отец и сын Брэгг в 1913 году смогли определить расположение ионов натрия и хлора в кристаллах столовой соли и таким образом стали первыми людьми, которые «увидели» атом [94] Hildebrandt G. The Discovery of the Diffraction of X-rays in Crystals – A Historical Review // Crystal Research and Technology, 28 (747). 1993.
. В настоящее время широко распространены ПЗС-детекторы вроде тех, что используются в цифровых фотоаппаратах, чтобы регистрировать эти пятна.
Несмотря на разговор о пиках и ущельях, мы забрели далеко от афганских гор. Я сделал это для того, чтобы вы смогли оценить истинную красоту ляпис-лазури (а вернее, минерала лазурита), великолепного синего компонента лазуритовых руд, потому что он бесконечно более тонкий и сложный, чем король драгоценных камней алмаз. Еще до Первой мировой войны отец и сын Брэгг смогли определить положение атомов углерода в алмазе при помощи фотопленки, карандаша и бумаги, но кристаллографы до сих пор бьются над определением структуры лазурита.
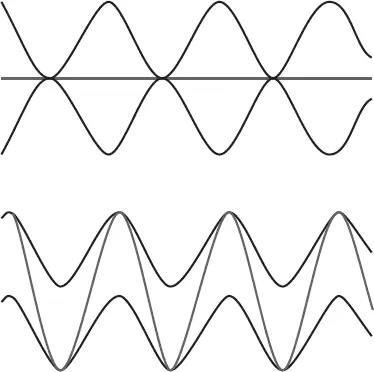
Рисунок 17.Вверху: максимумы и минимумы волн, которые совмещаются со сдвигом ровно на половину длины волны (серая линия), гасят друг друга и дают нулевой сигнал. Внизу: совпадающие по фазе совмещения усиливаются и дают мощный сигнал (серая волна).
Лазурит – сложный минерал, потому что его химическая формула изменчива. В отличие от алмаза – просто «С» – мы обычно записываем лазурит как Na 6Ca 2(Al 6Si 6O 24)[(SO 4), S, Cl, (OH)] 2, где точное количество последних четырех составляющих варьируется в зависимости от типа горной породы [95] В качестве примера, объясняющего принципы кристаллографии, это не лучшее соединение, так как оно несколько сложнее, чем среднестатистический кристалл. Вы можете представить себе, что меняющийся состав – это солдаты на параде, некоторые из которых надели другие фуражки и создали другой порядок в дополнение к тем, что стоят плечом к плечу в четких шеренгах и рядах. Технический термин для этого – «несоразмерная модуляция», и мои друзья-кристаллографы радостно сообщили мне, что тут все понятно: вы просто перемещаетесь в четвертое или пятое пространственное измерение.
. Почему же это вещество ведет себя так странно, не подчиняясь закону постоянства состава, который мы изучали в школе? Причина – пространственная структура фрагмента Al 6Si 6O 24. Ее можно достаточно просто определить на основе рентгеновской дифракционной картины: вы увидите бесконечную взаимосвязанную структуру, состоящую из тетраэдров AlO 4и SiO 4, где каждый атом кислорода служит мостиком в паре ионов металлов Al/Si [96] Hassan I., Peterson R.C., Grundy H.D. The Structure of Lazurite, Ideally Na6Ca2(A16 Si6O24) S2, a Member of the Sodalite Group // Acta Crystallographica, 41 (827). 1985; Arieli D., Vaughan D.E. W., Goldfarb D. New Synthesis and Insight into the Structure of Blue Ultramarine Pigments // Journal of the American Chemical Society, 126 (5776). 2004.
.
Ну и что такого, скажете вы: если вы были внимательны на уроках химии, то знаете, что алмаз тоже состоит из тетраэдров. Но в нашем случае расстояния между центрами ячеек (теми центрами, что связаны с четырьмя другими узлами) гораздо больше, что приводит к возникновению огромных, похожих на клетки областей пустого пространства внутри кристалла. Там мы обнаружим довольно скучные – маленькие и бесцветные – ионы натрия и калия, которые занимают области поменьше, и столь же прозрачные, но более крупные ионы сульфата, хлорида и гидроксида, заключенные в клетки большего размера. Так что же с цветом: значит, его дает каркас из алюминия и кремния? Нет, подобный каркас служит основой для многих минералов. Возможно, ключ к разгадке можно найти в другой составляющей лазурита: в горной породе присутствуют кристаллические частички железного колчедана (пирита, или «золота дураков»). «Золото дураков» не только придает камню красоту, но также может играть важную роль в образовании настоящих пленников этих кристаллических клеток – отрицательно заряженных ионов S 3 – [97] Fleet M.E., Liu X. Absorption Spectroscopy of Ultramarine Pigments: A New Analytical Method for the Polysulfide Radical Anion S3 – chromophore // Spectrochimica Acta Part B, 65 (75). 2010.
, поскольку пирит имеет формулу FeS 2и содержит структурные единицы S-S, которые когда-то могли стать начальной точкой для появления ионов S-S–S –.
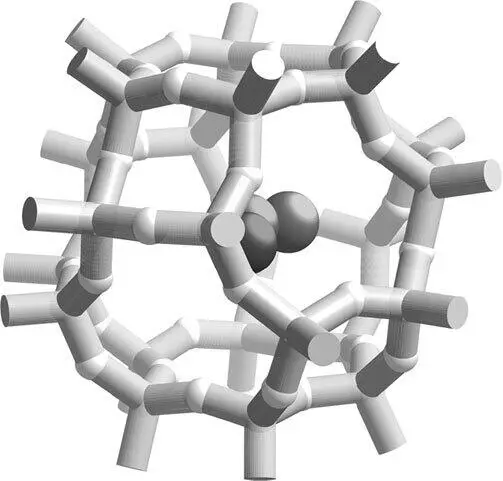
Рисунок 18.Кристаллическая ячейка лазурита из связей Al—O и Si—O и стабилизированный в ней ион-радикал S 3 –, придающий синий цвет ляпис-лазури (три более темные сферы).
Эти необычные частицы существуют в кристалле лишь в очень малых количествах, и их требуется держать в клетке-ловушке, поскольку это радикалы. (На самом деле химия не настолько консервативна, чтобы считать, что всех радикалов нужно держать под замком; дело просто в том, что молекулу, содержащую неспаренные электроны, мы называем радикалом, и такие ребята обычно весьма активны.) Вы, вероятно, слышали о «свободных радикалах», всячески вредящих вашему организму. Это радикалы ОН; а ион S 3 –представляет собой другую разновидность подобных частиц. Он придает синий цвет лазуриту, однако, если выпустить его из клетки, он будет немедленно разрушен и цвета исчезнут. Часть секрета изготовления из лазурита хорошей краски, вероятно, заключается в том, чтобы этого не случилось по ходу дела.
Читать дальшеИнтервал:
Закладка:










