Ник Лэйн - Кислород. Молекула, изменившая мир
- Название:Кислород. Молекула, изменившая мир
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:2016
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ник Лэйн - Кислород. Молекула, изменившая мир краткое содержание
Ник Лэйн ответит на вопрос: кислород — наш единственный шанс на выживание или самый худший враг?
Кислород. Молекула, изменившая мир - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Что же при этом происходит? В 1925 г. Роберт Малликен смог объяснить магнитные свойства кислорода, применив сформулированную незадолго до того квантовую теорию. Магнитные свойства вещества объясняются спином неспаренного электрона, а как показал Малликен, в молекуле кислорода есть два неспаренных электрона [36] Вокруг вращающейся заряженной частицы образуется магнитное поле. Это справедливо и для электрического тока в катушке проволоки, и для единственного электрона в атоме. Теоретически все химические (ковалентные) связи образованы парами электронов. Электроны в паре обычно имеют противоположно направленные (антипараллельные) спины. Противоположные спины уравновешивают друг друга, так что молекула в целом спином не обладает. По этой причине большинство химических соединений не проявляют магнитных свойств. Обладающие магнитными свойствами атомы или молекулы, такие как железо или кислород, обязательно имеют хотя бы один неспаренный электрон, а такое электронное состояние, как мы видели, является неустойчивым. Однако в соответствии с законами квантовой механики структура кислорода с двумя неспаренными электронами значительно устойчивее, чем структура с обычной двойной связью, о которой всем нам рассказывали в школе (см. рис. 8).
. Именно они определяют химические свойства этого элемента и усложняют получение молекулярным кислородом других электронов для образования химических связей (рис. 8). Из данного химического тупика есть два выхода. Во-первых, кислород может получить энергию от другой молекулы, возбужденной теплом или светом, что изменит спин одного из неспаренных электронов кислорода. Такое действие оказывают некоторые пигменты, что используется для фотодинамической терапии, основанной на способности активированного светом пигмента разрушать опухоли или другие патологические ткани.
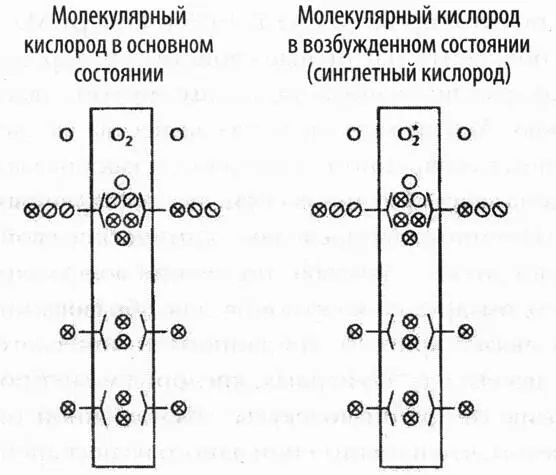
Изменение спина одного электрона приводит к образованию электронной пары и освобождению одной орбитали, что позволяет кислороду вступать в реакции (снимаются так называемые спиновые ограничения). Кислород в такой форме называют синглетным кислородом . Он быстро реагирует с органическими молекулами. Если бы синглетный кислород был единственной формой кислорода, он никогда бы не накапливался ни в атмосфере, ни в океане.
Второй способ заставить кислород вступать в химические реакции заключается в том, чтобы передавать ему дополнительные электроны по одному, так чтобы каждый из двух неспаренных электронов получил подходящего партнера независимо от другого. Это может делать железо, поскольку оно имеет собственные неспаренные электроны (которые объясняют его магнитные свойства) и существует в разных состояниях окисления, которые в нормальных условиях характеризуются примерно одинаковой энергетической стабильностью. (Отчасти дело в том, что атом железа большой и удаленные от ядра электроны связаны с ним не очень прочно.) Способность железа передавать электроны по одному объясняет его сродство к кислороду и ржавление железных изделий и минералов. С этим же связана необходимость прятать железо в организме в молекулярные ловушки. Некоторые другие металлы, например медь, которые тоже могут существовать в двух или нескольких степенях окисления, эффективно передают электроны кислороду и поэтому в свободном виде тоже опасны.
Живые системы вынуждены учитывать странные химические свойства кислорода и, чтобы заставить его реагировать, передают ему электроны по одному. Клетки научились разделять процесс окисления пищи на отдельные стадии, на каждой из которых выделяется некоторое количество энергии, запасаемой в виде молекул АТФ (см. главу 3). К сожалению, на каждой стадии могут выделяться одиночные электроны, способные присоединяться к кислороду с образованием супероксидных радикалов. Непрерывное возникновение супероксидных радикалов в клетках означает, что, как ни странно, дыхание таит в себе ту же опасность, что и облучение.
Когда мы находимся в состоянии покоя, от 1 до 2% поглощенного клетками кислорода выделяется в виде супероксидных радикалов, а при физической активности этот показатель может достигать 10%. Эти цифры не кажутся угрожающими, но следует помнить, что при каждом вдохе мы поглощаем много кислорода. Взрослый человек с массой тела 70 кг за минуту вдыхает около четверти литра кислорода. Даже если лишь 1% превращается в супероксидные радикалы, за год человек производит 1,7 килограмма этих частиц. А из супероксидных радикалов в соответствии с приведенными выше реакциями могут возникать гидроксильные радикалы и пероксид водорода.
Они могут возникать, но возникают ли они на самом деле? Человеческий организм выработал эффективные механизмы устранения супероксидных радикалов и пероксида водорода до того, как они встретятся с железом и образуют гидроксильные радикалы (подробнее об этих механизмах мы поговорим в главе 10). Можно ли оценить, сколько гидроксильных радикалов все же образуется в организме, несмотря на указанные защитные механизмы?
К решению этой задачи можно подойти с двух сторон. Во-первых, теоретически мы способны рассчитать скорость образования гидроксильных радикалов на основе оценочных значений стационарной концентрации пероксида водорода и железа и известной кинетики реакции. По-видимому, в теле человека пероксид водорода и железо содержатся в стационарной концентрации около миллионной части грамма на килограмм массы тела. Это означает, что в организме образуется меньше 10 -12г гидроксильных радикалов на килограмм массы тела в секунду. Представить себе столь малую величину невозможно, но, если с помощью числа Авогадро перевести количество граммов в количество молекул, получаем значительно более понятное значение: в каждой клетке человеческого тела за секунду образуется примерно 50 гидроксильных радикалов [37] Число Авогадро — количество молекул в одном моле любого вещества; численное значение 6,023 × 10 23 . Один моль вещества — это его молекулярная масса, выраженная в граммах. Молекулярная масса гидроксильного радикала 17, так что моль гидроксильных радикалов весит 17 г. Это означает, что в 17 г гидроксильных радикалов содержится 6,023 × 10 23 гидроксильных радикалов. Средний объем клетки млекопитающего составляет от 10 -9 до 10 -8 мл. Данный расчет (с модификациями) взят из книги Холлиуэлла и Гаттриджа «Свободные радикалы в биологии и медицине», см. список литературы в конце книги.
. Это означает, что за сутки каждая клетка выделяет 4 млн гидроксильных радикалов! Многие из них нейтрализуются тем или иным способом, а поврежденные молекулы ДНК или белков заменяются новыми, но со временем в организме, состоящем из 15 × 10 12клеток, накапливаются повреждения, которые вполне могут быть причиной старения.
Интервал:
Закладка:




![Ник Лэйн - Вопрос жизни [Энергия, эволюция и происхождение сложности]](/books/1098393/nik-lejn-vopros-zhizni-energiya-evolyuciya-i-proisho.webp)





