А. Дроздов - Неорганическая химия
- Название:Неорганическая химия
- Автор:
- Жанр:
- Издательство:Конспекты, шпаргалки, учебники «ЭКСМО»b4455b31-6e46-102c-b0cc-edc40df1930e
- Год:2008
- Город:Москва
- ISBN:978-5-699-26628-9
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
А. Дроздов - Неорганическая химия краткое содержание
Информативные ответы на все вопросы курса «Неорганическая химия» в соответствии с Государственным образовательным стандартом.
Неорганическая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
14б Влияние на растворимость природы компо–нентов
Способность веществ растворяться определяется характером сил взаимодействия между молекулами компонентов раствора X 1и Х 2: растворитель – раство–ритель (X 1– X 1), растворенное вещество – растворен–ное вещество (Х 2– Х 2), растворитель – растворенное вещество (Х 1– Х 2) (точки обозначают молекулярную связь).
Растворимость веществ колеблется в широких пре–делах. В примерах приведена растворимость различных солей в одном и том же растворителе (воде) и раство–римость одного и того же вещества (AgNО 3) в различных растворителях.
Вещества с ионным типом связи и вещества, состоя–щие из полярных молекул, лучше растворяются в поляр–ных растворителях, таких как вода, спирты. Эти раство–рители характеризуются высокой диэлектрической проницаемостью.
Высокая растворимость веществ довольно часто обус–ловлена образованием межмолекулярных, в частности водородных, связей. Так, неограниченная взаимная раст–воримость воды и спирта объясняется образованием водородных связей между молекулами воды и спирта, а растворение кристаллов AgcI в водном растворе ам–миака объясняется образованием химической донор-но-акцепторной связи иона серебра с молекулами ам–миака (AgCI в воде практически нерастворим). По этой же причине в пиридине – растворителе с низкой диэлек–трической проницаемостью – обнаруживается очень высокая растворимость.
Так как растворимость характеризует истинное рав–новесие, влияние внешних условий на это состояние (давления, температуры) можно качественно оценить, воспользовавшись принципом Ле Шателье. Подобные оценки необходимы в практике глубоководных погруже–ний, при работе в горячих цехах и т. п.
15. Растворимость газов в жидкостях. Законы Генри—Дальтона и Сеченова
Растворение газов в жидкостях почти всегда сопро–вождается выделением теплоты. Поэтому раствори–мость газов с повышением температуры согласно принципу Ле Шателье понижается. Эту закономер–ность часто используют для удаления растворенных га–зов из воды (например С0 2 ) кипячением. Иногда рас–творение газа сопровождается поглощением теплоты (например, растворение благородных газов в некото–рых органических растворителях). В этом случае повы–шение температуры увеличивает растворимость газа.
Газ не растворяется в жидкости беспредельно. При не–которой концентрации газа X устанавливается равно–весие:
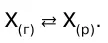
При растворении газа в жидкости происходит значи–тельное уменьшение объема системы. Поэтому повы–шение давления согласно принципу Ле Шателье долж–но приводить к смещению равновесия вправо, т. е. к увеличению растворимости газа. Если газ малораст–ворим в данной жидкости и давление невелико, то растворимость газа пропорциональна его давлению. Эта зависимость выражается законом Генри (1803г.): количество газа, растворенного при данной тем–пературе в определенном объеме жидкости, при равновесии прямо пропорционально давлению газа.
Закон Генри может быть записан в следующей форме:
с (Х)= K r(X) × P (X)
где – концентрация газа в насыщенном раство–ре, моль/л;
P (X)– давление газа X над раствором, Па;
K r(X)– постоянная Генри для газа X, моль×л-1 × Па -1.
Константа Генри зависит от природы газа, рас–творителя и температуры.
Закон Генри справедлив лишь для сравнительно раз–бавленных растворов, при невысоких давлениях и отсут–ствии химического взаимодействия между молекулами растворяемого газа и растворителем.
Закон Генри является частным случаем общего закона Дальтона. Если речь идет о растворении не одного газооб–разного вещества, а смеси газов, то растворимость каж–дого компонента подчиняется закону Дальтона: раство–римость каждого из компонентов газовой смеси при постоянной температуре пропорциональна парциаль–ному давлению компонента над жидкостью и не зави–сит от общего давления смеси и индивидуальности других компонентов.
Иначе говоря, в случае растворения смеси газов в жидкости в математическое выражение закона Генри вместо подставляют парциальное давление р! дан–ного компонента.
Под парциальным давлением компонента понимают долю давления компонента от общего давления газовой смеси:
Р i/ Р общ
Парциальное давление компонента рассчитывают по формуле
Изучая растворимость газов в жидкостях в присутст–вии электролитов, русский врач-физиолог И. М. Сече–нов (1829—1905) установил следующую закономерность (закон Сеченова): растворимость газов в жидкостях в присутствии электролитов понижается; происходит высаливание газов.
Р i= Р общ×(X i)
где p i– парциальное давление компонента Х i;
Р общ– общее давление газовой смеси;
х(Х i) – молярная доля i-ого компонента.
Изучая растворимость газов в жидкостях в присутствии электролитов, русский враччфизиолог И. М. Сеченов (1829—1905) установил следующую закономерность (закон Сеченова): растворимость газов в жидкостях в присутствии электролитов понижается; происходит высаливание газов.
16. Роль диффузии в процессах переноса веществ в биологических системах
Диффузия играет важную роль в биологических си–стемах. Прежде всего перемещение питательных ве–ществ и продуктов обмена в тканевых жидкостях проис–ходит посредством диффузии. Кроме того, во многих случаях скорость физико-химических процессов в жи–вых организмах определяется скоростью диффузии реа–гирующих веществ, так как диффузия реагентов, как правило, является наиболее медленной стадией про–цесса, в то время как биохимические реакции при учас–тии ферментов протекают очень быстро.
Всякая живая клетка окружена мембраной, которая служит для защиты и регуляции внутриклеточной сре–ды. Вещества проходят через мембраны по двум ос–новным механизмам: путем обычной диффузии (пас–сивный транспорт) и энергетически активированного переноса (активный транспорт).
Внутренний слой мембраны состоит из углеводород–ных цепей. Поэтому многие небольшие нейтральные молекулы и неполярные молекулы НМС растворимы в этом слое и могут проходить через мембрану путем обычной диффузии по градиенту концентрации. Такой транспорт веществ называется пассивным.
Диффузия играет большую роль в процессе насыще–ния крови кислородом в легких. Вследствие большой разветвленности поверхность альвеол легких велика (~ 80 м 2 ), поэтому кислород активно растворяется в плаз–ме и попадает в эритроциты. Венозная кровь обеднена кислородом – концентрация кислорода в венозной крови стремится к нулю. Следовательно, градиент кон–центрации кислорода между атмосферой и кровью, по–ступающей в легкие, высокий, что приводит к активно–му поглощению (по закону Фика).
Читать дальшеИнтервал:
Закладка:










