Гдаль Оксенгендлер - Яды и противоядия
- Название:Яды и противоядия
- Автор:
- Жанр:
- Издательство:Наука
- Год:1982
- Город:Ленинград
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Гдаль Оксенгендлер - Яды и противоядия краткое содержание
В книге на примерах распространенных отравлений рассматриваются сущность и особенности взаимодействия реактивных структур организма, ядов и противоядий. Освещаются пути и характер научного поиска токсикологов, химиков, биохимиков, фармакологов в раскрытии молекулярных механизмов токсических процессов. В связи с расширяющимся внедрением химических веществ в различные сферы человеческой деятельности особое место в книге занимает описание достижений науки и практики в создании эффективных антидотов, характеризуются возможности и перспективы их применения.
Яды и противоядия - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
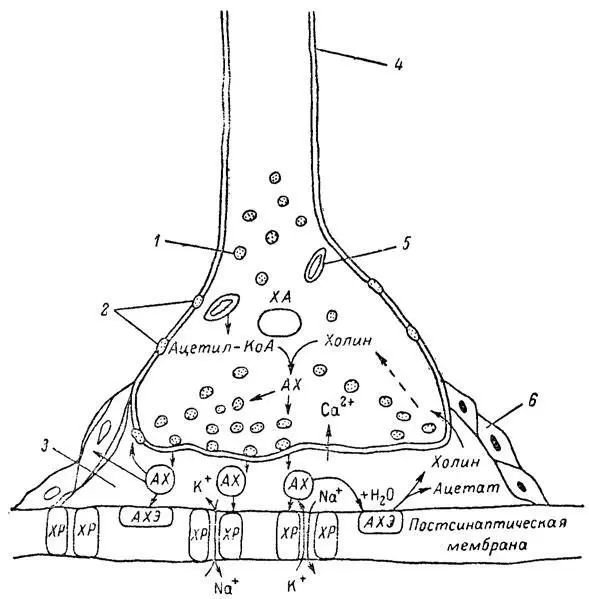
Молекулы ацетилхолина, выполнившие свою медиаторную функцию, должны быть немедленно инактивированы, в противном случае будет нарушена дискретность в проведении нервного импульса и проявится избыточная функция холинорецептора. Именно это осуществляет холинэстераза, мгновенно гидролизующая ацетилхолин. Каталитическая активность холинэстеразы превышает почти все известные ферменты: по разным данным, время расщепления одной молекулы ацетилхолина составляет около одной миллисекунды, что соизмеримо со скоростью передачи нервного импульса. Осуществление столь мощного каталитического эффекта обеспечивается наличием в молекуле холинэстеразы определенных участков (активных центров), обладающих исключительно хорошо выраженной реакционной способностью по отношению к ацетилхолину. [73] Розенгарт В. И. Холинэстеразы. Функциональная роль и клиническое значение. — В кн.: Проблемы медицинской химии. М.: Медицина, 1973, с. 66–104.
Будучи простым белком (протеином), состоящим только из одних аминокислот, молекула холинэстеразы, как теперь выяснено, исходя из ее молекулярной массы, содержит от 30 до 50 таких активных центров.
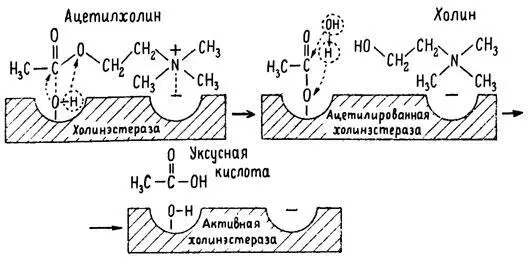
Как видно из рис. 6, участок поверхности холинэстеразы, непосредственно контактирующий с каждой молекулой медиатора, включает 2 центра, расположенных на расстоянии 0,4–0,5 мм: анионный, несущий отрицательный заряд, и эстеразный. Каждый из этих центров образован определенными группами атомов аминокислот, составляющих структуру фермента (гидроксилом, карбоксилом и др.). Ацетилхолин благодаря положительно заряженному атому азота (так называемой катионной головки) ориентируется за счет электростатических сил на поверхности холинэстеразы. При этом расстояние между атомом азота и кислотной группой медиатора соответствует расстоянию между активными центрами фермента. Анионный центр притягивает к себе катионную головку ацетилхолина и тем самым способствует сближению его эфирной группировки с эстеразным центром фермента. Затем рвется эфирная связь, ацетилхолин разделяется на 2 части: холиновую и уксусную, остаток уксусной кислоты присоединяется к эстеразному центру фермента и образуется так называемая ацетилирозанная холинэстераза. Этот крайне непрочный комплекс мгновенно подвергается спонтанному гидролизу, что освобождает фермент от остатка медиатора и приводит к образованию уксусной кислоты. С данного момента холииэстераза снова способна выполнять каталитическую функцию, а холин и уксусная кислота становятся исходными продуктами синтеза новых молекул ацетилхолина.
Механизм действия фосфорорганических соединений
Многие ФОС вследствие особого химического сродства к холинэстеразе ингибируют, т. е. блокируют, ее молекулы посредством взаимодействия с эстеразным центром. Как это видно из приводимой схемы, молекула фосфорор-ганического яда реагирует с гидроксильной группой фермента, причем анионный его центр участия в реакция не принимает:
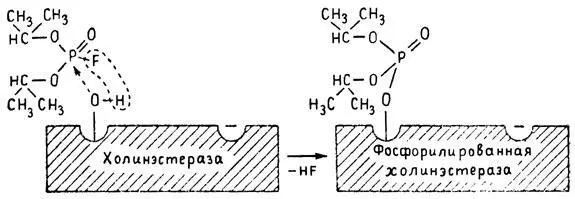
Однако в начале 50-х годов в Швеции в лаборатории Таммелина были синтезированы такие ФОС, которые реагируют и с анионным центром фермента. При этом химики исходили из предположения, что если яд будет сходен по структуре с естественным субстратом холинэстеразы (ацетилхолином), то он окажет на этот фермент более сильное ингибирующее действие. И действительно, такими мощными антихолинэстеразными веществами оказались соединения, которые содержат в своем составе остаток холина, как например метилфторфосфорилхолин. Совершенно естественно, что при его взаимодействии с холинэстеразой положительно заряженный атом азота будет реагировать с анионным центром фермента. Это обеспечивает дополнительный контакт яда с активной поверхностью холинэстеразы и делает связь между ними более прочной:
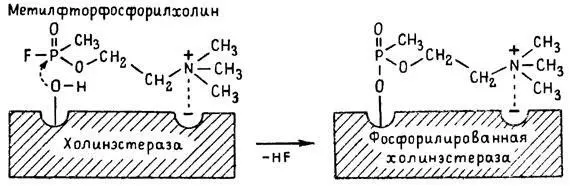
Можно представить также одномоментное ингибирование одной молекулой метилфторфосфорилхолнна двух молекул фермента: одну по анионному, вторую — по эстеразному центру. Как бы то ни было, яды Таммелина оказались в десятки раз более токсичными, чем даже такое сильнодействующее ФОС, как зарин. Образовавшаяся фосфорилированная холинэстераза в отличие от ацетилированной является соединением достаточно прочным и не подвергается самопроизвольному гидролизу. Оказалось, что процесс ингибирования холинэстеразы является двухэтапным. Вначале, на первом этапе, происходит обратимое, т. е. непрочное, ее блокирование, и лишь на втором этапе наступает необратимое блокирование фермента. Оба эти этапа являются результатом сложной, до конца еще не выясненной молекулярной перестройка в комплексе «ФОС-холинэстераза». Забегая несколько вперед, отметим значимость данного явления для практики применения некоторых антидотов, действие которых заключается в разрыве химической связи между ядом и ферментом. Таким образом, под влиянием антихолинэсте — разных веществ тормозится разрушение молекул ацетилхолина и он продолжает оказывать непрерывное действие на холинорецепторы. Отсюда следует, что отравление ФОС есть не что иное, как генерализованное перевозбуждение холинорецепторов, вызванное интоксикацией эндогенным, т. е. имеющим внутреннее происхождение, ацетилхолином. Вот почему основные симптомы отравления ФОС можно трактовать как проявление избыточной, нецелесообразной для организма деятельности ряда структур и органов, которая обеспечивается ацетилхолиновой медиацией (прежде всего это — функция нервных клеток, поперечнополосатых и гладких мышц, различных желез).
В настоящее время имеются доказательства непосредственного возбуждающего влияния некоторых ФОС на холинорецепторы. Тем самым не исключается, что ФОС оказывают токсический эффект, минуя холинэстеразный механизм:
Читать дальшеИнтервал:
Закладка:









