Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Цианистые соединения железа. При действии на растворы солей железа (II) растворимых цианидов, например цианида калия, получается белый осадок цианида железа(II):
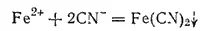
В избытке цианида калия осадок растворяется вследствие образования комплексной соли K 4[Fe(CN) 6] гексацианоферрата (II) калия
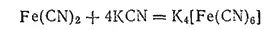
или
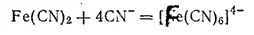
Гексацианоферрат(II) калия K 4[Fe(CN) 6]·3H 2O кристаллизуется в виде больших светло-желтых призм. Эта соль называется также желтой кровяной солью. При растворении в воде соль диссоциирует на ионы калия и чрезвычайно устойчивые комплексные ионы [Fe(CN) 6] 4-. Практически такой раствор совершенно не содержит ионов Fe 2+и не дает реакций, характерных для железа(II).
Гексацианоферрат (II) калия служит чувствительным реактивом на ионы железа(III), так как ионы [Fe(CN) 6] 4-, взаимодействуя с ионами Fe 3+, образуют нерастворимую в воде соль гексацианоферрат(II) железа (III) Fe 4[Fe(CN) 6] 3характерного синего цвета; эта соль получила название берлинской лазури:
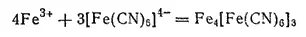
Берлинская лазурь применяется в качестве краски.
При действии хлора или брома на раствор желтой кровяной соли анион ее окисляется, превращаясь в [Fe(CN) 6] 3-
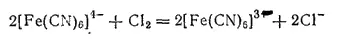
Соответствующая этому аниону соль K 3[Fe(CN) 6] называется гексацианоферратом(III) калия, или красной кровяной солью. Она образует красные безводные кристаллы.
- 671 -
Если подействовать гексацианоферратом(III) калия на раствор соли железа(II), то получается осадок гексацианоферрата (III), железа (И) (турнбулева синь), внешне очень похожий на берлинскую лазурь, но имеющий иной состав:
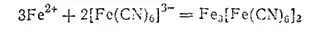
С солями железа (III) K 3[Fe(CN) 6] образует зеленовато-бурый раствор.
В большинстве других комплексных соединений, как и в рассмотренных цианоферратах, координационное число железа(II) и железа(III) равно шести.
Ферриты. При сплавлении оксида железа(III) с карбонатами натрия или калия образуются ферриты — соли не полученной в свободном состоянии железистой кислоты HFeO 2, например феррит натрия NaFeO 2:
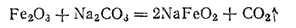
В технике ферритами или ферритными материалами называют продукты спекания порошков оксида железа(III) и оксидов некоторых двухвалентных металлов, например никеля, цинка, марганца. Спекание производится при 1000-1400°C. Ферриты обладают ценными магнитными свойствами и высоким электрическим сопротивлением, что обусловливает небольшую величину электрических потерь в них. Ферриты широко применяются в технике связи, счетно-решающих устройствах, в автоматике и телемеханике.
Если нагревать стальные опилки или оксид железа(III) с нитратом и гидроксидом калия, то образуется сплав, содержащий феррат калия K 2FeO 4— соль железной кислоты H 2FeO 4:
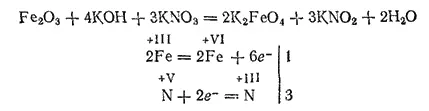
При растворении сплава в воде получается красно-фиолетовый раствор, из которого действием хлорида бария можно осадить нерастворимый в воде феррат бария BaFeO 4.
Все ферраты — очень сильные окислители (более сильные, чем перманганаты). Соответствующая ферратам железная кислота H 2FeO 4и ее ангидрид FeO 3в свободном состоянии не получены.
Карбонилы железа. Железо образует летучие соединения с оксидом углерода, называемые карбонилами железа. Пентакарбонил железа Fe(CO) 5представляет собой бледно-желтую жидкость, кипящую при 105°C, нерастворимую в воде, но растворимую во многих органических растворителях. Fe(CO) 5получают пропусканием СО над порошком железа при 150-200°C и давлении 10 МПа. Примеси, содержащиеся в железе, не вступают в реакции с СО, вследствие чего получается весьма чистый продукт. При нагревании в вакууме пентакарбонил железа разлагается на железо и СО; это используется для получения высокочистого порошкового железа — карбонильного железа (см. § 193).
Природа химических связей в молекуле Fe(CO) 5рассмотрена на стр. 430.
- 672 -
243. Кобальт (Cobaltum).
В природе кобальт мало распространен: содержание его в земной коре составляет около 0,004; (масс.). Чаще всего кобальт встречается в соединении с мышьяком в виде минералов кобальтовый шпейс CoAs 2и кобальтовый блеск CaAs.
Кобальт — твердый, тягучий, похожий на железо блестящий металл. Как и железо, он обладает магнитными свойствами. Вода и воздух на него не действуют. В разбавленных кислотах кобальт растворяется значительно труднее, чем железо.
Кобальт применяется главным образом в сплавах, которые используются в качестве жаропрочных и жаростойких материалов, для изготовления постоянных магнитов и режущих инструментов. Жаропрочный и жаростойкий сплав виталлиум содержит 60% Co, 28% Cr, 3% W и 4% Mo. Этот сплав сохраняет высокую прочность и не поддается коррозии при температурах до 800-850°C. Твердые сплавы стеллиты, содержащие 40-60% Co, 20-35% Cr, 5-20% W и 1-2% C, применяются для изготовления режущего инструмента. Кобальт входит также в состав керамикометаллических твердых сплавов — керметов (см. стр. 639). Соединения кобальта придают стеклу темно-синюю окраску (вследствие образования силиката кобальта). Такое стекло, истолченное в порошок, употребляется под названием «шмальты» или «кобальта» в качестве синей краски. Радиоактивный изотоп 60Co применяется в медицине как источник γ-излучения («кобальтовая пушка»).
Кобальт образует оксид кобальта(II), или закись кобальта, CoO и оксид кобальта (III), или окись кобальта, Co 2O 3, которым соответствуют гидроксиды Co(OH) 2и Co(OH) 3. Этим соединениям отвечают два ряда солей, но соли кобальта(III) нестойки и легко переходят в соли кобальта(II). Известен также смешанный оксид Co 3O 4(или CoO·Co 2O 3).
Соли кобальта(II) в безводном состоянии обычно синего цвета, а их водные растворы и кристаллогидраты имеют розовый цвет; например, хлорид кобальта (II) образует розовые кристаллы состава CoCl 2·6H 2O. Фильтровальная бумага, пропитанная раствором этой соли и потом высушенная, может служить грубым гигроскопом (указателем влажности), так как в зависимости от содержания влаги в воздухе принимает разные оттенки цветов — от синего до розового.
Читать дальшеИнтервал:
Закладка:






