Олег Спиридонов - Людвиг Больцман: Жизнь гения физики и трагедия творца
- Название:Людвиг Больцман: Жизнь гения физики и трагедия творца
- Автор:
- Жанр:
- Издательство:Книжный дом «ЛИБРОКОМ»
- Год:2013
- Город:М.
- ISBN:978-5-397-04175-1
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Олег Спиридонов - Людвиг Больцман: Жизнь гения физики и трагедия творца краткое содержание
Книга рассчитана на широкий круг читателей, интересующихся историей развития физики; может быть полезна студентам и аспирантам физико-математических вузов.
Людвиг Больцман: Жизнь гения физики и трагедия творца - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Дальнейшее развитие атомистической гипотезы было небезмятежным. В 1808 г. французский ученый Ж. Л. Гей-Люссак открыл закон объемных отношений, согласно которому объемы как участвующих в реакции газов, так и газообразных продуктов реакции находятся в простых кратных отношениях. Это противоречило теории Дальтона, в которой соединялись равные количества атомов, и… Дальтон отказывается признавать закон Гей-Люссака. Но один-единственный факт, не укладывающийся в какую-либо теорию, способен опровергнуть ее.
После открытия Гей-Люссака судьба всей атомной теории вызвала сомнения.
«Существует огромная разница между фантазиями натурфилософов, легкомысленно сбивающихся с пути опыта, и надежными выводами теоретической физики, медленно и методически продвигающейся вперед пол непрестанным контролем эксперимента. Последняя позволяет проникать глубоко в тайны природы, не теряя надежной почвы пол ногами, и в этом она достигает своих высших триумфов».
Блестящим подтверждением этих слов может служить гениальная идея итальянского ученого А. Авогадро (1776-1856). В 1811 г. он указал на возможность создания новой теории, объединяющей две существующие теории — Дальтона и Гей-Люссака. Авогадро вводит в науку о строении вещества понятие молекулы — соединения атомов. Удивительное предвидение! Еще под вопросом реальность атомов, а результаты исследований требуют объяснения и находят его в созданной Авогадро молекулярной теории строения вещества.
Важнейшим следствием гипотезы Авогадро является закон, имеющий громадное теоретическое значение, — при одинаковых температуре и давлении равные объемы любых газов содержат одно и то же число молекул! Этот вывод закреплял в науке представление о дискретном, зернистом, строении вещества. Используя данные опытов Дальтона и Гей-Люссака, Авогадро возводит удивительно стройное «молекулярное здание», предсказывая новые, уникальные факты.
Из гипотезы Авогадро вытекает существование постоянного числа молекул в моле [2] Моль — количество вещества, содержащее столько же молекул или атомов, сколько содержится атомов в углероде массой 0,012 кг.
любого вещества. Объем V 0, который занимает моль любого газа при нормальных условиях, также является постоянным. Этот объем был измерен экспериментально:
Одной из самых первоначальных задач науки стало определение числа молекул N Aв 1 моле любого вещества, получившего в дальнейшем название постоянной Авогадро. Зная V 0и N A, мы можем рассчитать важнейшие характеристики атомов — их массы, размеры, среднее расстояние между атомами в газах. Выполним эти расчеты.
Предположим, что постоянная Авогадро нам известна (о способах ее определения можно узнать в школьных учебниках физики):
Поскольку масса одного моля водорода равна 2,016 г и в нем содержится N A молекул, то масса одной молекулы водорода будет равна m H2= 3,35∙10 -24г, а масса одного атома m H= 1,675∙10 -24г. Поразительно могущество теории — мы «взвесили» атом водорода, не прибегая к помощи весов (да и возможны ли весы, способные взвешивать столь ничтожные тела?).
Оценим размеры атомов. Объем воды, равный 1 см 3, составляет 1/18 часть моля, поэтому в нем содержится 3,34∙10 22молекул. Объем, приходящийся на одну молекулу воды, равен (1/3,34)∙10 22см 3, т.е. примерно 3∙10 -23см 3. Предполагая, что молекулы расположены плотно друг к другу, оценим линейные размеры молекул воды:
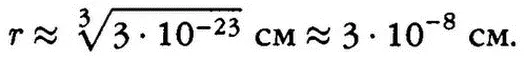
Размеры других атомов и простейших молекул — этого же порядка.
Расстояние между молекулами в газах можно оценить следующим образом:
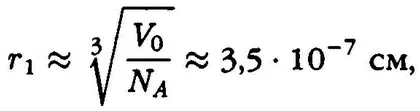
т. е. молекулы в газах находятся друг от друга на расстояниях, примерно в 10 раз больших, чем их собственные размеры.
Введение в химию атомистических представлений позволило ученым добиться несомненных успехов в познании строения вещества, но и поставило перед ними множество трудных вопросов. К открытому Бойлем и Мариоттом закону pV = const спустя почти 150 лет добавился закон Гей-Люссака, связывающий относительное изменение объема газа и его температуру T:
где α — коэффициент термического расширения газов, равный 1/273 К -1. Вскоре французский ученый Э. Клапейрон связал воедино все три параметра газа и получил уравнение состояния идеального газа, которое носит название уравнения Клапейрона:
Для одного моля газа константа в уравнении (5) равна R = 8,31 Дж/моль∙К). Это так называемая универсальная газовая постоянная.
Все эти законы были установлены экспериментально и должны были еще получить теоретическое обоснование. Пока же они порождали много вопросов, например: «Почему эти законы справедливы для всех газов, независимо от их химического состава?» Большие трудности были связаны с пониманием природы давления газов и их температуры. Все эти вопросы ставились на фоне отсутствия прямых экспериментальных доказательств реальности существования атомов. Становилось все более ясным, что искомые ответы можно было получить только при разработке каких-либо представлений о внутреннем строении газов, построении, как говорят, модели реального газа.
Попытаемся создать такую модель. Представим газ в виде собрания большого числа (коллектива) атомов или молекул. Как эти мельчайшие частицы могут образовывать упругую силу, т. е. создавать давление газа? При ходьбе, например, мы совершенно не ощущаем сопротивления воздуха. Но, с другой стороны, накачивая шину, мы ощущаем, как постепенно растет упругое противодействие нашим попыткам сжать ее. Какова природа этой силы?
Рассмотрим пример, который поможет понять сущность газового давления. Представьте себе небольшую мельницу (рис. 2). Возьмите песчинку и бросьте ее на одну из лопастей. Поскольку масса песчинки очень мала, она отскочит от лопасти, мельница останется в покое. Увеличим число падающих на лопасти песчинок. Начиная с некоторого момента мельница начнет вращаться. Мельчайшие по сравнению с массой мельницы песчинки создали вполне реальную силу давления на ее лопасти и явились причиной ее движения.
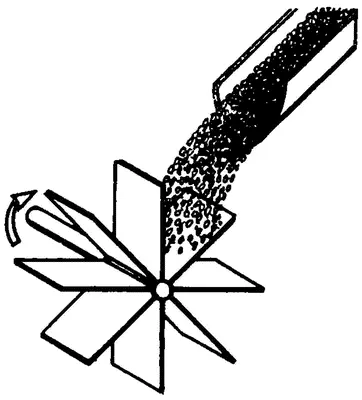
Обратимся к газам. Легко усмотреть аналогию с только что разобранным примером. Частиц газа очень много; так, в объеме 1 м 3при нормальных условиях содержится примерно 2∙10 25молекул. Чтобы создавать давление, частицы газа должны двигаться. Пока в нашем распоряжении нет никаких доказательств их движения, кроме демокритовой догадки. Но позвольте, а разве реально существующее давление газов не есть доказательство их движения? Ведь давление газа можно, по аналогии с опытом с мельницей, представить как результат соударений множества движущихся молекул газа со стенками сосуда.
Читать дальшеИнтервал:
Закладка:










