Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир
- Название:Абсолютный минимум. Как квантовая теория объясняет наш мир
- Автор:
- Жанр:
- Издательство:Питер
- Год:2015
- Город:Санкт-Петербург
- ISBN:978-5-496-01069-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир краткое содержание
Физика — это сложнейшая, комплексная наука, она насколько сложна, настолько и увлекательна. Если отбросить математическую составляющую, физика сразу становится доступной любому человеку, обладающему любопытством и воображением. Мы легко поймём концепцию теории гравитации, обойдясь без сложных математических уравнений. Поэтому всем, кто задумывается о том, что делает ягоды черники синими, а клубники — красными; кто сомневается, что звук распространяется в виде волн; кто интересуется, почему поведение света так отличается от любого другого явления во Вселенной, нужно понять, что всё дело — в квантовой физике. Эта книга представляет (и демистифицирует) для обычных людей волшебный мир квантовой науки, как ни одна другая книга. Она рассказывает о базовых научных понятиях, от световых частиц до состояний материи и причинах негативного влияния парниковых газов, раскрывая каждую тему без использования специфической научной терминологии — примерами из обычной повседневной жизни. Безусловно, книга по квантовой физике не может обойтись без минимального набора формул и уравнений, но это необходимый минимум, понятный большинству читателей. По мнению автора, книга, популяризирующая науку, должна быть доступной, но не опускаться до уровня читателя, а поднимать и развивать его интеллект и общий культурный уровень. Написанная в лучших традициях Стивена Хокинга и Льюиса Томаса, книга популяризирует увлекательные открытия из области квантовой физики и химии, сочетая представления и суждения современных учёных с яркими и наглядными примерами из повседневной жизни.
Абсолютный минимум. Как квантовая теория объясняет наш мир - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Из чего состоят жировые молекулы?
Слыша слово «жир», вы, вероятно, думаете о сливочном масле, сале, оливковом или хлопковом масле. Каждое из них в действительности представляет собой смесь различных жиров. На рис. 16.1 изображена одна конкретная молекула жира {28} 28 Точнее, молекула жирной кислоты. В английском языке термин fat (жир) может относиться к жирным кислотам, а не только к состоящим из них триглицеридам (о которых речь в конце главы), как в русском языке. В переводе такое упрощённое словоупотребление сохранено лишь там, где оно не приводит к недоразумениям, то есть в основном в диетологическом контексте. — Примеч. пер.
. Это стеариновая кислота. Она представляет собой длинную углеводородную цепочку с кислотной органической группой на конце. Стеариновая кислота содержит 18 атомов углерода. Крайний справа атом углерода входит в состав органической кислотной группы. На рис. 15.4 (внизу) изображена молекула уксусной кислоты, которая представляет собой кислотную группу с присоединённой к ней метильной группой. На рис. 15.5 изображён тетрадекан — входящий в состав нефти углеводород, который содержит 14 атомов углерода. Стеариновая кислота подобна уксусной кислоте, но вместо одиночной метильной группы к кислотной группе присоединена цепочка из 17 атомов углерода. Можно также рассматривать стеариновую кислоту как относительно длинный углеводород тетрадекан с кислотной группой на конце. В общем, жирная кислота — это длинная углеводородная цепочка с органической кислотной группой на одном из концов. Эта кислотная группа образует водородные связи с водой. Как говорилось в главе 15, уксусная кислота растворима в воде благодаря сильным водородным связям между кислотной группой и молекулами воды. Стеариновая кислота, как и жирные кислоты вообще, нерастворима в воде из-за длинной углеводородной цепочки. Хотя кислотная группа сильно взаимодействует с водой (гидрофильна), длинная углеводородная цепочка, подобно обсуждавшимся в главе 15 углеводородам, избегает взаимодействия с водой (гидрофобна). У жирных кислот влияние длинной углеводородной части молекулы перевешивает, и в общем случае они не растворяются в воде.
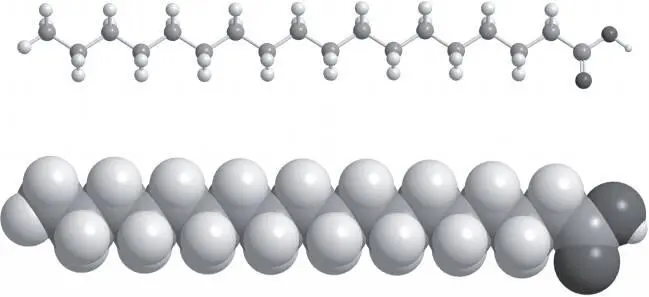
Рис. 16.1. Шаростержневая (вверху) и объёмная (внизу) модели стеариновой кислоты. Стеариновая кислота содержит 18 атомов углерода, 36 атомов водорода и два атома кислорода. Это 17-углеродный углеводород с кислотной группой −COOH на конце (справа)
Насыщенные и ненасыщенные жирные кислоты
Стеариновая кислота является насыщенной. Все атомы углерода в ней связаны с одним или двумя другими соседними углеродными атомами одиночной связью. Двойных связей между атомами углерода нет. К насыщенным относят такие жиры, в молекулах которых между атомами углерода есть лишь одиночные связи.
На рис. 16.2 изображена шаростержневая модель олеиновой (масляной) кислоты. Олеиновая кислота, как и стеариновая, содержит 18 атомов углерода и кислотную группу на конце. Однако у неё имеется двойная связь между девятым и десятым атомами углерода (нумерация начинается от атома углерода в составе карбоксильной кислотной группы {29} 29 Карбоксильная группа — группа −COOH, характерная для класса карбоновых кислот, к числу которых относятся жирные кислоты. — Примеч. пер.
). Олеиновая кислота — мононенасыщенная. Она является ненасыщенной, потому что имеет двойную связь, и моно ненасыщенной, потому что такая связь только одна . В насыщенных жирах нет двойных связей между атомами углерода.
В стеариновой кислоте все атомы углерода, кроме входящего в кислотную группу, используют для образования связей четыре гибридные sp 3-орбитали. Атомы углерода, которые не находятся на концах молекулы стеариновой кислоты, используют две из четырёх гибридных sp 3-обиталей для образования одиночных связей с двумя соседними атомами углерода и две другие для связей с атомами водорода.
Все атомы углерода, кроме входящего в кислотный остаток, имеют тетраэдрическую конфигурацию связей с другими атомами углерода и водорода. В олеиновой кислоте девятый и десятый атомы углерода используют три гибридные sp 2-орбитали для образования σ-связей — одной с водородом и двух с соседними атомами углерода. Остающиеся 2 p -орбитали девятый и десятый атомы углерода используют для образования между собой π-связи. Таким образом, девятый и десятый атомы углерода соединены двойной связью и имеют треугольную, а не тетраэдрическую конфигурацию связей. Это различие в геометрии отчётливо видно на рис. 14.14 при сравнении моделей этана (одиночная углерод-углеродная связь) и этилена (двойная углерод-углеродная связь). В этане углеродные центры тетраэдрические, в этилене — треугольные. Олеиновая кислота содержит 34 атома водорода против 36 в стеариновой кислоте. В олеиновой кислоте для образования двойной связи используются две орбитали, которые в стеариновой кислоте служат для присоединения атомов водорода. Насыщенные жиры содержат максимально возможное число атомов водорода, что означает отсутствие двойных связей.
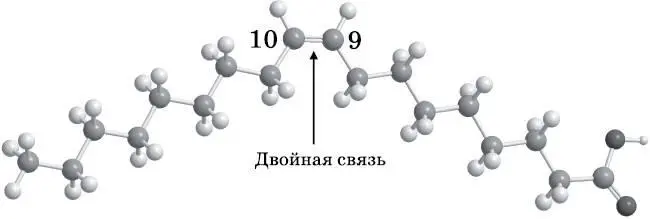
Рис. 16.2. Шаростержневая модель олеиновой кислоты. Олеиновая кислота содержит 18 атомов углерода подобно стеариновой кислоте на рис. 16.1, но у неё есть одна двойная углерод-углеродная связь между девятым и десятым атомами углерода, считая от кислотной группы
Формы жировых молекул
Стеариновая кислота, изображённая на рис. 16.1, целиком находится в транс-конформации. На рис. 14.13 изображена молекула бутана в транс-конформации, но с поворотом вокруг одной из связей, дающим гош-конформацию. Молекула стеариновой кислоты может принимать множество конформаций, помимо изображённой чистой транс-конформации. Для насыщенных углеводородов и насыщенных жирных кислот чистая транс-конформация является самой прямолинейной и низкоэнергетической. В силу наличия только одиночных углерод-углеродных связей насыщенные жирные кислоты постоянно переходят из одной конформации в другую. На рис. 15.7 изображён гептадеканацетат в конформации, которая не является чистой транс-конформацией.
В отличие от стеариновой кислоты олеиновая кислота (см. рис. 16.2) не может естественным образом находиться в чистой транс-конформации. На рис. 16.2 углы между атомами углерода 8, 9 и 10, а также 9, 10 и 11 составляют 120° (что соответствует треугольнику), а не 109,5° (что характерно для тетраэдра). Таким образом, в нормальных биологических условиях добавление одной двойной связи фиксирует конкретную форму молекулы вблизи этой связи.
Читать дальшеИнтервал:
Закладка:










