Enrique Alvarez - Масса атомов. Дальтон. Атомная теория
- Название:Масса атомов. Дальтон. Атомная теория
- Автор:
- Жанр:
- Издательство:Де Агостини
- Год:2014
- Город:М.
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Enrique Alvarez - Масса атомов. Дальтон. Атомная теория краткое содержание
Джон Дальтон является основоположником атомной теории и одним из создателей современной химии. Преподаватель скромной начальной школы Манчестера обратился к идеям, сформулированным за тысячу лет до него Демокритом и другими греческими философами, и предположил, что весь мир состоит из неделимых атомов и в результате их взаимодействия появляются элементы, которые, в свою очередь, образуют химические соединения. Несмотря на то что существование атомов вызывало серьезные споры вплоть до начала XX века — то есть и через 100 лет после публикации труда Дальтона, — именно работа этого просветителя, не получившего университетского образования, легла в основу концептуальной революции, изменившей лицо науки.
Масса атомов. Дальтон. Атомная теория - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Открытие электрона было еще впереди. Только в 1897 году Джозеф Джон Томсон (1856-1940), лауреат Нобелевской премии по физике 1906 года, осуществил свой знаменитый опыт с катодными лучами. Его последователем в изучении субатомных частиц был уже неоднократно упоминавшийся Эрнест Резерфорд, директор лаборатории Кавендиша в Кембридже и лауреат Нобелевской премии по химии 1908 года. Резерфорд и его ученик Нильс Бор (1885-1962), лауреат Нобелевской премии по физике 1922 года, в XX веке осуществили нужные опыты и сформулировали положения, необходимые для понимания структуры атома. И хотя потом выяснилось, что атомы, образующие молекулы, способны делиться на другие частицы (протоны и нейтроны, сосредоточенные внутри маленького плотного атомного ядра, и электроны, находящиеся на его периферии), атомная теория Дальтона заложила солидную основу для этих исследований. Как замечают многие авторы, в области химии атом по-прежнему неделим. И только современная физика, изучающая ядерный распад, а также существование изотопов — разновидности атомов, ядерный состав которых и масса меняются в зависимости от количества нейтронов, — частично опровергли огромное наследие Джона Дальтона.
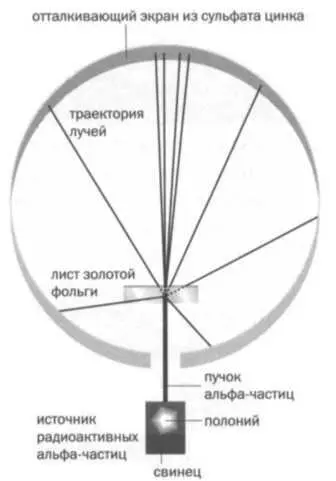
В 1909 году Ханс Гейгер (1882- 1945) и Эрнест Марсден (1889- 1970), ассистенты Резерфорда в Манчестере, осуществили опыт с золотой фольгой. Они разместили естественный источник радиоактивного излучения — полоний Марии Кюри, элемент, все 33 изотопа которого радиоактивны, особенно изотоп 210Ро, — в свинцовую полость ^РЬ. Источник испускал альфа-частицы (ядра гелия), направленный пучок которых попадал через прорезь на золотую фольгу перпендикулярно ее поверхности. В качестве детектора для обнаружения вспышек альфа-частиц исследователи использовали сферический экран из сульфата цинка. Если модель Томсона была правильной и атом являлся однородной структурой, то альфа-частицы не должны были сильно отклоняться. Однако некоторые частицы отклонялись, а одна из восьми тысяч даже отскакивала назад. "Это было почти столь же невероятно, как если бы вы стреляли 15-дюймовым снарядом в кусок тонкой бумаги, а снаряд возвратился бы к вам и нанес удар", — заметил по этому поводу Резерфорд. Из поведения альфа-частиц он заключил, что атом состоит из пустоты и невероятно плотной, крошечной, положительно заряженной центральной зоны.
Ученый продолжал исследования газов и химических соединений до самой смерти в 1844 году, но ни один из его трудов не стал таким же важным, как знаменитая "Новая система химической философии". Став президентом Lit & Phil в 1817 году, Дальтон написал и представил более 120 научных работ. За исключением сэра Гемфри Дэви в первые годы, никто из химиков того времени не ставил под сомнение его атомную теорию, и даже Дэви, похоже, в итоге отказался от своих возражений и предложил Дальтону вступить в Лондонское Королевское общество, президентом которого он являлся. Это был коварный подарок. Дэви знал, что ученый не сможет нести расходы, связанные с этим членством, и откажется. Так и вышло. Однако Дальтон не предполагал, что он будет избран членом общества, даже несмотря на отказ: ученый пользовался все большим уважением, и правительство назначило ему пожизненное денежное содержание, которое существенно облегчило его научные исследования. После смерти Дэви Французская академия наук предложила его пост Дальтону, который до этого, в 1822 году, ненадолго приехал в Париж для встреч с некоторыми авторитетными коллегами. Дальтон испытывал глубокое уважение к Лавуазье, своему несчастному учителю. Кроме того, получив признание, он читал лекции в Оксфорде, Бристоле, Дублине и других городах. К сожалению, слабое сердце вынудило ученого вернуться в промышленный Манчестер, где 27 июля 1844 года он скончался в одиночестве — как, впрочем, и жил. Незадолго до смерти земляки Дальтона в знак признания воздвигли ему огромный памятник. Об удивительных примерах восхищения и признательности жителей Манчестера после смерти Дальтона мы уже говорили в начале этой главы.
Дальтон, возможно, единственный ученый, удостоенный памятника при жизни.
Высказывание неизвестного современника ученого
В дальнейшем некоторые ученые сомневались в существовании атомов. Наибольшую критику высказывал австрийский физик и философ Эрнст Мах (1838-1916), открывший отношение скорости тела к скорости звука. Этот философ-позитивист заявил: "Атомы не подвластны ни одному из органов чувств, они являются лишь плодом разума". Мах утверждал, что в науке следует принимать во внимание лишь то, что можно проверить эмпирически, поэтому отрицал понятия материи, необходимости и казуальности. Атомы Дальтона необходимы для объяснения молекулы, однако сами молекулы являются мыслительными конструктами, и их существование не может быть проверено прямым наблюдением, потому их Мах также не признавал. Эта категоричная точка зрения была распространена среди немецких интеллектуалов, хотя ученый из Вены Людвиг Больцман (1844-1906) ее не разделял.

Джон Дальтон, гравюра Джозефа Аллена (1814).
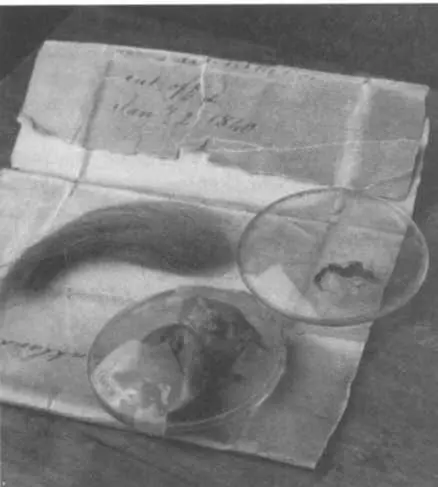
Дальтон первым исследовал дефект, которым страдал сам и который позже был назван дальтонизмом. Он завещал науке собственные глаза —они изображены на рисунке вместе с очками и прядью волос.

Современное здание Религиозного общества Друзей в Манчестере.
Больцман и Мах не были близки ни в личном, ни в профессиональном плане. Больцман основывал свои работы — прежде всего в области статистической механики и термодинамики — на существовании атомов. Это его убеждение полностью разделяли такие признанные ученые, как Джозайя Уиллард Гиббс (1839-1903) и особенно шотландец Джеймс Клерк Максвелл (1831-1879), создатель теории электромагнитного поля. Он работал вместе с Больцманом над кинетической теорией газов, которая сегодня называется статистикой Максвелла — Больцмана. Критика оппонентов, сначала одного его наставника, Эрнста Маха, а затем и второго, Вильгельма Оствальда (1853- 1932), так сильно повлияла на Людвига Больцмана, что он погрузился в депрессию и покончил с собой в 1906 году. Почти в то же время было доказано существование атомов — еще до их бомбардировок частицами, осуществленных Эрнестом Резерфордом. Доказательство представил начинающий исследователь Альберт Эйнштейн (в статье о броуновском движении атомов, опубликованной в 1905 году), а также Жан Батист Перрен в работах по изучению коллоидов, которые позволили подтвердить научную состоятельность постоянной Больцмана и постоянной Авогадро. Постоянная Авогадро — это величина, равная числу структурных элементов (атомов или молекул) в 1 моле вещества. Она не зависит ни от вещества, ни от рассматриваемой частицы и названа в честь итальянца Амедео Авогадро (1776-1856) — странного угрюмого человека, который в 1811 году открыл, что при одинаковых температуре и давлении в равных объемах идеальных газов содержится одинаковое число молекул. Так, 1 моль водорода (Н 2, 2,012 грамма) или 1 моль углерода (С, 12 граммов, взятых как образец) содержат 6, 0221367 х 10 23молекул или атомов. Исходя из этих данных можно измерить размер и массу атомов. Так, две бутылки одинакового размера, одна из которых наполнена кислородом, а другая — гелием, содержат одинаковое количество молекул. Таким образом, число атомов кислорода в два раза больше, поскольку его молекула состоит из двух атомов, тогда как молекула гелия, инертного газа, состоит из одного атома.
Читать дальшеИнтервал:
Закладка: