Андрей Каменский - Биология. Общая биология. 10–11 классы
- Название:Биология. Общая биология. 10–11 классы
- Автор:
- Жанр:
- Издательство:Array Литагент «Дрофа»
- Год:2013
- Город:Москва
- ISBN:978-5-358-11652-8
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Андрей Каменский - Биология. Общая биология. 10–11 классы краткое содержание
Учебник соответствует Федеральному государственному образовательному стандарту среднего (полного) общего образования.
Данная линия учебников (5—11 классы) построена по концентрическому принципу. Учебник для 10—11 классов посвящен проблемам общей биологии, которые освещены в нем более глубоко и подробно, чем в учебнике 9 класса, где учащиеся впервые познакомились с ними, с учетом последних достижений в различных областях биологической науки.
Биология. Общая биология. 10–11 классы - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
§ 8. Минеральные вещества и их роль в клетке
1. Какие вещества называются минеральными?
2. Какой процесс называется диссоциацией?
3. Что такое ионы?
Минеральные вещества клетки.Большая часть минеральных веществ клетки находится в виде солей, диссоциированных на ионы, либо в твёрдом состоянии.
В цитоплазме практически любой клетки имеются кристаллические включения, состоящие, как правило, из слаборастворимых солей кальция и фосфора. Кроме них могут содержаться двуокись кремния и другие неорганические вещества. Они используются для образования опорных структур клетки (например, минеральный скелет радиолярий) и организма – минерального вещества костной ткани (соли кальция и фосфора), раковин моллюсков (соли кальция), хитина (соли кальция) и др.
Неорганические ионы, имеющие немаловажное значение для обеспечения процессов жизнедеятельности клетки, представлены катионами (К +, Na +, Ca 2+, Mg 2+, NH) и анионами (Cl -, HPO, Н 2РО, НСО, NO, PO, СО) минеральных солей. Концентрация катионов и анионов в клетке и в окружающей её среде различна. В результате образуется разность потенциалов между содержимым клетки и окружающей её средой, обеспечивающая такие важные процессы, как раздражимость и передача возбуждения по нерву или мышце.
По своей реакции растворы могут быть кислыми, основными и нейтральными. Кислотность или основность раствора определяется концентрацией в нём ионов Н +. Эту концентрацию выражают при помощи водородного показателя – рН («пэ-аш»). Нейтральной реакции жидкости отвечает рН = 7,0, кислой реакции – рН < 7,0 и основной – рН > 7,0. Протяжённость шкалы рН – от 0 до 14,0.
Значение рН в клетках примерно равно 7,0. Изменение его на одну-две единицы губительно для клетки. Постоянство рН в клетках поддерживается благодаря буферным свойствам их содержимого. Буферным называют раствор, содержащий смесь какой-либо слабой кислоты и её растворимой соли. Когда кислотность (концентрация ионов Н +) увеличивается, свободные анионы, источником которых является соль, легко соединяются со свободными ионами Н +и удаляют их из раствора. Когда кислотность снижается, высвобождаются дополнительные ионы Н +. Так в буферном растворе поддерживается относительно постоянная концентрация ионов Н +. Некоторые органические соединения, в частности белки, также имеют буферные свойства.
Являясь компонентами буферных систем организма, ионы определяют их свойства – способность поддерживать рН на постоянном уровне (близко к нейтральной реакции), несмотря на то что в процессе обмена веществ непрерывно образуются кислые и щелочные продукты. Так, фосфатная буферная система млекопитающих, состоящая из НРО 4 2-и Н 2РО 4 -, поддерживает рН внутриклеточной жидкости в пределах 6,9–7,4. Главной буферной системой внеклеточной среды (плазмы крови) служит бикарбонатная система, состоящая из Н 2СO 3и HCO 4 -и поддерживающая рН на уровне 7,4.
Соединения азота, фосфора, кальция и другие неорганические вещества используются для синтеза органических молекул (аминокислот, белков, нуклеиновых кислот и др.).
Ионы некоторых металлов (Mg, Ca, Fe, Zn, Cu, Mn, Mo, Br, Со) являются компонентами многих ферментов, гормонов и витаминов или активируют их. Например, ион Fe входит в состав гемоглобина крови, ион Zn – гормона инсулина. При их недостатке нарушаются важнейшие процессы жизнедеятельности клетки.
Буферная система.
1. В каком виде минеральные вещества представлены в живых организмах?
2. Какова роль неорганических ионов в клетке?
3. Какова роль ионов в буферных системах организма?
4. Почему недостаток или отсутствие ионов некоторых металлов приводит к нарушению жизнедеятельности клеток?
Важную роль для жизнедеятельности организмов играют неорганические кислоты и их соли. Так, соляная кислота входит в состав желудочного сока и создаёт условия для переваривания белков пищи. Остатки серной кислоты способствуют выведению из организма нерастворимых в воде веществ.
§ 9. Углеводы и их роль в жизнедеятельности клетки
1. Какие вещества, относящиеся к углеводам, вам известны?
2. Какую роль играют углеводы в живом организме?
Углеводы и их классификация. Углеводы, или сахариды, входят в состав клеток всех живых организмов. Содержание углеводов в животных клетках составляет 1–5 %, а в некоторых растительных клетках может достигать до 90 %.
Различают три основных класса углеводов: моносахариды, олигосахариды и полисахариды.
Моносахариды (от греч. monos – один) – бесцветные кристаллические вещества, легко растворимые в воде и имеющие сладкий вкус.
Из моносахаридов наибольшее значение для живых организмов имеют рибоза, дезоксирибоза, глюкоза, фруктоза, галактоза (рис. 8).
Рибоза входит в состав РНК, АТФ, витаминов группы В, ряда ферментов. Дезоксирибоза входит в состав ДНК. Глюкоза (виноградный сахар) является мономером полисахаридов (крахмала, гликогена, целлюлозы). Она есть в клетках всех организмов. Фруктоза входит в состав олигосахаридов, например сахарозы. В свободном виде содержится в клетках растений. Галактоза также входит в состав некоторых олигосахаридов, например лактозы.
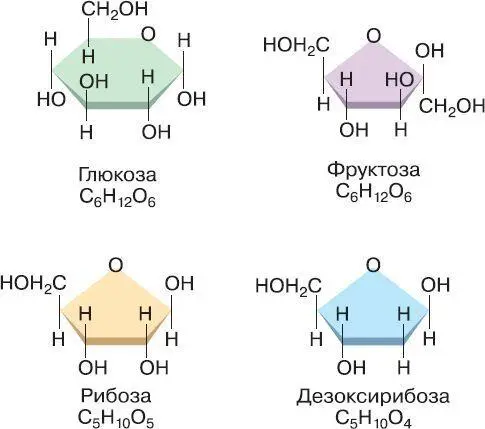
Рис. 8. Моносахариды
Олигосахариды (от греч. oligos – немного) образованы двумя (тогда их называют дисахариды) или несколькими моносахаридами, связанными ковалентно друг с другом с помощью гликозидной связи. Большинство олигосахаридов растворимы в воде и имеют сладкий вкус.
Из олигосахаридов наиболее широко распространены дисахариды: сахароза (тростниковый сахар), мальтоза (солодовый сахар), лактоза (молочный сахар) (рис. 9).
Полисахариды (от греч. poly – много) являются полимерами и состоят из неопределённо большого (до нескольких сотен или тысяч) числа остатков молекул моносахаридов, соединённых ковалентными связями. К ним относятся крахмал, гликоген, целлюлоза, хитин и др. Интересно, что крахмал, гликоген и целлюлоза, играющие важную роль в живых организмах, построены из мономеров глюкозы, но связи в их молекулах различны. Кроме того, у целлюлозы цепи не ветвятся, а у гликогена они ветвятся сильнее, чем у крахмала (рис. 10).
С увеличением количества мономеров растворимость полисахаридов уменьшается и исчезает сладкий вкус.
Некоторые углеводы способны образовывать комплексы с белками (гликопротеиды) и липидами (гликолипиды).
Функции углеводов.Основная функция углеводов – энергетическая. При их ферментативном расщеплении и окислении молекул углеводов выделяется энергия, которая обеспечивает жизнедеятельность организма. При полном расщеплении 1 г углеводов освобождается 17,6 кДж.
Читать дальшеИнтервал:
Закладка: