Оксана Пономаренко - Вопросы и упражнения по дисциплине ВОУД «Неорганическая химия»
- Название:Вопросы и упражнения по дисциплине ВОУД «Неорганическая химия»
- Автор:
- Жанр:
- Издательство:Казахский национальный университет имени аль-Фараби Литагент
- Год:неизвестен
- ISBN:978-601-04-1417-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Оксана Пономаренко - Вопросы и упражнения по дисциплине ВОУД «Неорганическая химия» краткое содержание
Вопросы и упражнения по дисциплине ВОУД «Неорганическая химия» - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
7) окислительные свойства увеличиваются
46. Укажите правильную формулировку периодического закона с точки зрения современной науки:
1) свойства простых тел, а также формы их соединений находятся в периодической зависимости от их атомной массы
2) свойства простых тел, а также формы их соединений находятся в периодической зависимости от суммы их атомных масс
3) свойства простых тел, а также формы их соединений находятся в периодической зависимости от величины заряда ядер их атомов
4) свойства простых тел, а также формы их соединений находятся в периодической зависимости от суммы зарядов их атомов
5) правильный ответ не приведен
47. Укажите правильную формулировку основного положения теории Планка:
1) световая энергия поглощается и излучается непрерывно
2) световая энергия поглощается и излучается не непрерывно, а отдельными неделимыми порциями – квантами
3) световая энергия не поглощается
4) световая энергия излучается непрерывно
5) правильный ответ не приведен
48. Укажите значение постоянной Планка:
1) h = 6.626·10 -27эрг.с
2) h = 0.1·10-10 эрг.с
3) h = const
4) h > 1
5) правильный ответ не приведен
49. В малом периоде с возрастанием порядкового номера химического элемента происходит:
1) уменьшение атомного радиуса
2) уменьшение электроотрицательности атомов
3) возрастание атомного радиуса
4) возрастание электроотрицательности атомов
5) атомные радиусы и электроотрицательность не меняются
6) неметаллические свойства усиливаются
7) восстановительные свойства усиливаются
8) окислительные свойства ослабевают
50. Укажите правильную формулировку модели строения атома Резерфорда:
1) планетарная модель: в центре плотное положительно заряженное ядро, а вокруг ядра, на расстоянии, превышающем размеры ядра в ~ 10000 раз, вращаются легкие отрицательно заряженные электроны
2) положительный заряд размазан по всему атому, отрицательный заряд вкраплен в него
3) электроны по крутой орбите вращаются вокруг ядра
4) электроны имеют двойственный характер: частица и волна. Поэтому атом имеет волновой характер и движение электрона в нем определяется уравнением стоячей волны
5) правильный ответ не приведен
51. Укажите правильное определение постулата Бора:
1) электроны не вращаются вокруг ядра, облако электрона существует самостоятельно
2) электроны вращаются вокруг ядра только по определенным стационарным орбитам, находясь на которых электрон не теряет и не поглощает энергию
3) электрон вращается только вокруг собственной оси
4) электрон вращается вокруг ядра по боровской орбите и непрерывно поглощает энергию
5) электрон вращается только вокруг собственной оси и непрерывно испускает энергию
52. Укажите правильное определение физического смысла квадрата волновой функции │Ψ│2:
1) │Ψ│2 – атомная орбиталь
2) │Ψ│2 – плотность электронного облака между ядром и последним электроном
3) │Ψ│2 – плотность вероятности нахождения электрона в определенной области пространства
4) │Ψ│2 – возбужденная атомная орбиталь
5) │Ψ│2 – форма молекулярной орбитали
53. Сродством к электрону называют:
1) энергию, необходимую для отрыва электрона от невозбужденного атома
2) способность атомов данного элемента притягивать к себе электронную плотность
3) энергию, выделяющуюся при присоединении электрона к атому
4) энергию, которая поглощается при присоединении электрона к атому
5) способность атомов данного элемента смещать от себя электронную плотность
54. Энергией ионизации называют:
1) энергию, необходимую для отрыва электрона от невозбужденного атома
2) способность атомов данного элемента притягивать к себе электронную плотность
3) энергию, выделяющуюся при присоединении электрона к атому
4) энергию, которая поглощается при присоединении элек-трона к атому
5) способность атомов данного элемента смещать от себя электронную плотность
55. Укажите число неспаренных электронов в основном состоянии у атома железа:
1) 2
2) 4
3) 3
4) 7
5) 6
6) 1
7) 5
56. Укажите правильное определение «главного квантового числа» «орбитального (побочного) квантового числа»:
1) размер электронного облака
2) энергетический уровень электрона в атоме, который определяет энергию
3) форма электронного облака
4) магнитное состояние электрона в атоме
5) момент количества движения
6) определяет пространственную форму орбитали
7) энергетический уровень
57. Укажите правильную формулировку правила Клечковского:
1) при одинаковых значениях суммы (n+l) заполнение орбиталей происходит последовательно в направлении воз-растания значения главного квантового числа «n»
2) при одинаковых значениях суммы (n+m) заполнение орбиталей происходит последовательно в направлении возрастания значения главного квантового числа «n»
3) вначале заполняется та орбиталь, у которой значение главного квантового числа «n» меньше
4) при одинаковых значениях суммы (n+s) заполнение орбиталей происходит последовательно в направлении возрастания значения главного квантового числа «n»
5) расположение электронов в периодической системе соответствует электронному строению их атомов
58. Укажите правильное определение «магнитного квантового числа» m:
1) m – момент количества движения
2) m – форма электронного облака
3) m – ориентация электронного облака в пространстве
4) m – энергетический уровень
5) m – энергетический подуровень
59. Укажите правильное определение «спинового квантового числа» S:
1) S – одна из возбужденных атомных орбиталей
2) 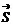 – собственный магнитный момент
– собственный магнитный момент
3) 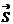 – результат вращения электрона вокруг собственной оси
– результат вращения электрона вокруг собственной оси
4) S – проекция магнитного квантового числа на ось движения
5) S – энергетический подуровень
60. Укажите правильную формулировку принципа Паули:
1) в атоме может быть несколько энергетических уровней с одинаковыми квантовыми числами
2) в атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковыми
3) в атоме может быть только два электрона с одинаковыми квантовыми числами
4) в атоме только на р подуровне могут быть электроны с одинаковыми квантовыми числами
5) правильный ответ не приведен
61. Укажите правильную формулировку «правила Хунда»:
Читать дальшеИнтервал:
Закладка:










